早钟缘何而鸣:饶毅团队揭示MARK2是哺乳动物生物钟蛋白PER2的生理性激酶|Cell Chemical Biology
2026年3月11日,北京脑科学与类脑研究所饶毅团队在Cell Chemical Biology发表题为“Discovery of MARK2 as a physiological kinase for PER2 in the mammalian clock”的研究论文,揭示MARK2是PER2 S662位点的新激酶,证明了其在生物钟调控中的作用。

生物钟对基本生理功能至关重要,其紊乱与睡眠障碍、免疫炎症、代谢紊乱等多种健康问题密切相关。PERIOD2 (PER2) 是生物钟的核心调控蛋白,人类PER2基因第662位丝氨酸突变为甘氨酸(S662G)会导致家族性睡眠状态提前综合征(Familial advanced sleep phase syndrome,FASPS),患者表现为睡眠-觉醒节律比常人提前约4小时,在人群中患病率约为0.21%至0.5%。S662G突变消除了S662位点的磷酸化修饰,而正常情况下,这一位点的磷酸化如同一个“分子开关”,稳定PER2蛋白,维持正常的生物钟周期。早期研究曾认为CK1δ/ε激酶磷酸化PER2,并于2005年被认为PER2 S662的激酶,但2007年同一团队因未能在体外检测到该激酶对PER2 S662肽段的直接磷酸化,又推翻了这一结论,直到2018年,CK1δ/ε磷酸化PER2 S662又再次被证实。饶毅研究团队注意到在CK1δ/ε双敲除的HEK293细胞中,S662位点的磷酸化信号依然存在,提示存在CK1δ/ε以外的新激酶磷酸化S662位点。
研究团队利用磷酸化S662特异性抗体,从50L HEK293细胞裂解液中,通过生物化学纯化技术鉴定出MARK2(属于AMPK相关激酶家族成员)是PER2 S662的新激酶。在细胞中过表达MARK2会增强S662磷酸化水平,而敲除MARK2则降低之;体外实验证实,细菌表达的MARK2的活化突变体直接磷酸化PER2的S662位点。
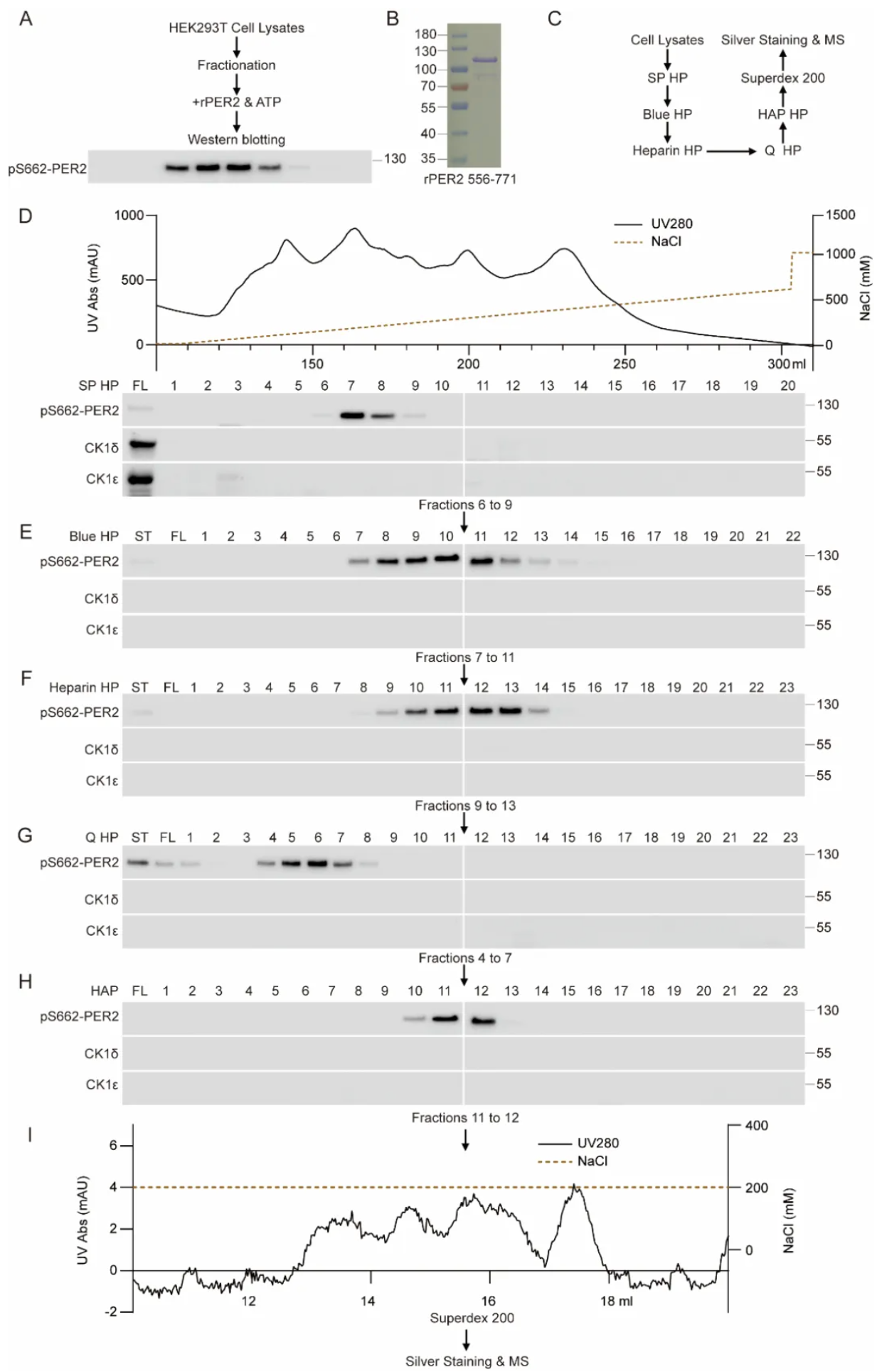
图1 从HEK293细胞中纯化磷酸化PER2 S662的活性组分
MARK2与PER2特异性结合,并通过磷酸化S662位点延缓PER2蛋白的降解。在野生细胞中敲除MARK2导致细胞节律周期缩短,而在引入S662G突变的细胞中再次敲除MARK2,则不再影响细胞节律,表明其调控作用完全依赖于S662位点。
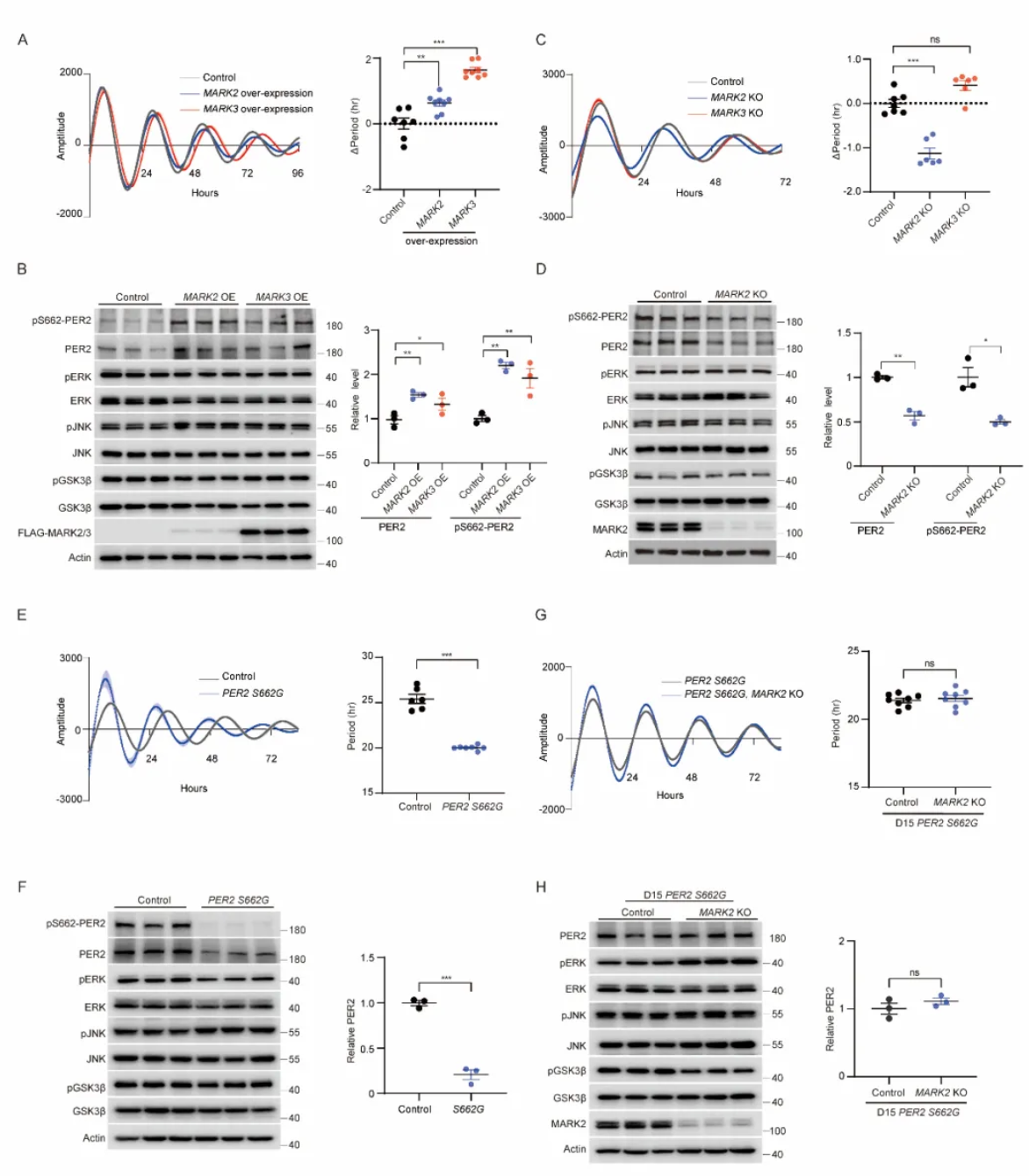
图2 MARK2通过PER2 S662调控细胞节律周期
为进一步验证MARK2的生理功能,构建了神经元特异性Mark2敲除的小鼠。结果显示,敲除小鼠表现出与人类FASPS患者类似表型——即活动起始时间提前、生物钟周期缩短。
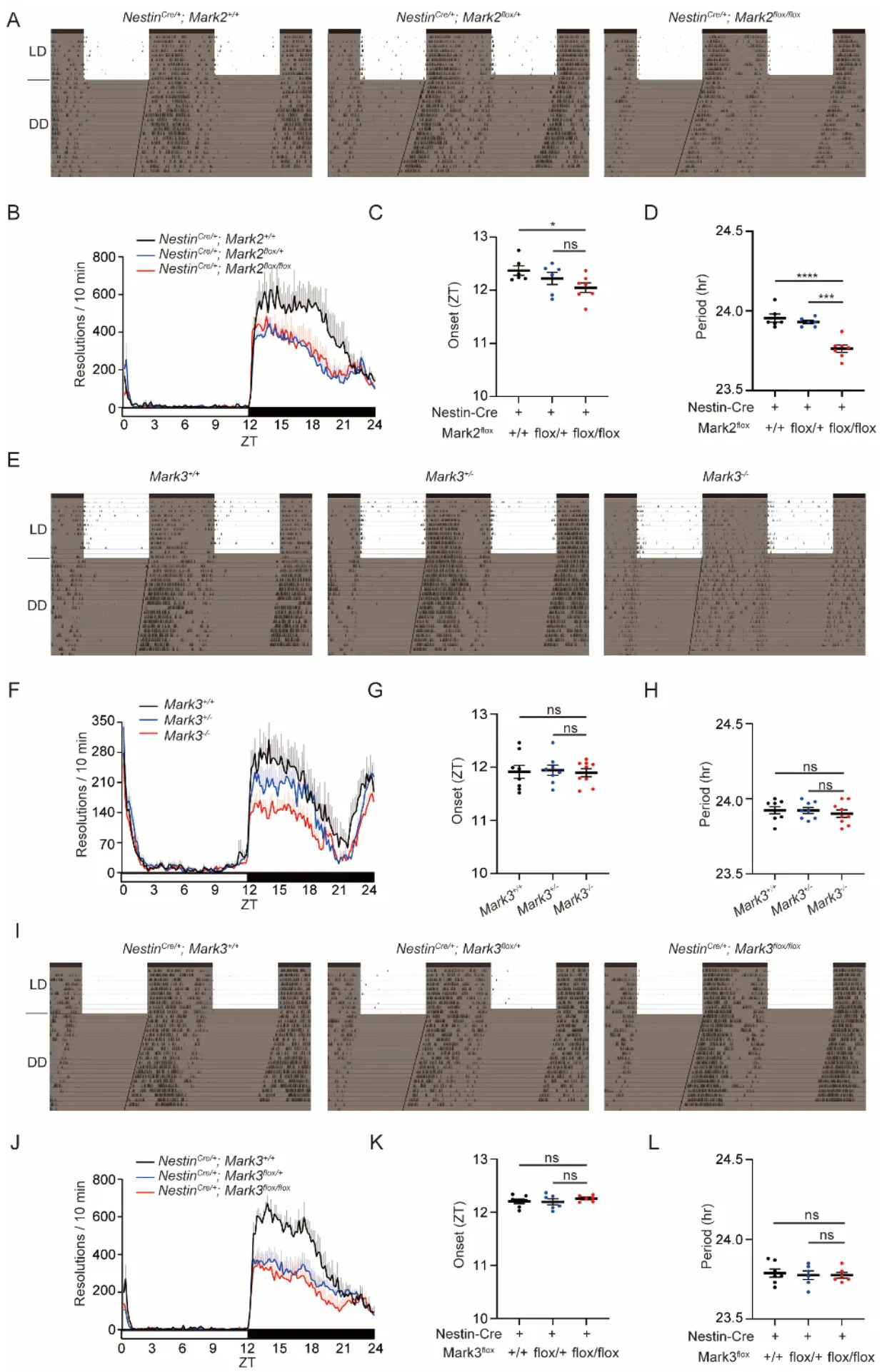
图3 Mark2调控小鼠活动起始时间和生物钟周期
研究还系统评估了所有21种AMPK相关激酶对PER2 S662的磷酸化能力,发现SIK1-3、TSSK1/2等亦可在体外磷酸化该位点。尽管这些激酶在小鼠模型中未表现出明显节律表型,但其体外活性提示可能存在功能冗余或组织特异性调控机制,值得进一步探索。
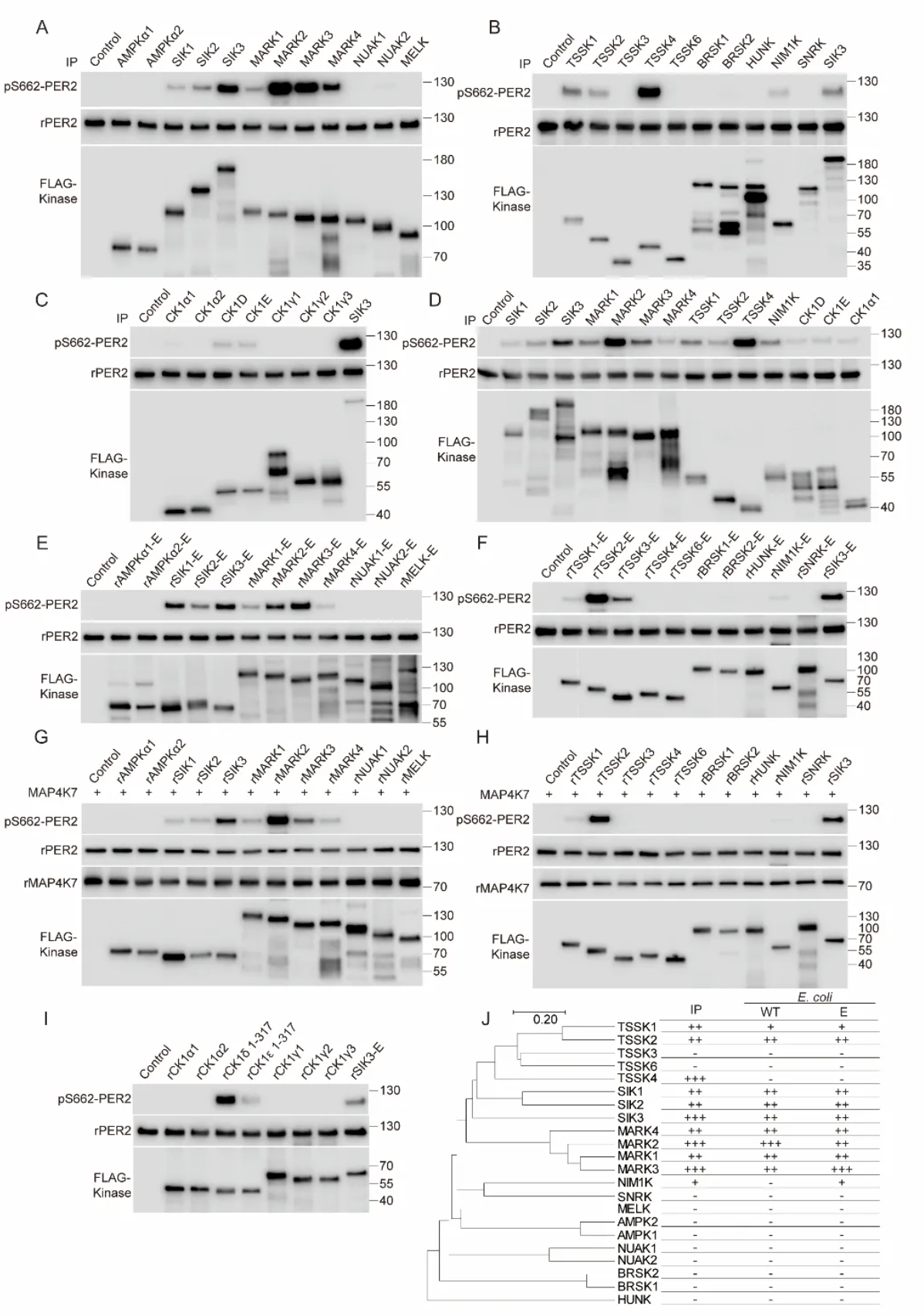
图4.AMPK相关激酶家族对PER2 S662的磷酸化作用
本研究历时14年,最终通过生化方法找到了PER2 S662新的调控激酶——MARK2,并证明了MARK2调控小鼠生物钟,为理解生物钟的精细调控机制提供了全新视角。

论文信息
该研究工作由北京脑科学与类脑研究所饶毅课题组完成,刘玉祥、李扬、余腾辉、王涛为共同第一作者,崔云凤、朱晨、贾晓波、李成钢、沈雨欣、王准、刘尚臣亦有诸多实验贡献,北京脑科学与类脑研究所李佳越为本文配图。研究得到了北京脑科学与类脑研究所遗传操作中心黄娟博士和行为分析中心孙晓敬博士、罗沛宜博士、高子龙博士以及北京大学国家蛋白质科学中心刘栋博士、张琪博士的支持。
原文链接: https://www.cell.com/cell-chemical-biology/fulltext/S2451-9456(26)00062-0



