经典神经毒素竟能抗癌?北京脑所石玮团队揭示6-OHDA激活抗肿瘤免疫新机制|Neuron
2026年3月18日,北京脑科学与类脑研究所石玮课题组在Neuron杂志发表题为"6-Hydroxydopamine promotes antitumor immunity through macrophage remodeling beyond sympathetic ablation"的研究论文。研究发现,神经毒素6-羟基多巴胺(6-OHDA)具有不依赖于交感神经清除的肿瘤免疫调节功能。

交感神经系统在生理或心理压力下可被激活,并通过调节激素分泌、血流及免疫应答等生理过程参与机体稳态维持。回顾性研究提示,慢性压力可能与癌症发病风险上升及预后不良相关。然而,慢性压力影响的生理过程十分广泛,并不仅限于交感神经系统。
基于小鼠模型的临床前研究中,交感神经信号被认为可通过多种途径影响癌症进展,包括直接作用于肿瘤细胞、调控肿瘤血管生成,以及重塑肿瘤免疫微环境等。然而,不同研究结论并不一致:部分报道指出抑制交感神经活动可减缓肿瘤生长,另一些则显示效果有限,甚至可能加速肿瘤进展。上述差异引发了我们对“单纯抑制交感神经活动是否足以有效抑制肿瘤进展”这一问题的深入思考。
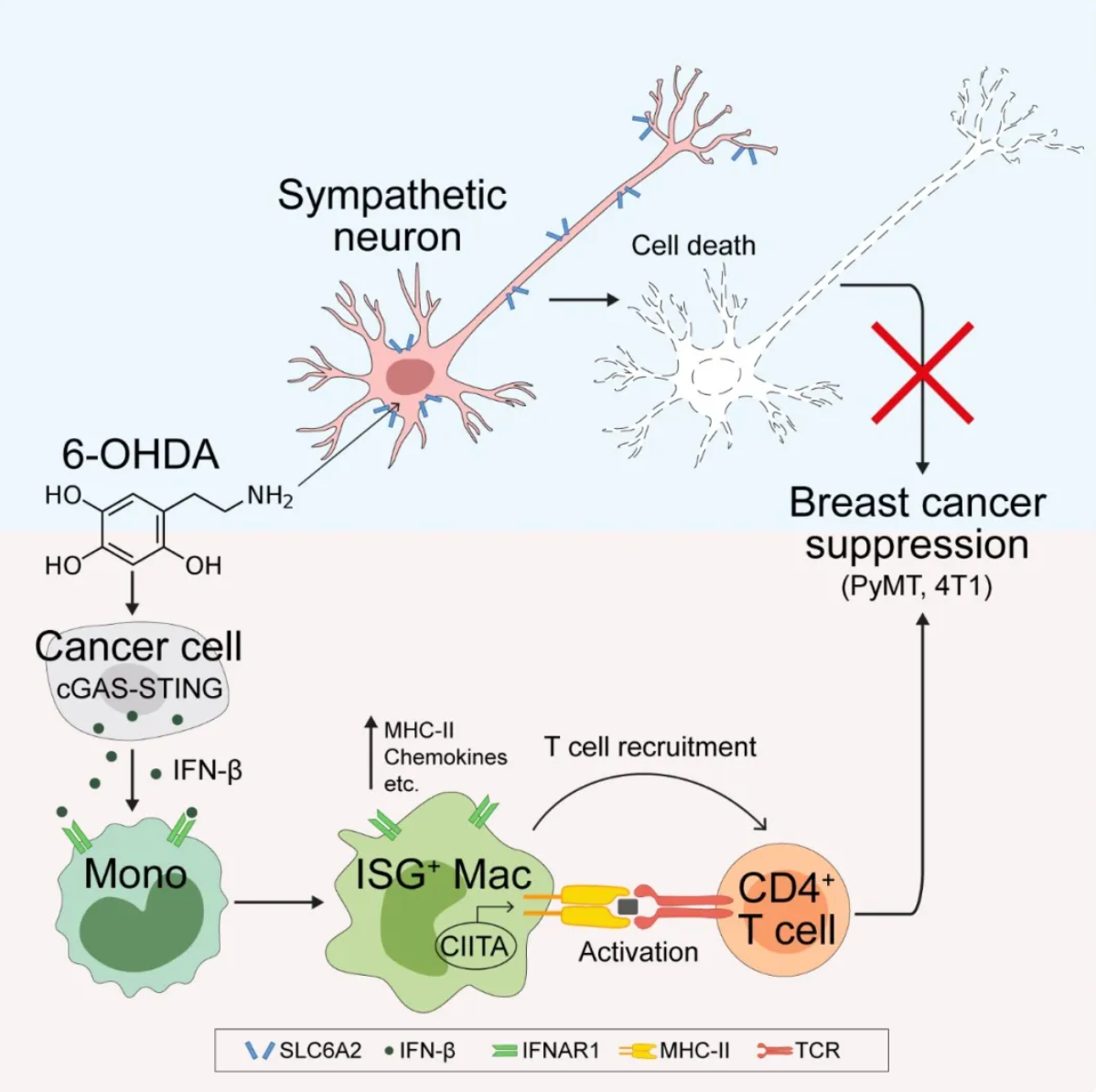
本研究在PyMT自发乳腺癌小鼠模型中,采用遗传学干预、化学药物(6-OHDA)及手术去神经等多种方法清除交感神经,并系统比较了不同清除方法对肿瘤进展的影响。研究意外发现,尽管所有方法均能清除肿瘤内的交感神经投射,仅有6-OHDA处理能够显著抑制PyMT肿瘤进展。6-OHDA的经典神经毒性机制是经由去甲肾上腺素转运体(NET)进入交感神经元,进而诱导神经元死亡。本研究进一步在特异性敲除NET从而保护交感神经元的条件下检测6-OHDA的作用。在这些小鼠中,6-OHDA的交感神经毒性显著减弱,但抗肿瘤效应仍然保留。上述结果提示,6-OHDA的抗肿瘤作用并非由其杀灭交感神经这一经典作用直接介导。
进一步机制研究表明,6-OHDA主要通过免疫激活途径抑制肿瘤进展。具体来说,6-OHDA通过cGAS-STING信号通路,促进肿瘤细胞分泌IFN-β,进而驱动单核细胞向具有干扰素刺激基因(ISG)表达特征的促炎性巨噬细胞(ISG⁺ Macs)分化。这类ISG⁺ Macs对Ⅰ型辅助T细胞(TH1)的扩增起到关键作用,两者共同构成的 “ISG⁺ Macs-TH1轴”介导了持续的抗肿瘤效应。相比之下,单纯去除交感神经并未影响巨噬细胞的分化过程,也未对肿瘤生长产生显著调控作用。
综上所述,本研究揭示,6-OHDA除已知的神经毒性外,还具有重要的免疫调节功能。其所揭示的ISG⁺ Macs-TH1轴可能成为乳腺癌治疗的潜在干预靶点。因此,在未来利用6-OHDA开展神经-免疫互作相关研究时,应谨慎区分其神经毒性效应和免疫调节作用。
论文信息
北京脑科学与类脑研究所博士生于家林和助理研究员张昊博士为论文共同第一作者,北京脑科学与类脑研究所石玮研究员为本文的通讯作者。感谢课题组李美瑶和陈姗姗在本研究做出的重要贡献,感谢MSKCC李明教授的宝贵建议。本研究获得北京市科技新星计划,中国国家自然科学基金及北京脑所的支持。
原文链接: https://www.cell.com/neuron/abstract/S0896-6273(26)00133-9



