北京脑中心2022年代表性科研论文成果
陈坚 研究员

l 北京脑科学与类脑研究中心研究员
代表性成果:ApoE 多肽修饰的CpG纳米免疫佐剂用于恶性脑胶质瘤的靶向治疗
2022年3月7日,陈坚教授和苏州大学材料与化学化工学部孟凤华教授合作在Advanced Science在线发表题为“Immunotherapy of malignant glioma by noninvasive administration of TLR9 agonist CpG nano-immunoadjuvant”的研究论文。
肿瘤免疫治疗通过激活宿主的免疫反应来抑制肿瘤生长从而改善患者的生存,然而恶性脑胶质瘤是一种高度免疫抑制的“冷”肿瘤,内部浸润了大量免疫抑制性的细胞,并且由于血脑屏障的存在,治疗药物很难到达胶质瘤部位。
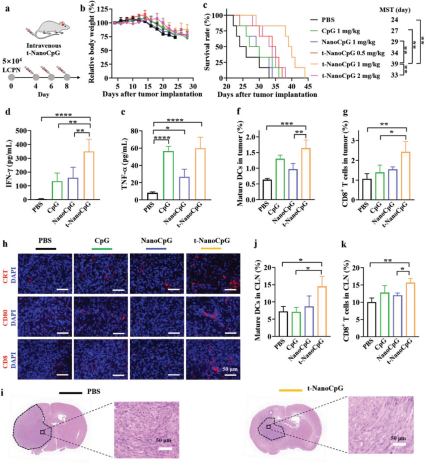
为了能够有效提高免疫治疗的效果,陈坚教授团队和合作者设计了ApoE多肽修饰的双硫交联的具有不对称膜结构的聚合物囊泡,通过静电作用来稳定高效地装载免疫佐剂CpG——Toll 样受体 9(TLR9)激动剂。ApoE-PS-CpG 的粒径较小且均匀(~ 40 nm)、载药量(10-20 wt.%)和载药效率(> 90%)较高。其能在体内高效穿透血脑屏障、靶向胶质瘤,强烈刺激抗原递呈细胞的成熟和促炎细胞因子的分泌。通过低/非侵入性的给药方式递送到原位胶质瘤,避免了侵入性的颅内或鞘内给药带来的低效率和免疫毒性等问题。无论是通过静脉注射还是鼻腔注射,ApoE-PS-CpG 均能显著延长LCPN原位胶质瘤小鼠的生存期,联合放疗后免疫疗效进一步增强。
这种靶向胶质瘤的 CpG 纳米免疫佐剂能实现 CpG对血脑屏障的穿透并防止其体内快速降解,避免了侵入性的颅内或鞘内注射引起的毒副作用,拓宽了 CpG 的应用途径,为胶质瘤的高效免疫治疗提供了一种新的靶向策略。
文章链接:https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202103689
柳昀哲 研究员

l 北京脑科学与类脑研究中心研究员
l 北京师范大学认知神经科学与学习国家重点实验室研究员
代表性成果:提出神经活动解码表征富集理论
2022年3月8日,柳昀哲课题组在Nature Reviews Neuroscience上发表长篇综述,系统整合近年来课题组在神经活动解码方面的重要贡献,并提出表征富集理论(representation-rich)。
早期人们理解人类意识的内涵,主要通过采用主观报告以及其他主观推论等方式,与过去经验相结合,探寻梦境内容所反应出的现实问题。神经科学的出现让我们能采用无创方式对人类认知背后的神经信号进行探索。自时间相关电位、磁共振功能成像、脑磁图等无创神经信号采集范式兴起以来,数以万计的文章采用精妙的实验设计,从时间维度和空间维度对人类的高级认知过程进行了探查。
但一直以来,自发神经活动缺乏实验设计的操纵,人们在自发性活动中引入任务相关的实验刺激,将自发活动人为分割为施加刺激相关的任务诱发实验,这在一定程度上探索了自发神经活动背后的功能意义,但自发神经活动仍然是“黑箱”。
结合表征相似性分析的进展,结合任务诱发的神经信号与自发神经信号,柳昀哲博士及其团队提出表征富集理论(representation-rich)。该理论基于大脑神经信号对于刺激的表征在任务诱发和自发活动下相似的假设,将任务诱发时的神经信号作为特征,解码自发神经活动背后的功能意义。在时间维度上,基于该理论,对于一段时间的自发神经活动进行解码,我们便能够获得自发神经活动的时间维度表征形式,即什么样的神经表征,从何处开始,持续了多久时间。这种在时间维度上的表征特性与动物海马位置细胞研究有相似之处。动物在静息和睡眠状态下,海马通过尖波涟漪进行神经活动重现,从而对于动物探索迷宫的路径信息进行模拟,因此探索迷宫诱发的神经活动会以不同位置信息神经活动重现的形式在海马被解码出来。人类不仅对于位置信息的加工有着相似的机制,对于关联信息特征也存在类似的加工方式,因此,从自发性神经活动中解码任务内容的表征,为我们理解人类高级智能提供了一扇窗,即采用表征富集理论,探究人类神经活动重现的作用与意义。
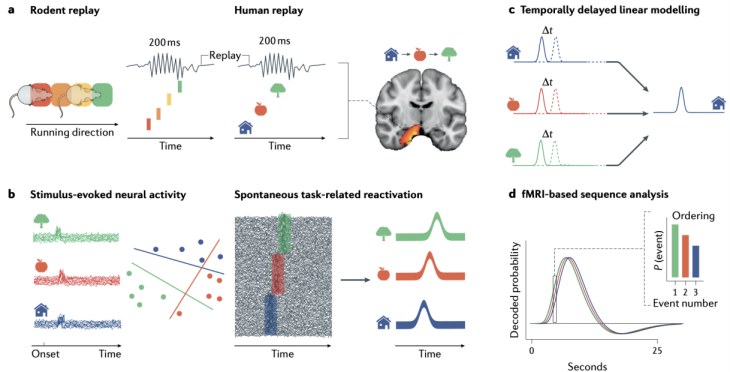
a. 模式动物与人类的神经重现特征。b. 刺激诱发的神经活动与自发神经活动重激活。c. TDLM算法(详情请见Liu et al., 2021 elife)。d. 基于功能磁共振的序列分析(神经活动重现)。
文章链接:https://doi.org/10.1038/s41583-022-00570-z
崔再续 研究员

l 北京脑科学与类脑研究中心研究员
代表性成果:个体化脑功能网络形态与精神疾病的关联
2022年5月18日,崔再续研究员和美国宾夕法尼亚大学Ted Satterthwaite教授合作在Biological Psychiatry在线发表题为“Linking individual differences in personalized functional network topography to psychopathology in youth”的研究论文。
大脑皮层由多个功能上分化的分布式大尺度脑网络组成,脑功能网络在皮层上的位置在个体之间存在差异,但尚不清楚个体化的脑功能网络皮层形态与精神疾病的关系。
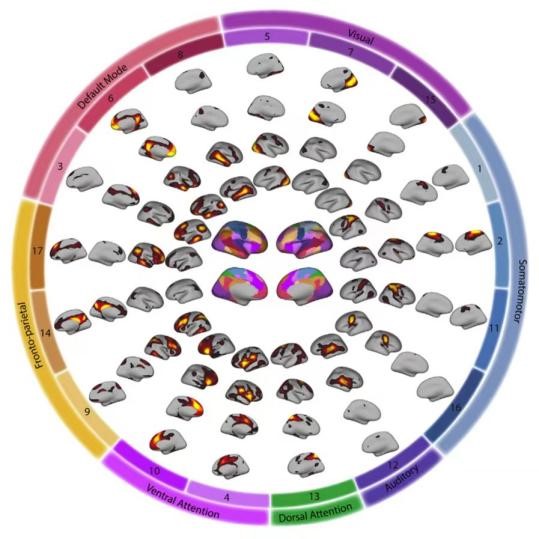
本研究采用公开数据库Philadelphia Neurodevelopmental Cohort采集的8-23岁的790名儿童青少年的27分钟功能磁共振成像数据。该数据构建了一个从正常到患有各类不同精神疾病的儿童青少年的连续谱系。我们采用非负矩阵因子分解将每个个体的大脑皮层划分为17个大尺度功能网络,并采用因子分析及临床症状数据(112项)提取总体精神病理学因子(也称为’p-factor’),该变量越高表明个体越倾向于患各类精神疾病。我们发现功能网络皮层形态信息(即某个体素属于哪一个功能网络)可显著预测个体的总体精神病理学因子得分。包括额顶控制网络与腹侧注意网络在内的高级网络对预测的贡献权重为负值,表明高级功能网络在皮层的总面积与总体精神病理学因子呈现负相关。
文章链接:
https://www.biologicalpsychiatryjournal.com/article/S0006-3223(22)01251-3/fulltext
熊巍 研究员

l 北京脑科学与类脑研究中心研究员
代表性成果:通过在体基因编辑治疗遗传性耳聋
2022年7月12日,熊巍实验室在Cell Reports杂志上发表长文:Template-independent genome editing in the Pcdh15av-3j mouse, a model of human DFNB23 nonsyndromic deafness(不依赖于修复模板的基因编辑应用于Pcdh15av-3j小鼠品系,一个人类非综合性耳聋DFNB23的动物模型)。本工作首次在哺乳动物模型上展示了利用非同源末端连接(NHEJ)的基因修复通路有效实现先天性遗传疾病的在体基因治疗。
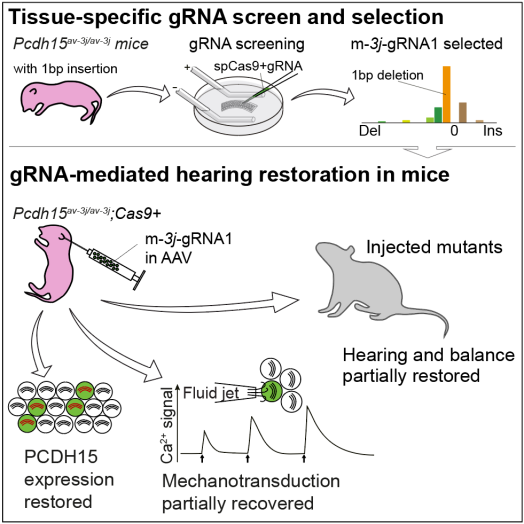
基因治疗是治疗基因突变相关遗传性疾病的金钥匙,目前该领域大部分工作集中在针对mRNA的基因替代(Gene replacement)或者基因沉默(Gene silence)方面,若干适用性好的靶基因已经被用于临床,表明基因治疗具有可行性。然而就中心法则而言,在mRNA水平的修复还是治标不治本,因此针对DNA的基因修复代表了下一代基因治疗的新方向。本研究提出特别针对DNA移码突变的一个方案,并系统展示了在耳蜗毛细胞DNA水平的基因编辑有效恢复动物听觉的过程。
本研究利用小鼠耳蜗培养组织验证了终端分化的功能细胞上编辑产物也具有可重复性,并利用该原理实现了单个gRNA即可修复移码突变,实现小鼠的在体基因治疗。本研究展示了接收声音振动的听觉毛细胞可以利用内源性DNA修复通路中的最主要方式NHEJ(大于90%)修复InDel导致的移码突变,在遗传性耳聋动物模型(Pcdh15av-3j小鼠,携带一个腺苷的插入突变)上实现了导入单个gRNA有效修复该插入导致的遗传性耳聋,而PCDH15蛋白是毛细胞tip link的组分,是毛细胞机械转导通道开放的关键蛋白,蛋白质量有215kD之巨。该概念的成功验证,提示占人类单基因遗传病中22%的移码突变导致的遗传性疾病有广阔的治疗前景。
文章链接:https://doi.org/10.1016/j.celrep.2022.111061
Carlos Ibanez 特聘研究员

l 北京脑科学与类脑研究中心特聘研究员
l 瑞典卡罗林斯卡学院神经科学系教授
l 北京大学生命科学学院教授
代表性成果:聚敛多巴胺与ALK4的PCBP1信号通路控制FosB选择性剪接与可卡因行为敏化
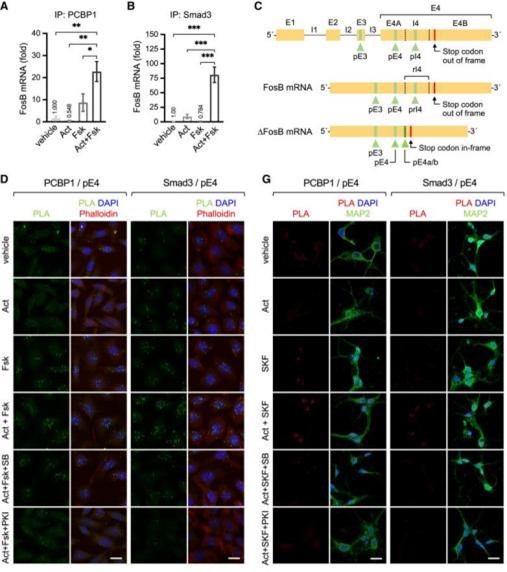
2022年7月22日,Carlos Ibanez教授等人在The EMBO JOURNAL发表题为“Convergent dopamine and ALK4 signaling to PCBP1 controls FosB alternative splicing and cocaine behavioral sensitization”的研究论文。
研究发现多巴胺D1受体信号通路与激活素/ALK4/Smad3通路协同起效,通过激活RNA结合蛋白PCBP1 (mRNA剪接调节因子),增强伏隔核(NAc)棘突神经元(MSNs)ΔFosB mRNA的生成。D1和ALK4信号通路同时激活PCBP1和Smad3可诱导它们相互作用、核易位,并与FosB mRNA的外显子-4和内含子-4序列结合。在重复刺激D1和ALK4受体后,消融MSNs中的ALK4或PCBP1会损害ΔFosB mRNA对ΔFosB蛋白的诱导与核易位作用。伏隔核MANs中ALK4是成年小鼠对可卡因行为敏化所必需的。
这些发现揭示了一种意料之外的机制,即ΔFosB的产生与药物诱导敏化通过聚敛多巴胺和ALK4信号通路形成。
文章链接:https://www.embopress.org/doi/full/10.15252/embj.2022110721
罗敏敏 特聘研究员

l 北京脑科学与类脑研究中心主任、特聘研究员
l 北京生命科学研究所资深研究员
l 清华大学教授
代表性成果:开发出一系列能够在体内和体外高效侵染小胶质细胞的新型rAAV载体
2022年7月25日,罗敏敏实验室在Nature Methods在线发表题为“Directed evolution of adeno-associated virus for efficient gene delivery to microglia”的研究论文。该研究通过定向进化策略,开发了一系列能够在体内和体外高效侵染小胶质细胞的新型rAAV载体,实现对小胶质细胞的标记、在体观测和基因编辑。
研究人员针对野生血清型AAV9的衣壳蛋白进行改造。AAV由衣壳蛋白和单链DNA基因组所构成,其侵染特性由衣壳蛋白所决定。研究人员成功得到了高效侵染体外培养小胶质细胞的AAV-cMG衣壳蛋白,并确认AAV-cMG侵染体外培养小胶质细胞并不导致小胶质细胞的激活。然而,体外筛选得到的这些AAV突变衣壳蛋白并不足以在小鼠脑内介导高效的小胶质细胞基因递送。研究人员进一步进行针对性体内筛选,成功鉴定得到两个衣壳蛋白,AAV-MG1.1和AAV-MG1.2,能够在体内高效侵染小胶质细胞。并确认AAV-MG1.1和AAV-MG1.2介导的侵染并不导致脑内小胶质细胞的激活。
这些新型rAAV病毒载体能够将众多基因编码的工具蛋白直接递送入小胶质细胞,无需针对每一个工具蛋白重新构建新的转基因小鼠品系,大大提高了研究效率。更重要的是,这些新型rAAV病毒载体使得对小胶质细胞进行快速基因编辑成为可能。
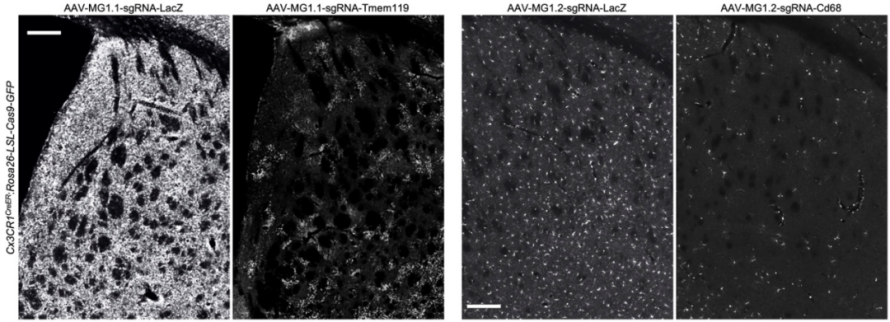
图:AAV-MGs介导小胶质细胞在体基因敲除
该研究成功开发了两类分别适用于体外侵染培养小胶质细胞和体内侵染内源性小胶质细胞的新型rAAV载体,拓展了各种研究手段被用于小胶质细胞研究的可行性,并有希望应用于小胶质细胞基因疗法的开发。
文章链接:https://doi.org/10.1038/s41592-022-01547-7
马继延 资深研究员

l 北京脑科学与类脑研究中心资深研究员
代表性成果:由错误折叠蛋白质所导致的致死性神经退行性疾病
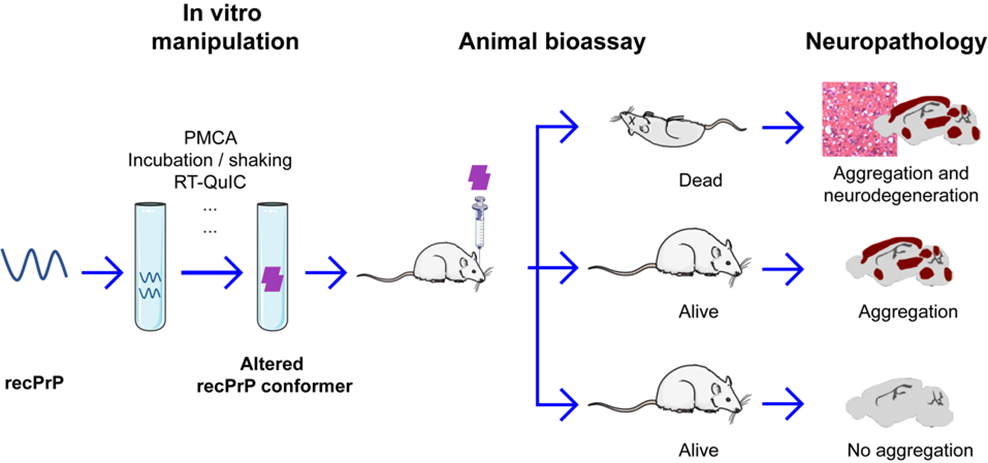
2022年8月31日,马继延教授团队在Viruses发表了题为“Recombinant Mammalian Prions: The “Correctly” Misfolded Prion Protein Conformers” 的综述,总结了多年来运用重组朊蛋白在体外折叠成朊病毒的研究,并展望了未来的发展。
40多年前,Stanley Prusiner提出了著名的“朊病毒假说”,认为在朊病毒疾病中传递致病遗传信息的物质是错误折叠的蛋白质——朊病毒。他提出朊病毒具有独特的“种籽效应”,能诱导体内正常朊蛋白错误折叠,形成更多的朊病毒,导致致死性的神经退行性病变。因为这一假说背离了现代生物学的中心法则,即遗传信息是由核酸所传递,该假说在学界受到广泛的质疑,尽管Prusiner于1997年获得诺贝尓奖,相关质疑也未能完全平息。
朊病毒假说最好的证明方法是用大肠杆菌表达的重组朊蛋白,在试管中折叠成朊病毒的错误构象,并在动物体内证明体外形成的重组朊病毒具有全部的致病特性。几十年来,全世界许多科学家对这一难题进行了各种探索,在体外构建了许多朊蛋白聚集体。马继延团队梳理了这一领域的所有工作,提出“种籽效应”与致病性存在差异——体外错构朊蛋白聚集体均具有“种籽效应”,然而仅有少数朊蛋白错构体具有与朊病毒疾病相同的致病性,由此提出“正确的”朊蛋白错误折叠的概念。
目前在老年痴呆症等神经退行性疾病中,错误折叠的蛋白聚集体也发现有类似朊病毒的“种籽效应”。根据朊病毒研究中发现的“种籽效应”与致病性的差异,提示了对这类错构蛋白的致病性需要进一步的研究。同时,对“正确”错误折叠朊蛋白的结构研究也将从分子层面揭示朊病毒的致病机理,为最终防治这类神经退行性疾病打下基础。
文章链接:https://www.mdpi.com/1999-4915/14/9/1940
孙文智 研究员

l 北京脑科学与类脑研究中心研究员
l 首都医科大学基础医学院研究员
代表性成果:建立特异类型单神经元全脑功能投射研究方法
2022年10月13日,孙文智研究员团队与华中科技大学周伟副教授等研究团队合作,在Advanced Science在线发表论文“Mapping the function of whole-brain projection at the single neuron level”,建立了能对特定类型神经元进行单细胞分辨的神经活动成像,并绘制出同一个神经元在全脑范围精细轴突投射的方法。该方法结合遗传型功能探针稀疏标记、活体双光子荧光成像、高清fMOST全脑精细结构成像和跨模态细胞匹配等多项技术,能获取同一神经元的神经活动与全脑投射信息,并在单神经元水平探索了功能偏好与轴突投射特性的关系。
研究采用rAAV体系的二元表达系统,用遗传型钙探针GCaMP6稀疏标记神经元,通过活体钙成像方法,记录清醒小鼠神经元的视觉功能响应;利用高清荧光显微光学切片断层成像技术(High-definition fluorescent micro-optical sectioning tomography, HD-fMOST),获取GCaMP6标记神经元的全脑解剖形态和位置信息;通过项目组开发的方法实现跨模态细胞匹配,整合活体钙成像与高分辨率的全脑结构成像的信息,得到单神经元水平全脑投射的功能注释(functional annotation of whole-brain projection at the single neuron level, FAWPS),由此建立了获取同一神经元的功能响应特征和轴突全脑投射信息的方法。
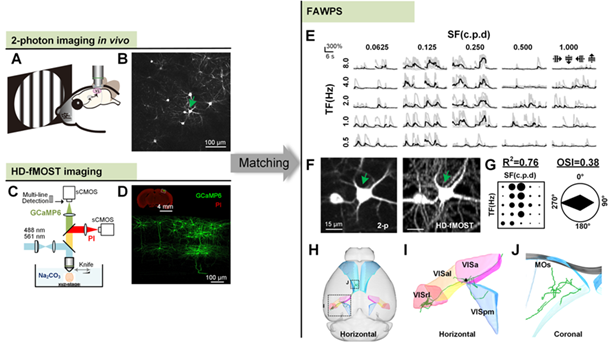
图.FAWPS的获取流程示意
该研究中遗传型功能探针是连接同一个神经元的功能与全脑投射成像的桥梁。具体解决了遗传功能探针的稀疏标记、荧光增强和信噪比提升等技术难题。精细结构成像结果证实了GCaMP6的轴突标记与膜定位蛋白类似,且轴突信号的信背比与已发表的GFP信号相当,从而确保了单神经元轴突完整重建的可靠性。这些研究共同证实了遗传功能探针不仅能用于功能记录,也能用作全脑精细结构表征。
文章链接:https://doi.org/10.1002/advs.202202553
杨玉超 双聘研究员

l 北京脑科学与类脑研究中心双聘研究员
l 北京大学长聘教授/博雅特聘教授
l 北京大学信息工程学院副院长
l 北京大学人工智能研究院类脑智能芯片中心主任
代表性成果:基于忆阻器的多模态多尺度储备池计算
2022年10月13日,杨玉超双聘研究员团队在仿生光电突触与多模态多尺度储备池计算研究中取得重要进展,相关成果以“An optoelectronic synapse based on α-In2Se3 with controllable temporal dynamics for multimode and multiscale reservoir computing”为题,发表在Nature Electronics上。
物理系统的动态演化过程可以作为一种高效的计算资源应用于信息处理,储备池计算是其中备受关注的一种计算范式,具有易于训练、硬件开销低等优点,且可以使用各种电学和光学硬件实现,在语音数字识别、混沌系统预测、二阶非线性任务和实时神经活动分析等方面取得了显著进展。然而,当前储备池仍然面临非线性映射模式固定、无法处理多模态信号、缺乏多尺度特征提取能力等问题,因而限制了储备池的信息处理能力,难以实现多模态多尺度的储备池计算系统。
针对以上关键问题,杨玉超教授课题组构建了基于α-In2Se3的多功能光电忆阻器件,利用其光电耦合的动力学特性,实现了多模态融合、多时间尺度的储备池计算。团队构建了多模态融合的储备池计算系统,成功实现了多模态的手写数字识别和二维码识别任务。此外,背栅电压/光照作为第三端可以进一步实现异源突触可塑性,解决了已有忆阻器弛豫时间相对固定的问题,并进一步实现了多尺度的储备池计算。该项研究利用α-In2Se3忆阻器中的多种物理机制,实现了跨模态的突触可塑性和弛豫时间的可调性,提供了多种非线性映射的模式、多模态融合的创新方案、多尺度特征提取的能力,为储备池计算应用于更复杂的任务和更广阔的场景奠定了坚实的基础。
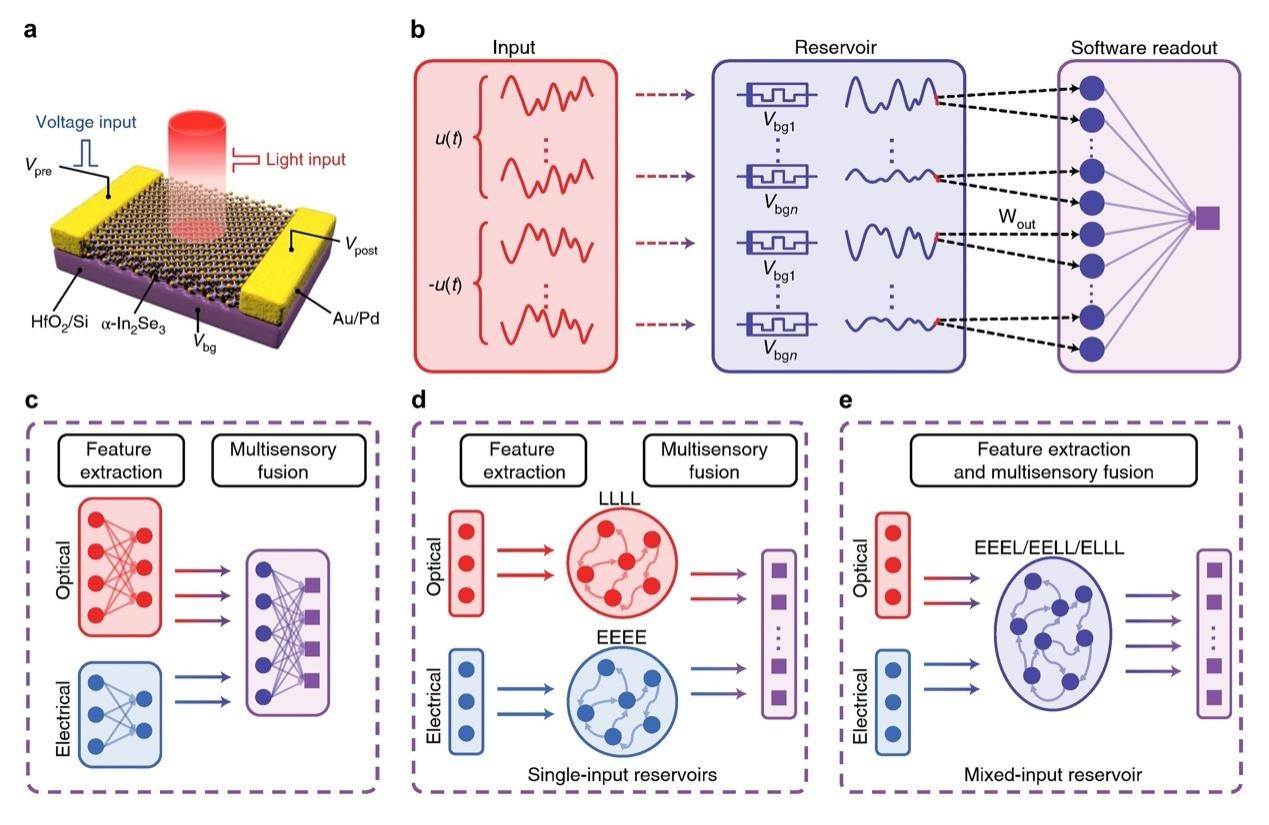
图:光电忆阻器与多模态多尺度储备池计算
文章链接:https://www.nature.com/articles/s41928-022-00847-2
饶毅 特聘研究员

l 北京脑科学与类脑研究中心主任、特聘研究员
l 北京大学终身讲席教授
l 首都医科大学校长
睡眠的分子机理:饶毅实验室发现蛋白激酶LKB1调控果蝇和小鼠的睡眠
睡眠的分子和细胞机理,迄今尚不清楚而有较多研究。从2017年起,饶毅实验室发表了5篇论文,涉及睡眠的分子机理。2022年,他们发表第6篇睡眠分子机理的文章。
睡眠的重要性不言而喻,但睡眠的两大问题:睡眠机理和为什么要睡眠,都不清楚。对于睡眠机理的研究,早期注重参与睡眠的脑区,后来到现在都有很多电生理研究睡眠的细胞机理。而对于睡眠的分子机理,早期依赖对神经递质的研究,二十年前开始有用果蝇遗传学研究睡眠的分子机理。果蝇的遗传学和分子生物学有助于揭示睡眠的分子机理,但果蝇的睡眠与哺乳类的睡眠是否保守、在机理上是否保守,有些证据支持,有些反对。因为在果蝇发现的分子比较多,而显然有些分子在果蝇调控睡眠,但在哺乳动物并不调控睡眠。
饶毅实验室的研究生钱永军等于2017年发表的文章显示,果蝇的神经递质五羟色胺(5HT)的受体2b,在少到两个神经元中起调控睡眠的作用,特别是睡眠剥夺后的恢复。在小鼠,五羟色胺是否参与睡眠调控,很长时间有争议。饶毅实验室的博士后张娴等于2018年发表的文章显示,五羟色胺确实参与小鼠睡眠调控,但影响的程度不如在果蝇中那么大。2019年饶毅实验室博士后邓博文等的化学连接组工作,也显示了更多参与果蝇睡眠调控的神经递质及其受体。2019年,饶毅实验室的研究生戴熙慧敏和周恩兴等发现,长期被人们认为在生物体内不存在的D型丝氨酸,不仅在果蝇存在,而且调控睡眠。戴熙慧敏和周恩兴等发现,D型丝氨酸可以在肠道上皮细胞(不是肠道内部细菌)合成,从而作用于神经细胞的NMDA受体再调控睡眠。这一作用在果蝇很显著,但迄今没有看到D型丝氨酸是否在哺乳动物调控睡眠的证据,也没有在哺乳动物的肠道上皮细胞发现D型丝氨酸。2021年,戴熙慧敏和周恩兴等发现,果蝇的神经递质乙酰胆碱(ACh)通过作用于果蝇有些细胞的一种ACh受体亚型起促进睡眠的作用,通过另外一些细胞上另外一种ACh受体而抑制睡眠。这些研究也没有哺乳类的工作。
饶毅实验室2022年的睡眠研究,在果蝇和小鼠研究了同一个分子对睡眠的作用,发现这个分子在果蝇和小鼠都调控睡眠。
这篇文章的作者为:研究生刘子怡、博士后姜丽芬和李超逸、技术员李成钢和杨靖群,以及研究生余建军和毛仁波,通讯作者饶毅。文章刊于美国遗传学会主办的、摩尔根创办的Genetics(遗传学)。
刘子怡等研究的分子是LKB1,即“肝激酶B1”。它是蛋白激酶,但它并非肝脏特异的,而在很多器官有表达,包括脑。
LKB1的重要性,在1997年被发现。1921年和1949年,两位科学家发现一种提高多种组织癌症危险的胃肠道息肉的疾病,被称为Peutz-Jeghers 综合症(PJS)。1997年和1998年,LKB1基因突变被发现是PJS的致病原因,因此LKB1是抑癌基因。其缺失导致胃肠道肿瘤、肺腺瘤、子宫颈癌、卵巢癌、乳腺癌、胰腺癌和黑色素瘤。
LKB1基因编码的蛋白质是一种蛋白激酶。那么它磷酸化的底物是什么呢?2003年,英国和美国科学家们发现LKB1可以磷酸化AMPKα的T172位点。AMPK是代谢调控的重要蛋白激酶。一般认为AMPK有十几种相关蛋白质,被称为AMPK相关激酶(ARKs)。2004年,英国和芬兰科学家认为LKB1可以磷酸化当时认为的全部(14个)ARKs。
2016年,日本科学家通过遗传筛选,发现小鼠的SIK3影响睡眠。他们发现,如果SIK3因为突变而功能增强,小鼠的睡眠增加。也就是说,SIK3促进睡眠。他们发现果蝇的SIK3也有类似作用。他们后来还发现,如果小鼠的SIK1和SIK2有类似SIK3的功能增加的突变,也可以导致小鼠睡眠增加。
饶毅实验室的研究生李扬、博士后刘玉祥等发现,剔除SIK3基因的小鼠,睡眠减少。剔除SIK1和SIK2基因则不影响小鼠睡眠。也就是说只有内源的SIK3参与睡眠调控,而SIK1和SIK2在生理情况下不调控小鼠睡眠(李扬等,审稿中)。
饶毅实验室的博士后刘玉祥和研究生王涛、技术员崔云凤等发现,虽然从HEK培养细胞中免疫沉淀的LKB1可以磷酸化SIK3,但是细菌表达的重组LKB1能够磷酸化AMPK而不能磷酸化SIK3。他们因此研究并发现了更多的磷酸化ARK的蛋白激酶(刘玉祥等,2022a,2022b)。
刘子怡等分析了小鼠和果蝇的基因突变造成的LKB1功能降低。LKB1的基因不能完全缺失。如果完全缺失后,果蝇和小鼠都在胚胎期就死亡,无法分析成年动物中LKB1对睡眠的作用。刘子怡等成功地获得了LKB1功能大大降低的突变株。
她们发现,随着LKB1基因突变带来其mRNA表达减少,睡眠减少,无论在果蝇、还是在小鼠。这些结果表明LKB1从果蝇到小鼠都具有保守的、调控睡眠的作用。对果蝇睡眠的影响特别在夜晚,睡眠总时间减少,关灯后到睡眠的潜伏期延长,每段睡眠时间减少。这些作用有剂量依赖效应,杂合体果蝇的睡眠也有部分减少。而这种量效关系与mRNA表达水平呈相关性。转基因引入野生型LKB1可以挽救突变株的睡眠减少表型。
如果只在果蝇的神经细胞剔除LKB1基因,也出现类似的睡眠表型。但是单纯在野生型果蝇的神经细胞过表达LKB1,观察不到睡眠表型的变化。
果蝇AMPK的T184相当于哺乳动物的T172位点。这个位点如果是野生型的T、或突变的E,对野生型果蝇的睡眠表型没有影响,但如果在LKB1已经下降的情况下,再引入AMPK T184A,果蝇的睡眠进一步下降。这种位点特异的遗传相互作用,提示--但不证明--LKB1和AMPK可以有睡眠方面的功能关系。SIK3同类突变与LKB1没有显示睡眠方面的遗传相互作用。SIK3同类突变与LKB1在致死方面显示遗传相互作用。
虽然以前有研究显示转录因子DEC1可以调节昼夜节律,而且可以降低LKB1的基因转录,从而降低AMPK活性,刘子怡等没有观察到LKB1参与果蝇的昼夜节律生物钟。
刘子怡等用条件性敲除LKB1基因的小鼠,通过成年注射病毒而导致小鼠脑内神经元缺失LKB1基因。发现小鼠白天(小鼠正常睡眠时段)的睡眠减少,特别是非快动眼睡眠(NREM)减少。而几种对照组不出现这一表型。快动眼睡眠(REM)也不受影响。指征睡眠需求的NREM之δ功率密度,在神经细胞减少LKB1之后,也显著降低,说明LKB1对于睡眠需求是必需的。
刘子怡等的研究表明,LKB1对于果蝇和小鼠都是必需的,而且在两种动物都是在神经细胞内调控睡眠。因为有脑电图帮助分析,在小鼠还可以发现LKB1促进睡眠需求。
LKB1下游到底是什么,AMPK是一种可能,但证据比较间接(遗传相互作用)。LKB1在什么细胞起调控睡眠的作用?哪些神经细胞?神经细胞之外是否还有其他细胞?神经系统之外是否就完全与睡眠无关?
AMPK对代谢很重要。LKB1调控睡眠是否与调控代谢有关?什么关系?平行还是上下游?都是有待进一步探究的有趣和重要的问题。
文章列表:
- Qian YJ, Cao Y, Deng BW, Yang G, Li J, Xu R, Zhang D, Huang J and Rao Y (2017). Sleep homeostasis regulated by 5HT2b receptor in a small subset of neurons in the dorsal fan-shaped body of Drosophila. eLife 6:e26519.
- Zhang X, Yan HM, Huang ZL and Rao Y (2018). Independence of 5HT involvement in sleep and arousal from thermoregulation in mice. Mol Pharmacol 93:657-664.
-Deng BW, Li Q, Liu XX, Cao Y, Li BF, Qian YJ, Xu R, Mao RB, Zhou EX, Zhang WX, Huang J and Rao Y (2019) Chemoconnectomics: mapping chemical transmission in Drosophila. Neuron 101:876-893.
-Dai XHM, Zhou EX, Yang W, WX Zhang and Rao Y (2019). D-Serine promotes sleep through the NMDA receptor in Drosophila melanogaster. Nature Communications 10:1986.
-Dai XHM, Zhou EX, Yang W, Deng BW, Li Q, Liu XX, Zhang WX and Rao Y (2021). Molecular resolution of a behavioral paradox: sleep and arousal are regulated by distinct acetylcholine receptors in different neurons of Drosophila. Sleep 10, 1093.
- Liu ZY, Jiang LF, Li CY, Li CG, Yang JQ, Yu JJ, Mao RB and Rao Y (2022). LKB1 is physiologically required for sleep from Drosophila melanogaster to the Mus musculus. Genetics 221, iyac082.



