Allergy | 井淼/赵嘉惠团队揭示“PAR2-TRPV3-IL33”信号轴在特应性皮炎表皮-肥大细胞-外周神经互作中的关键作用
特应性皮炎(Atopic Dermatitis,AD)是一种慢性、复发性、瘙痒性皮肤疾病。其复杂的发病机制,尤其是皮肤离子通道调控神经-免疫通讯的具体路径,一直是医学研究的热点及难点。
2026年3月8日,北京脑科学与类脑研究所井淼团队联合北京大学第一医院皮肤科赵嘉惠团队于Allergy(IF=12.0)在线发表题为“Epidermal PAR2-TRPV3-IL-33 Signaling Promotes Mast Cell Recruitment and Sensory Nerve-Mast Cell Interactions in Atopic Dermatitis”的论文,首次揭示了瞬时受体电位通道TRPV3偶联G蛋白受体PAR2调控皮肤神经免疫反应的具体机制。
研究团队首先发现,AD病变皮肤中肥大细胞数量与活性显著升高,而在TRPV3基因敲除小鼠中,这一异常现象明显缓解。进一步通过组织免疫荧光染色和血管通透性检测表明,TRPV3缺失可显著减少血管周围肥大细胞聚集,降低皮肤水肿并减轻炎症反应。为明确TRPV3作用的细胞来源,研究人员构建了角质形成细胞特异性TRPV3敲除小鼠,其炎症表型与全身敲除小鼠高度一致,提示角质形成细胞上的TRPV3是驱动AD中肥大细胞招募的重要离子通道。
机制研究中,研究团队进一步发现PAR2作为TRPV3的重要上游信号,可促进白细胞介素33(IL-33)的表达。实验表明,PAR2激活显著增强角质形成细胞IL-33的产生。同时 Transwell实验表明,IL-33能够剂量依赖性诱导骨髓来源肥大细胞迁移,而阻断其受体ST2信号时,该迁移效应显著减弱,明确了表皮PAR2-TRPV3-IL-33轴是介导肥大细胞募集的关键信号轴(图1)。
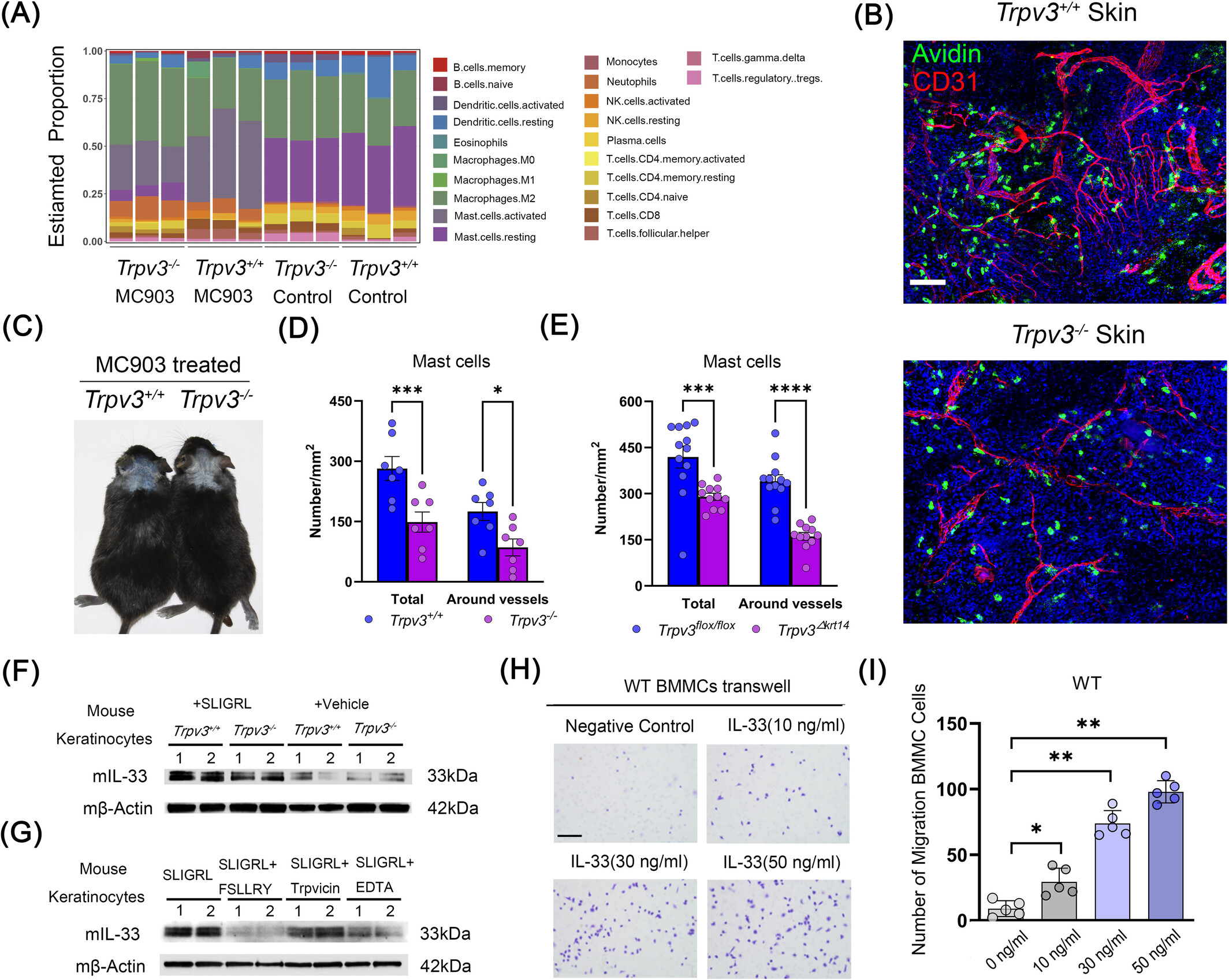
图1 TRPV3 缺陷减少皮肤中肥大细胞的募集并抑制 IL-33 依赖性炎症反应。
值得关注的是,该研究还揭示了TRPV3驱动的IL-33对感觉神经元的调控作用。研究发现,TRPV3基因敲除小鼠中,AD相关神经肽P物质(Substance P, SP)的表达显著降低;免疫染色显示,背根神经节中小直径神经元共表达SP和IL-33受体ST2,表明IL-33可直接作用于感觉神经元调控神经肽分泌。进一步功能实验证实,口服NK1受体拮抗剂(SP受体拮抗剂)可有效减轻皮肤水肿,提示SP-NK1R信号参与介导肥大细胞依赖的血管通透性调节,这也与此前荨麻疹研究中发现的肥大细胞、皮肤神经与血管内皮的密切交互机制相呼应,揭示了过敏性皮肤病共通的致病回路(图2)。
研究负责人表示,此次发现的表皮PAR2-TRPV3-IL-33轴,是调控AD皮肤屏障-免疫-神经交互的核心枢纽,该通路通过PAR2整合环境及蛋白水解信号,借助IL-33介导的肥大细胞招募放大炎症,同时通过神经肽驱动神经源性炎症,形成完整的致病循环。这一机制的阐明,打破了以往对AD神经-免疫调控的认知局限。
此外,研究团队还提供了临床转化相关证据,发现AD患者血清中IL-33显著高于荨麻疹患者、健康对照组,且皮损的神经周围存在肥大细胞聚集,进一步验证了该信号轴在人类疾病中的高度相关性(图2)。
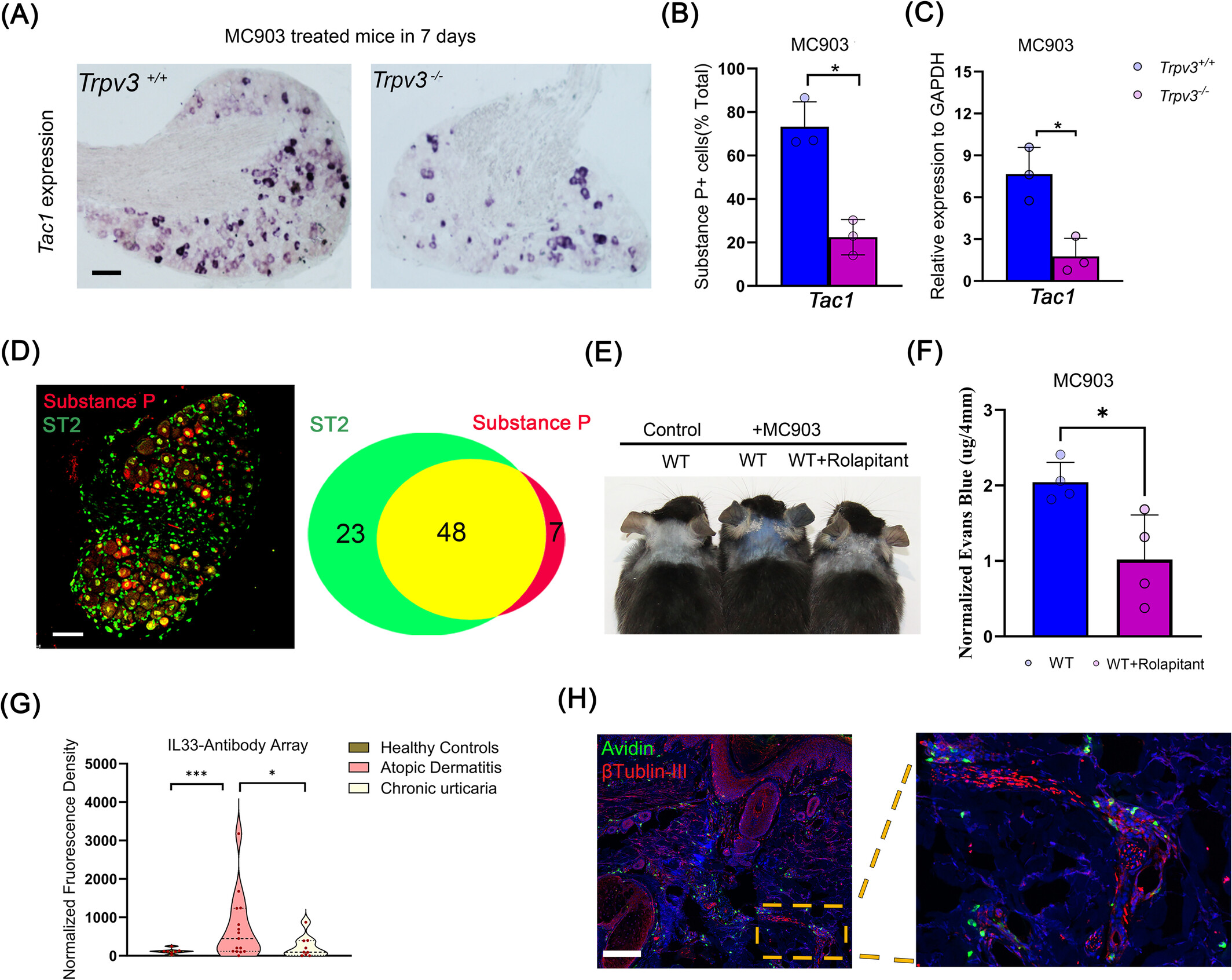
图2 TRPV3-IL-33轴调节P物质和神经-肥大细胞相互作用。
该研究不仅深化了对AD发病机制的理解,更为治疗提供了多个潜在靶点—针对PAR2、TRPV3、IL-33或NK1R等轴上关键分子的联合干预方案,有望实现对AD炎症和瘙痒的精准抑制,为开发新型治疗药物提供了重要靶点支撑。
论文信息
赵嘉惠副研究员为本文的第一及通讯作者,北京大学第一医院硕士研究生周灵萱及北京脑科学与类脑研究所博士研究生王晨雨为共同第一作者,井淼研究员为本文的共同通讯作者。该研究工作受到国家自然科学基金 (#82373468和32371150),北京脑科学与类脑研究所科研开发合作基金(#2020-NKX-XM-08)等项目的资助。研究过程得到了美国纽约西奈山医院胡宏镇教授、首都医科大学基础医学院免疫系孙英教授及北京大学医学部基础医学院赵东宇教授的指导。本研究感谢中国医学科学院杨勇教授提供TRPV3特异性抑制剂,北京生命科学研究所陈婷教授提供实验动物支持。



