
马继延
美国伊利诺伊大学芝加哥分校,生物化学与分子生物学博士
上海医科大学(现复旦大学上海医学院),医学硕士
上海医科大学(现复旦大学上海医学院),医学学士
现任北京脑科学与类脑研究所资深研究员
曾任美国范安德研究所教授;美国俄亥俄州立大学长聘(tenured)副教授;美国俄亥俄州立大学助理教授;美国芝加哥大学/霍华德休斯医学研究所博士后研究员
我们研究的最终目标是阐明错误折叠蛋白在神经退行性疾病中的致病机理,并研发出针对这类疾病有效的诊疗措施。Alzheimer病和帕金森病等神经退行性疾病多在老年群体中发生,我们至今还没有有效的手段来防止、治疗或减缓这类疾病。日益老龄化的社会迫切需要我们对这类疾病进行深入的研究,从而开发出有效的预防、诊断和治疗手段。
虽然各种迟发性神经退行性疾病的临床表现有很大不同,但它们都具有一个共同点:在发病的中枢神经系统中都有错误折叠蛋白的聚集。尽管我们知道这些蛋白聚集体的产生与疾病的发生发展相关,但许多重要的、也是非常基本的问题依然还没有得到回答。如这些错误折叠蛋白聚集体是如何形成的?它们又是如何引起神经退行性病变的?消除这些蛋白聚集体能否减缓疾病的发展或老年性的记忆衰退?我们希望回答这些问题,从而找到治疗这类疾病的方法。我们目前的研究主要集中在两种蛋白:α-突触核蛋白和朊蛋白。
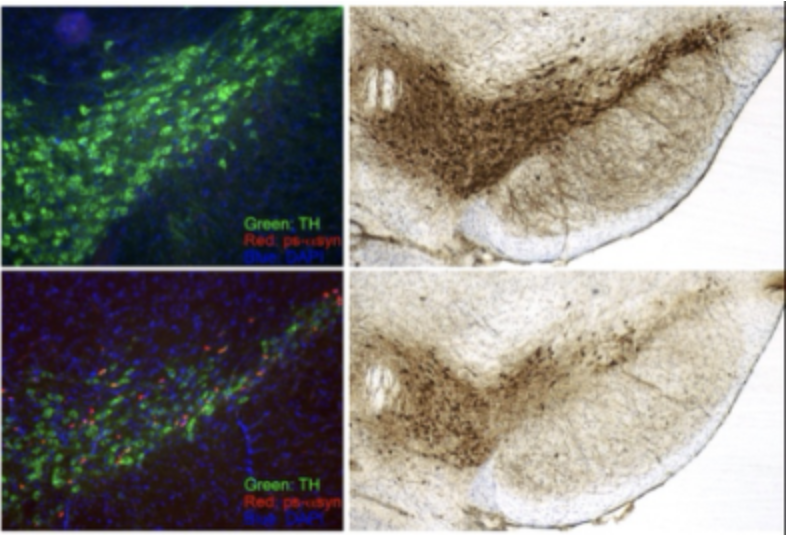
α-突触核蛋白 (α-syn)的错误折叠与聚集,会导致α-突触核蛋白病这一类神经退行性疾病。这类疾病包括帕金森病 (PD)、路易氏体失智症 (DLB) 和多系统萎缩 (MSA)等。以往的研究证明了错误折叠的α-syn和神经退行性变之间的相关性,然而我们还不知道为什么α-syn会错误折叠以及错误折叠的α-syn如何导致神经毒性。我们将综合应用多种现代生物学方法来研究α-syn在神经退行性疾病中的作用。利用α-syn淀粉样纤维种籽效应的实验模型,我们目前的研究聚焦于错误折叠α-syn直接导致的分子与细胞生物学变化。此外,我们也在研究α-syn种籽效应的体外检测方法,以期确定α-syn聚集体的种籽活性能否发展成为可靠且方便使用的生物标志物。
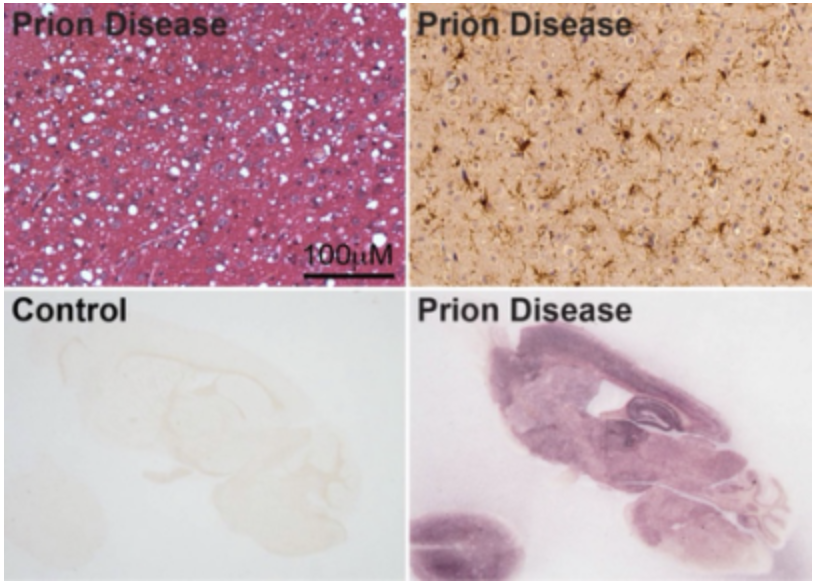
朊蛋白 (PrP) 是一种宿主编码的、锚定于细胞膜上的糖蛋白。错误折叠的PrP存在于一类称为传染性海绵状脑病 (TSE) 或朊病毒病的神经退行性疾病中,其中包括人的克雅氏病、羊的搔痒病以及鹿和麋鹿的慢性消耗性疾病。这类神经退行性疾病的独特之处在于它们也是传染病。几十年来,学界有关错误折叠的PrP是否是TSE中的传染因子(朊病毒假说)存在着激烈的争论。我们的研究为证明这一假说提供了无可辩驳的证据。我们目前研究的一个关注点是确定PrP聚集体的哪些特征对朊病毒的传染性至关重要,并尝试寻找检测和抑制错误折叠PrP的新策略。朊病毒病是啮齿动物中的神经退行性疾病,它的病理变化过程真实地反映了神经退行性疾病的发病过程,所以这类疾病的研究也将为揭示其他神经退行性疾病的致病机制提供启示。另外,我们也对正常PrP的功能以及PrP在其他疾病中的作用十分感兴趣,希望揭示PrP的正常功能并通过调节PrP来辅助其他疾病的预防和治疗。
伊利诺伊大学芝加哥分校研究生院奖学金
瑞士蛋白转输、糖基化与健康国际大会青年科学家奖
艾立森医学基金会青年学者奖
俄亥俄州立大学医学院优秀教学奖
亚太朊病毒协会(APSPR)理事;曾任美国NIH评审小组和研究项目计划的常任以及即席评审专家,并任英国医学研究委员会(MRC)和生物技术和生物科学研究委员会(BBSRC)、英国帕金森研究基金、加拿大艾伯塔省朊病毒研究所、艾伯塔Alzheimer病(老年性痴呆)研究计划、德以科学研究基金会、以色列科学基金会、意大利卫生部、Alzheimer病基金会、美国衰老研究联合会等国际研究机构的评审专家。
Selected Publications
Prion
1. Ma Y and Ma J. (2020) Immunotherapy against prion disease. Pathogens. 9(3):216
2. Wang F, Wang X, Orrú C.D., Groveman B. R., Surewicz K., Abskharon R., Imamura M., Yokoyama T., Kim Y.S., Vander Stel K.J., Sinniah K., Priola S.A., Surewicz W.K., Caughey B., Ma J. (2017) Self-propagating, protease-resistant, recombinant prion protein conformers with or without in vivo pathogenicity. PLOS Pathog 13(7): e1006491.
3. Wang X, McGovern G, Zhang Y, Wang F, Zha L, Jeffrey M, Ma J. (2015) Intraperitoneal infection of wild-type mice with synthetically generated mammalian prion PLOS Pathog 11(7):e1004958.
4. Ma J. (2012) The role of Cofactors in Prion Propagation and Infectivity PLOS Pathog 8(4): e1002589.
5. Wang, F.*, Wang, X.*, Yuan, C., Ma, J. (2010) Generating a Prion with Bacterially Expressed Recombinant Prion Protein Science 327:1132-1135. (* equal contribution)
6. Wang, F., Yang, F., Hu, Y., Wang, X., Wang, X., Jin, C., Ma, J. (2007) Lipid interaction converts prion protein to a PrPSc-like proteinase K resistant conformation under physiological conditions Biochemistry. 46(23):7045-7053.
7. Ma, J., Wollmann, R., Lindquist, S. (2002) Neurotoxicity and neurodegeneration when PrP accumulates in the cytosol Science 298(5599):1781-5
8. Ma, J. and Lindquist, S. (2002) Conversion of PrP to a self-perpetuating PrPSc-like conformation in the cytosol Science 298(5599):1785-8
9. Ma, J. and Lindquist, S. (2001) Wild-type and mutant PrP accumulate in the cytoplasm upon proteasome inhibition Proc. Natl. Acad. Sci. USA. 98:14955-14960.
10. Ma. J. and Lindquist, S. (1999) De novo generation of a PrPSc-like conformation in living cells Nat. Cell Biol. 1:358-361.
α-synuclein
1. Bargar C, Wang W, Gunzler SA, LeFevre A, Wang Z, Lerner AJ, Singh N, Tatsuoka C, Appleby B, Zhu X, Xu R, Haroutunian V, Zou W*, Ma J*, Chen SG*. (2021) Streamlined alpha-synuclein RT-QuIC assay for various biospecimens in Parkinson’s disease and dementia with Lewy Bodies. Acta Neuropathol Commun. 9(1):62. (*co-corresponding authors)
2. Wang Z, Becker K, Donadio V, Siedlak S, Yuan J, Rezaee M, Incensi A, Kuzkina A, Orrú CD, Tatsuoka C, Liguori R, Gunzler SA, Caughey B, Jimenez-Capdeville ME, Zhu X, Doppler K, Cui L, Chen SG*, Ma J*, Zou W*. (2020) Skin α-synuclein aggregation seeding activity as a novel biomarker for Parkinson’s disease. JAMA Neurol. 78(1):1-11. (*co-senior authors)
3. Roux A, Wang X, Becker K, Ma J. (2020) Modeling α-synucleinopathy in organotypic brain slice culture with preformed α-synuclein amyloid fibrils. J Parkinsons Dis. 10(4):1397-1410.
4. Marshall LL, Killinger BA, Ensink E, Li P, Li KX, Cui W, Lubben N, Weiland M, Wang X, Gordevicius J, Goetzee GA, Ma J, Jovinge S, Labrie V. (2020) Epigenomic analysis of Parkinson’s disease neurons identifies Tet2 loss as neuroprotective. Nat Neurosci. 23(10):1203-1214.
5. Wang X, Becker K, Levine N, Zhang M, Lieberman AP, Moore DJ, Ma J. (2019) Pathogenic alpha-synuclein aggregates preferentially bind to mitochondria and affect cellular respiration. Acta Neuropathol Commun. 7(1):41.
6. Chen X, Kordich JK, Williams ET, Levine N, Cole-Strauss A, Marshall L, Labrie V, Ma J, Lipton JW, Moore DJ. (2019) Parkinson’s disease-linked D620N VPS35 knockin mice manifest tau neuropathology and dopaminergic neurodegeneration. Proc Natl Acad Sci USA. 116(12):5765-5774.
7. Graham SF, Rey NL, Ugur Z, Yilmaz A, Sherman E, Maddens M, Bahado-Singh RO, Becker K, Schulz E, Meyerdirk LK, Steiner JA, Ma J, Brundin P. (2018) Metabolomic profiling of bile acids in an experimental model of prodromal Parkinson’s disease. Metabolites 8(4):71.
8. Wang B, Underwood R, Kamath A, Britain C, McFerrin MB, McLean PJ, Volpicelli-Daley LA, Whitaker RH, Placzek WJ, Becker K, Ma J, Yacoubian TA. (2018) 14-3-3 proteins reduce cell-to-cell transfer and propagation of pathogenic alpha-synuclein. J Neurosci. 38(38): 8211-8232.
9. Graham SF, Rey NL, Yilmaz A, Kumar P, Madaj Z, Maddens M, Bahado-Singh RO, Becker K, Schulz E, Meyerdirk LK, Steiner JA, Ma J, Brundin P. (2018) Biochemical profiling of the brain and blood metabolome in a mouse model of prodromal Parkinson’s disease reveal distinct metabolic profiles. J Proteome Res. 17(7): 2460-2469.
10. Becker K, Wang X, Vander Stel K, Chu Y, Kordower J, Ma J. (2018) Detecting alpha synuclein seeding activity in formaldehyde-fixed MSA patient tissue by PMCA. Mol Neurobiol. 55(11):8728-8737.



