突破多靶点高通量检测瓶颈!罗敏敏团队/林睿团队联合开发抗体模块化DNA标记策略(MaMBA),实现高通量多重检测 | eLife
引言
曾经备受瞩目的Theranos公司,凭借”一滴血检测上百种疾病”的宏大愿景在硅谷崛起,一度估值90亿美元。然而,随着其技术缺乏科学依据的事实逐渐暴露,这场所谓的“医疗革命”最终走向失败。Theranos事件不仅成为商业领域的重要警示,也揭示了生物医学领域一个核心需求——从有限且珍贵的临床样本中提取尽可能多的信息。近日,北京脑科学与类脑研究所罗敏敏实验室与北京生命科学研究所/清华大学交叉医学研究院林睿实验室联合发布的一项关于抗体模块化DNA标记策略(MaMBA)的研究,为满足这一需求提供了关键性技术支撑。
免疫化学分析(如免疫荧光染色、酶联免疫吸附技术ELISA等)是生物医学检测中最为常用的技术。该技术基于抗体和抗原间的特异性结合,通过检测抗体所偶联的信号分子,实现对样品中特定生物分子的定量和定位。由于信号分子(如荧光分子和化学发光底物)的种类有限,传统免疫化学分析方法难以在一个样品中同时检测多个目标分子。为了扩展检测的多重性并实现更高的检测通量,近年来研究人员将抗体与DNA分子连接,利用DNA序列的高度多样性和特异性,将不同的抗体用不同的DNA序列(即DNA条形码)区分开来以实现许多目标分子的同时检测,这种技术已经被广泛用于从诊断到治疗的众多应用中【1】。然而,当前的DNA条形码标记方法需要针对每一个抗体做定制化的制备流程,耗时且成本高,并且常用非位点特异性的偶联方式,降低了抗体的亲和力和特异性。
2025年7月22日,罗敏敏实验室与林睿实验室在eLife期刊在线发表了题为“Modular DNA barcoding of nanobodies enables multiplexed in situ protein imaging and high-throughput biomolecule detection”的研究论文。该研究提出了一种简单、经济且高效的模块化DNA条形码标记策略MaMBA(Multiplexed and Modular Barcoding of Antibodies)。

为了实现模块化的DNA条形码标记,研究者使用高亲和力的靶向IgG的纳米抗体(Nanobodies)来携带DNA。利用酶促反应【2,3】,研究者可以大量制备携带不同序列DNA寡核苷酸的纳米抗体(Nb-DNA)(图1)。该纳米抗体可以位点特异性地和IgG的可结晶片段区域(Fc)结合【4】,而不会影响到IgG的抗原识别区域(Fab),尽可能地减少了对IgG抗原识别能力的潜在干扰。利用纳米抗体单价结合的特性,研究者可以简单地将需要标记的IgG抗体与某一特定序列的Nb-DNA直接混合,从而实现抗体的DNA条形码标记。在给每种IgG抗体带上独特的DNA条形码后,靶向不同抗原分子、来自同一种属源的抗体就可以直接混合在一起进行后续的实验应用(图1)。
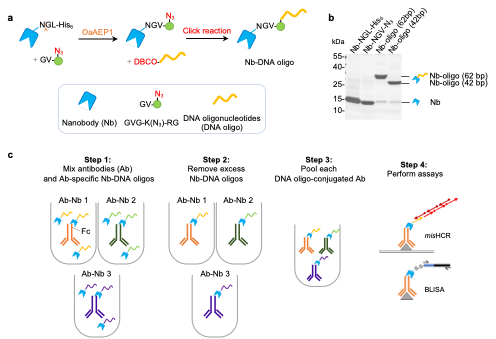
图1: MaMBA策略设计
研究者将MaMBA策略与前期开发的isHCR免疫信号放大方法【5】结合,有效地将isHCR实验流程简化为一步染色(misHCR,图2)。在此基础之上,研究者在纳米抗体和DNA寡核苷酸之间引入了一个二硫键连接物(disulfide linker),发展了可切除版本的MaMBA策略(图2)。通过将可切除版本的MaMBA策略与misHCR方法相结合,进一步拓展了该方法的多重检测能力(misHCRn,图2)。研究者使用misHCR方法对银屑病患者的皮肤活检样品进行6种细胞类型生物标记物的多重免疫染色(图2),在这当中同时使用了4种兔源IgG一抗和2种小鼠源IgG1一抗,misHCR成功地展示了每种细胞类型的不同定位模式。研究者分别使用3轮和2轮misHCRn成功对小鼠中缝背核(Dorsal Raphe Nucleus)脑区切片样品进行9种和12种靶标蛋白的原位成像,且所用一抗均为兔源IgG。这些结果表明,基于MaMBA的misHCR方法可以实现特异性的、灵活的以及多重的原位生物分子成像。
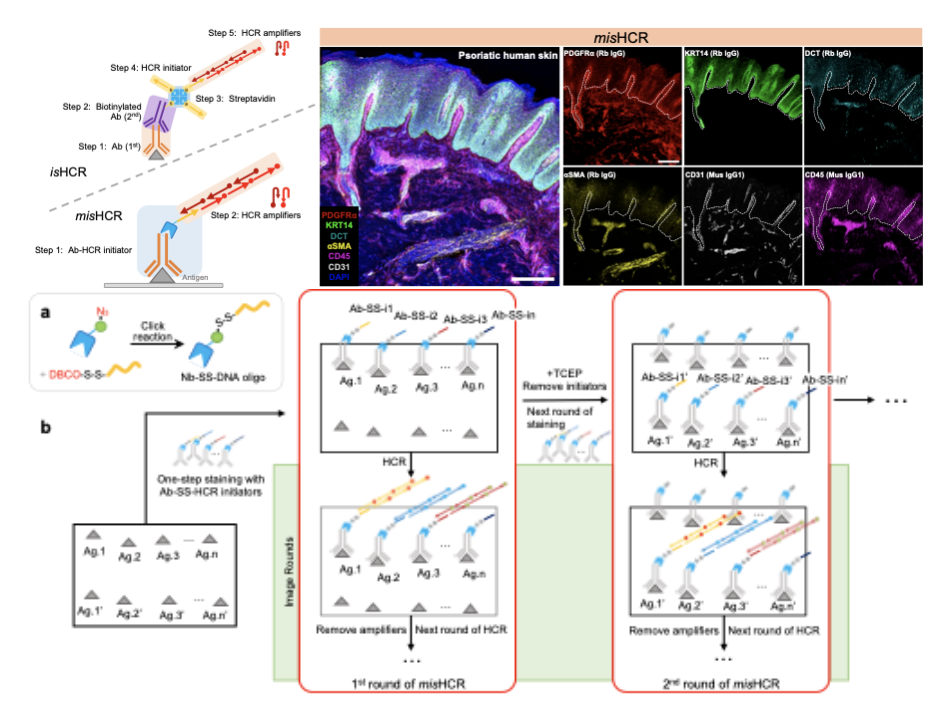
图2: misHCR/misHCRn多重免疫染色成像
研究者还将MaMBA策略与经典ELISA技术结合,开发了可用于多重生物分子检测的方法BLISA。区别于经典ELISA中使用荧光或化学发光等光学手段来读取信号,BLISA利用检测抗体所携带的DNA条形码作为信号读出,通过高通量测序技术量化每一特定序列的DNA条形码,从而推断出样品中对应目标分子的相对数量(图3)。研究者使用BLISA成功在约500份人血清样品中快速检测抗严重急性呼吸系统综合症冠状病毒2型(SARS-CoV-2)IgG抗体,并成功在超过1000份人血清中实现对2种乙肝重要抗原标志物—乙肝表面抗原(HBsAg)和乙肝e抗原(HBeAg)的同时检测。研究者还使用磁珠(Magnetic beads)作为结合介质来替代传统的微孔板(酶标板),进一步提升了BLISA的多重检测能力,实现对8个目标蛋白的同时、高通量检测(图3)。
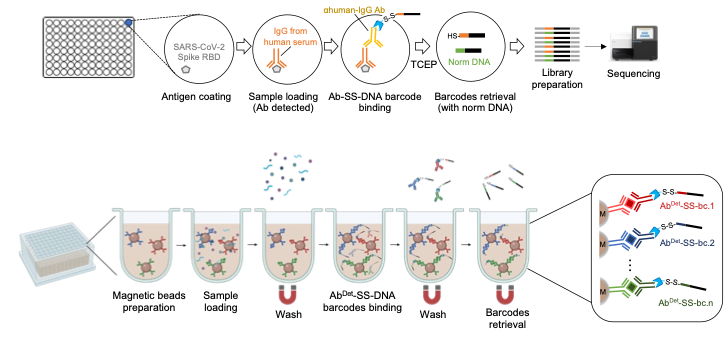
图3: 测序联合以及结合磁珠的BLISA检测
综上,该研究开发了MaMBA策略,提供了一种有潜力的对抗体进行DNA条形码标记的方法,验证了应用于不同免疫检测方法的可行性和通用性。这种简单的DNA条形码标记的制备流程有利于以更高的效率和更低的成本获得标记抗体,有助于基于DNA条形码标记抗体的技术的广泛应用以及新技术的开发。
论文信息
北京生命科学研究所林睿实验室博士后钟诗琳博士(罗敏敏实验室博士毕业生)为该论文第一作者,北京脑科学与类脑研究所罗敏敏博士与北京生命科学研究所/清华大学交叉医学研究院林睿博士为共同通讯作者。该论文的其他作者还包括北京脑科学与类脑研究所罗敏敏实验室王睿宇博士、光学影像中心工程师高辛未、光学影像中心主任郭青春博士。本研究得到了北京生命生命科学研究所/清华大学交叉医学研究院陈婷博士对于提供皮肤样本的支持。SARS-CoV-2 IgG和HBV抗原检测实验的试剂以及血清样本由北京万泰生物药业、北京大学国际医院和北京天坛医院提供支持。感谢罗敏敏实验室和林睿实验室的所有成员在本研究中的协助与支持。
本研究受科技部科技创新 2030-「脑科学与类脑研究」重大项目、中国医学科学院医学神经生物学创新单元、新基石研究员项目、北京市科技新星计划、国家自然科学基金委及北京市政府的资助。
原文链接
https://elifesciences.org/articles/105225
参考文献
1. Dovgan, I., Koniev, O., Kolodych, S. & Wagner, A. Antibody–Oligonucleotide Conjugates as Therapeutic, Imaging, and Detection Agents. Bioconjug. Chem. 30, 2483–2501 (2019).
2. Rehm, F. B. H. et al. Site-Specific Sequential Protein Labeling Catalyzed by a Single Recombinant Ligase. J. Am. Chem. Soc. 141, 17388–17393 (2019).
3. Yang, R. et al. Engineering a Catalytically Efficient Recombinant Protein Ligase. J. Am. Chem. Soc. 139, 5351–5358 (2017).
4. Pleiner, T., Bates, M. & Görlich, D. A toolbox of anti–mouse and anti–rabbit IgG secondary nanobodies. J Cell Biol 217, 1143–1154 (2018).
5. Lin, R. et al. A hybridization-chain-reaction-based method for amplifying immunosignals. Nat. Methods (2018) doi:10.1038/nmeth.4611.



