大脑如何“计算”损伤?北京脑所井淼团队揭示胶质细胞反馈回路实现损伤信息的动态校准和平衡应答 | Neuron
中枢神经系统损伤是导致全球慢性残疾和死亡的主要原因之一[1]。急性损伤发生后,大脑会启动复杂的内源反应以应对创伤并维持组织正常功能,然而过度或持续存在的应答反应可能破坏组织完整性,进而引发继发性损伤和长期功能障碍[2]。损伤应答的强度、时间以及空间分布需要被精确调控,以匹配损伤程度并确保适度反应,然而其具体的调控机制仍然未被完全解析。

2026年4月15日,北京脑科学与类脑研究所井淼团队在 Neuron 期刊在线发表了题为 “A reciprocal glial circuit calibrates injury information and governs the tissue response balance” 的研究文章。
井淼课题组在近期工作中揭示了大脑损伤中存在一类特征性的闪烁状ATP信号(Inflare),其不同于伴随细胞凋亡的被动ATP泄露,可特异性的由损伤周围的星形胶质细胞释放并独立的影响损伤应答和组织结局[3]。
在本工作中,研究团队进一步探索了星形胶质细胞ATP信号介导的损伤应答如何维持其稳定性。利用激光诱导不同程度的大脑损伤,研究团队定量刻画了组织创伤程度与Inflare性质之间的关系,发现Inflare的频率、随时间和空间的分布规律均与组织损伤程度呈线性关系,表明内源星形胶质细胞ATP介导的应答过程与损伤自身具有严格的对应关系,存在平衡的类稳态的调控过程。
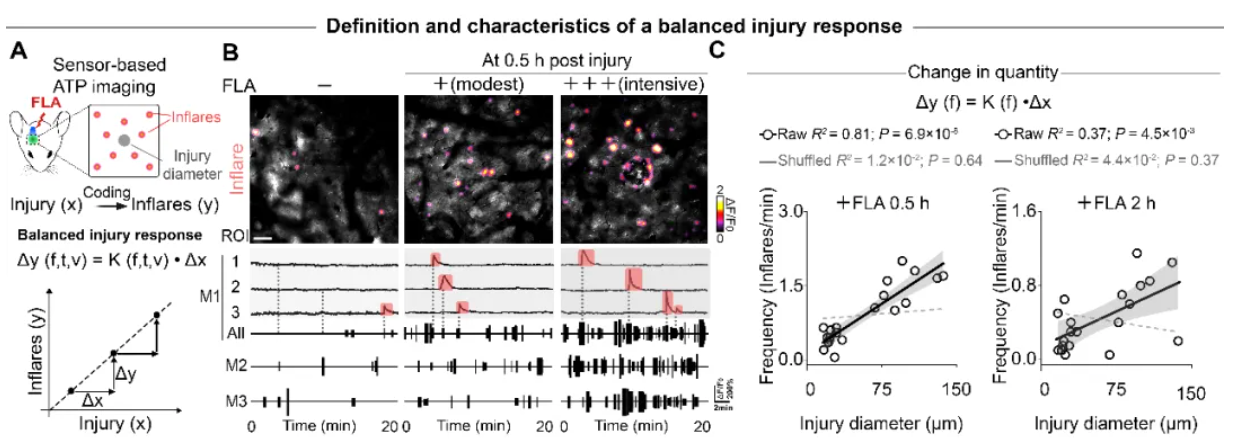
图1. Inflare与损伤的定量关系支持平衡调控的内源损伤应答过程
1. 小胶质细胞负反馈调控星形胶质细胞ATP释放以维持损伤应答稳态
机体内的平衡调控常通过负反馈调节来实现。为了探索星形胶质细胞ATP释放是否接收来源于其他细胞的反馈调控,研究团队对脑内不同细胞进行了干预,最终锁定了小胶质细胞作为潜在的调节者。小胶质细胞不仅具有感知ATP的对应受体,也可释放多种化学物质影响星形胶质细胞的活性。
为了直接评估小胶质细胞在稳态反应中的必要性,作者通过CSF1R抑制剂清除小胶质细胞,或通过去除药物以促进小胶质细胞的再殖,并在整个过程中记录损伤诱导的Inflare事件。结果表明,小胶质细胞清除导致相同强度损伤诱发的Inflare事件显著升高,而其再殖又可重塑Inflare与损伤之间的对应性,使其在群体频率和时空分布上恢复到接近正常状态。
为了进一步探索小胶质细胞自身状态是否影响其反馈能力,作者通过敲除小胶质细胞的ATP受体P2Y12,或通过化学遗传学方法特异性的干预小胶质细胞的活性。P2Y12受体的缺失导致小胶质细胞降低了其负反馈能力,体现为更多的损伤诱导的ATP释放。相反,化学遗传学操控小胶质细胞的活性增强了其负反馈能力,从而压低了损伤导致的ATP释放。
这一系列实验结果证明小胶质细胞的存在对星形胶质细胞Inflare的释放具有负反馈抑制作用,且其可动态的调整负反馈的强度从而维持损伤应答的平衡。两类细胞之间通过特定且动态变化的化学递质通讯形成了交互式的胶质细胞回路,从而对损伤信息进行校准并动态维持内源应答的稳定性。
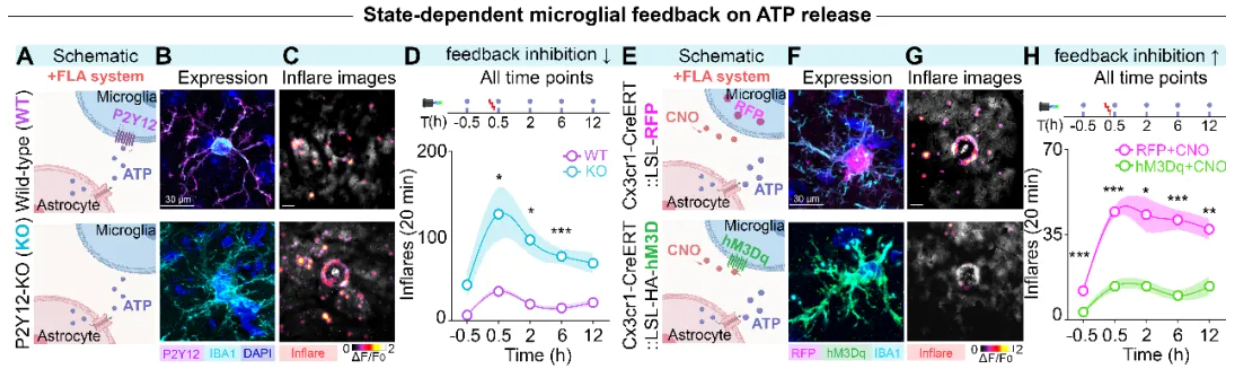
图2. 小胶质细胞整合自身状态实现可调的反馈抑制并调控损伤应答
2. 胶质细胞IL-1β–IL-1R1信号轴介导对星形胶质细胞ATP释放的负反馈调控
研究团队进一步探索了小胶质细胞执行负反馈功能的具体分子机制。通过对组织基因表达水平进行测序分析,作者锁定了部分细胞外分泌的因子作为潜在的因素,并建立了体外的筛选体系探究特定分子是否具有抑制损伤诱导ATP释放的能力。
筛选最终锁定白介素IL-1β作为潜在的抑制分子,其能够强烈且快速的抑制损伤诱导的Inflare事件的出现,且该效果可被IL-1β的中和抗体或其受体拮抗剂所阻断。作者进一步在体内注射IL-1β受体IL-1R的阻断药物Anakinra,发现其可明显抑制内源IL-1β的负反馈功能,从而造成损伤诱发更多的Inflare释放。
通过细胞特异性的遗传学筛选,作者分别构建了小胶质细胞特异性的IL-1β敲除品系和星形胶质细胞IL-1R1受体的敲除品系,进一步证明了该负反馈抑制为小胶质细胞IL-1β直接作用于星形胶质细胞受体所造成的,为该稳态损伤反应提供了分子基础。
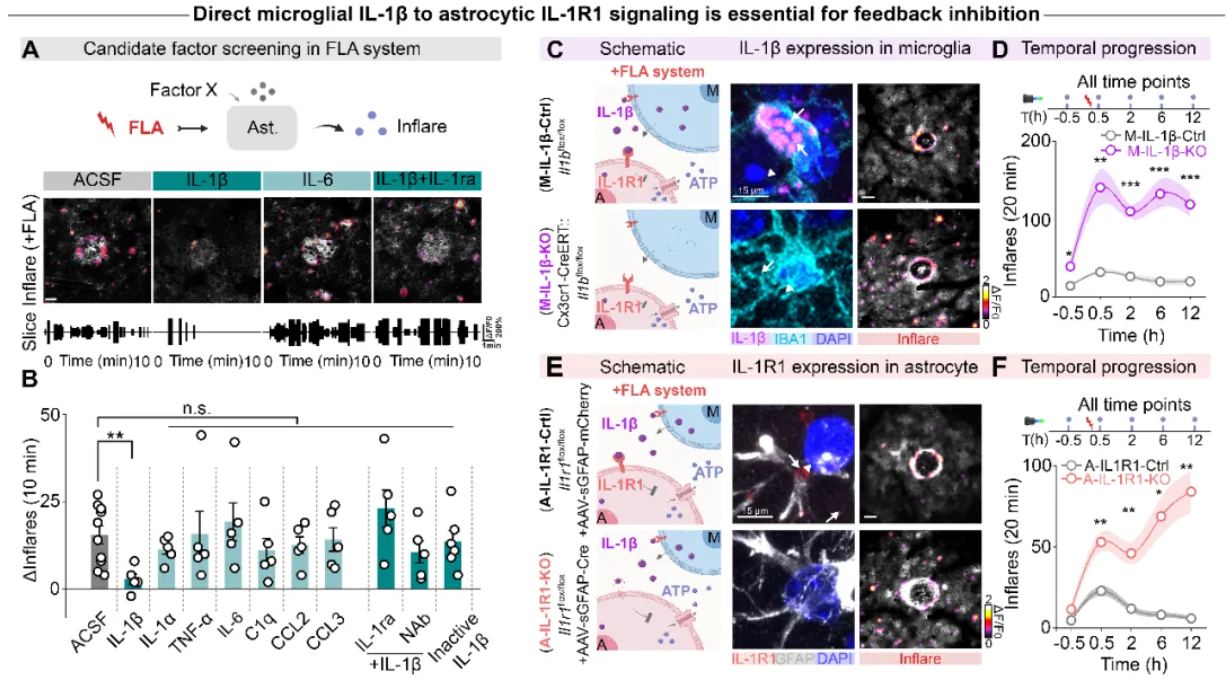
图3. 小胶质细胞和星形胶质细胞通过IL-1β-IL-1R轴的直接相互作用调节应答
3. ATP–IL-1β协同调控损伤应答及其对损伤结局的双重作用
ATP与IL-1β分子均为经典的炎症诱导分子,其阻断常被用于治疗脑损伤和炎症等疾病,暗示其在损伤中扮演恶化损伤结局的作用。然而,本工作揭示了星形胶质细胞ATP和小胶来源的IL-1β共同塑造了稳态的损伤应答平衡,其中IL-1β扮演了负向调控损伤信号的功能,与其传统的促炎功能截然不同。
为了探究该胶质细胞网络介导的平衡性损伤应答对损伤结果的影响,作者通过构建局部创伤性脑损伤模型,系统性的评估缺失小胶IL-1β负反馈对损伤结局的影响。小胶质细胞特异性敲除IL-1β可以显著增加损伤前期的组织破坏和细胞凋亡,表明该负反馈调控介导的内源应答平衡对短期损伤结局具有积极的影响。相对的,在该局部损伤模型中长期的损伤结局并未受到小胶质细胞IL-1β敲除的改变。
综上表明,ATP与IL-1β介导的胶质细胞相互作用通过协调多细胞适应过程,以细胞特异性和损伤状态依赖的方式影响组织的功能结局。这同时提示干预该类损伤和炎症相关分子的治疗方法需要同时考虑其在不同应答反应中的异质性功能,从而更好的保护脑组织并治疗损伤相关疾病。
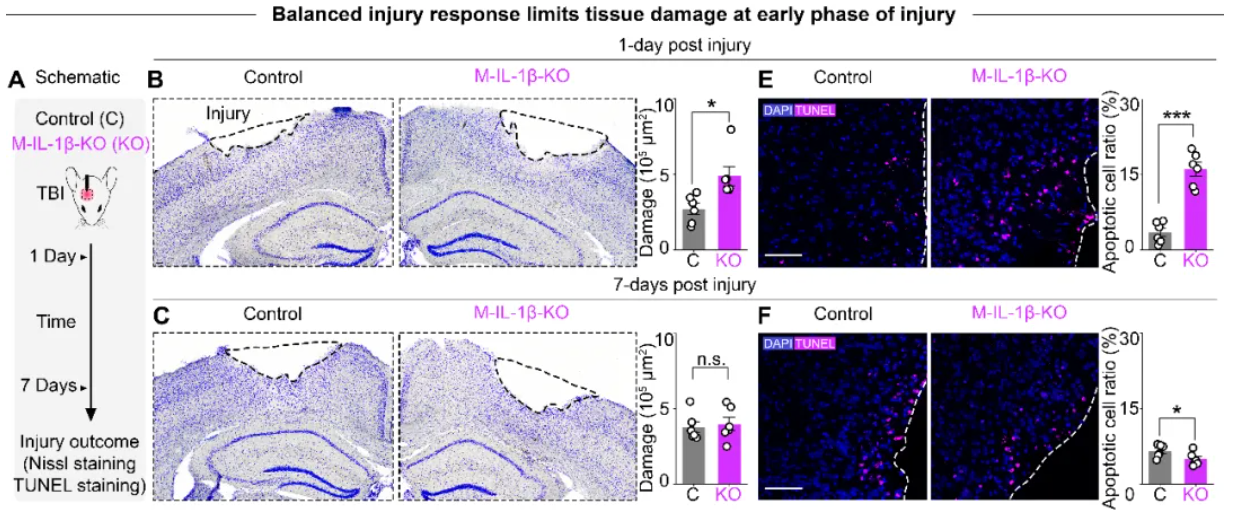
图4. 损伤应答平衡的破坏加剧损伤早期阶段的预后结果
总结
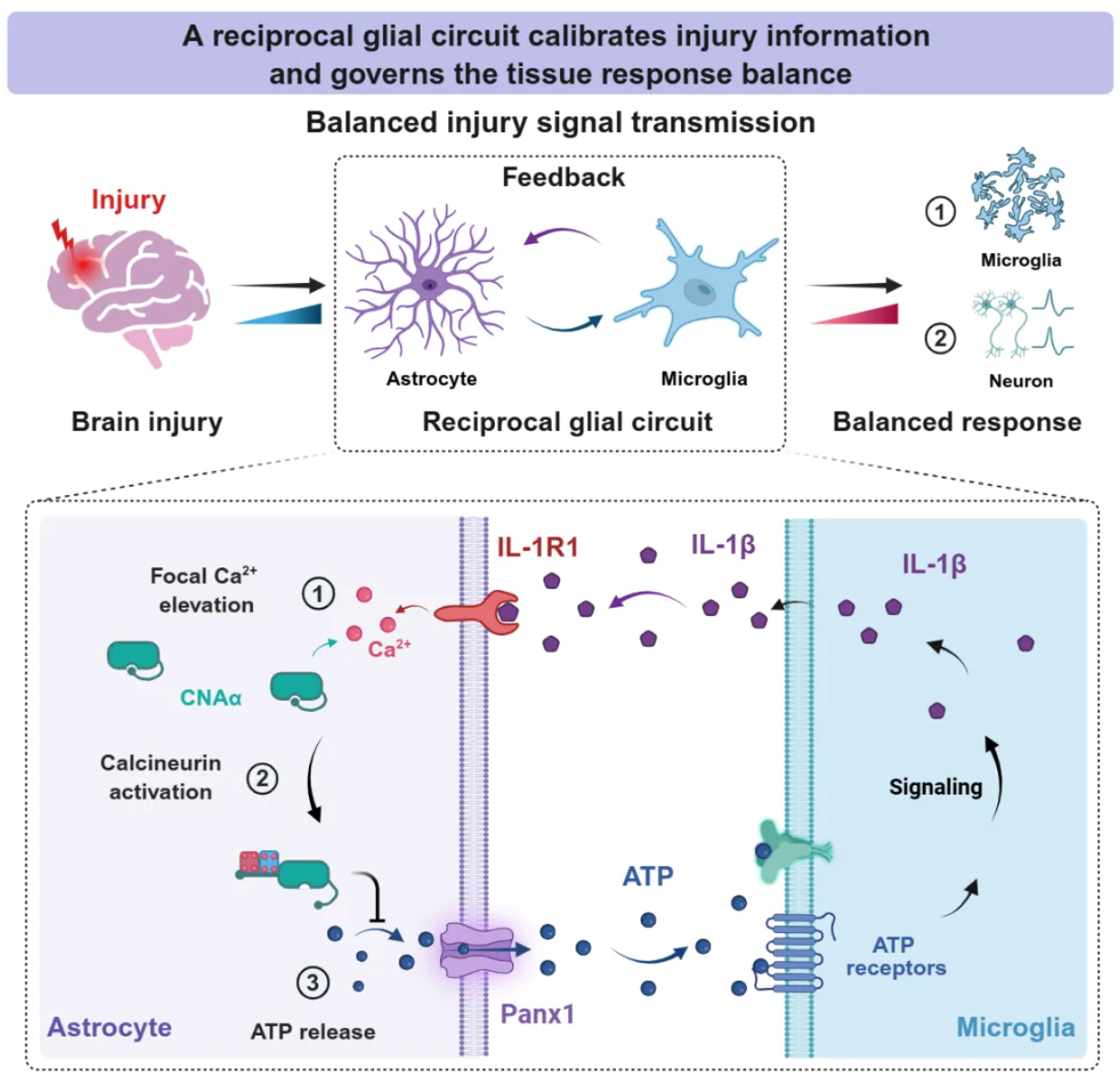
本文揭示了存在于大脑胶质细胞之间的交互式信号通路,其以动态调控ATP和白介素IL-1β的方式校准损伤信息,并对组织损伤应答的稳态和功能结局产生重要的影响。
胶质细胞的协同像是表演者与调音师之间的互动,其中星形胶质细胞如同不断输出信号的“演奏者”,将损伤信息转化为可被感知的动态模式(Inflares);小胶质细胞则类似“调音师”,基于当前的演奏信息进行实时的整合与反馈校准,从而确保演奏的平稳。
该过程不同于经典的ATP和IL-1β在放大炎症反应中的正反馈功能,而是通过负反馈回路实现损伤应答的平衡调控,并对损伤结果产生积极影响。相应的,破坏该环路中的任何一环均会导致损伤应答平衡的破坏并改变创伤结局,提示其在损伤相关疾病的发生和发展中具有重要的意义。
论文信息
本工作由北京脑科学与类脑研究所井淼实验室与匈牙利HUN-REN实验医学研究所Ádám Dénes实验室合作完成,井淼为最后通讯作者。北京脑科学与类脑研究所、北京大学联合培养博士生栾朋伟为该论文的第一作者。井淼实验室成员贾剑铭(现深圳医学科学院博士生),陈阅(现清华大学博士生),席凤雪等,以及匈牙利HUN-REN实验医学研究所Anett D. Schwarcz等对工作做出重要贡献。感谢北京脑科学与类脑研究所的罗敏敏教授、赵瑚教授和周景峰教授,以及来自中国科学院的徐敏教授和武照伐教授提供转基因小鼠等资源。本研究获得国家科技创新2030“脑科学与类脑研究”重大项目,科技部政府间科技创新合作项目等的资金支持。
参考文献
1. Spencer, L., James., Alice, T., and Richard, G., Ellenbogen. (2019). Global, regional, and national burden of traumatic brain injury and spinal cord injury, 1990-2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet Neurol 18, 56-87. 10.1016/S1474-4422(18)30415-0.
2. Simon, D.W., McGeachy, M.J., Bayır, H., Clark, R.S., Loane, D.J., and Kochanek, P.M. (2017). The far-reaching scope of neuroinflammation after traumatic brain injury. Nature reviews. Neurology 13, 171-191. 10.1038/nrneurol.2017.13.
3.Chen, Y., Luan, P., Liu, J., Wei, Y., Wang, C., Wu, R., Wu, Z., and Jing, M. (2024). Spatiotemporally selective astrocytic ATP dynamics encode injury information sensed by microglia following brain injury in mice. Nat Neurosci 27, 1522-1533. 10.1038/s41593-024-01680-w.



