Genome Research | 北京脑所Koziol团队发现高密度m6A修饰转录本与阿尔茨海默症等神经系统疾病显著关联
2024年7月16日,北京脑科学与类脑研究所Koziol实验室博士生冯爽爽以及其他合作者在《基因组学研究》(Genome Research)在线发表了题为“Single cell discovery of m6A RNA modifications in the hippocampus”(小鼠海马单细胞中RNA修饰m6A的研究)的研究论文。
冯等人在单细胞单分子分辨率下研究了海马体中的m6A,绘制了单个相同细胞内m6A修饰的图谱。研究者发现了一些具有高密度m6A修饰的转录本,这些转录本与阿尔茨海默症等神经系统疾病有显著关联。此外研究结果表明,富集了m6A修饰的转录本在CAMK2A神经元中起着关键作用。
N6-methyladenosine (m6A)是精细调控大脑功能的指挥官
N6-methyladenosine (m6A),哺乳动物大脑中含有最高丰度的m6A甲基化修饰1,能调控大脑的发育与功能,m6A的紊乱直接或间接导致脑的相关疾病2,因此m6A在大脑这个复杂的组织中发挥着重要的作用。
单细胞测序技术革新了对复杂组织中细胞异质性和不同亚群的理解3,将这一技术应用于m6A的研究,将深度揭示m6A在海马功能中的细胞特异性作用,并推动未来靶向治疗的发展。研究者首先优化并增强了m6A的检测技术,并成功将其应用在小鼠的海马区域,这项工作使单细胞单分子水平研究复杂组织中的m6A修饰成为可能,并为未来研究健康和疾病大脑中RNA m6A精细的动态调控奠定了基础。
优化并加强m6A的检测方法-可视化m6A细胞
为了在复杂的脑组织小鼠海马中更好地在单细胞水平检测到m6A修饰,研究者优化并强化了非抗体依赖的DART-seq(Deamination adjacent to RNA modification targets sequencing)技术4,该方法的优势是前期通过在体内表达融合蛋白APOBEC1-YTH(对照YTHmut、APOBEC1),通过将胞嘧啶脱氨酶APOBEC1与YTHDF2的m6A结合结构域YTH融合,APOBEC1-YTH可以将m6A邻近的胞嘧啶编辑为尿嘧啶,后期无需对单细胞测序过程中的产物进行任何处理,m6A通过测序数据中的突变进行检测。若想在体内每个细胞中表达该融合蛋白是不易的,如何区分融合蛋白表达的细胞还是背景细胞,对于准确获取m6A修饰的信息至关重要,于是本研究通过将该蛋白APOBEC1-YTH等与EGFP利用H2A序列进行连接,便能可视化m6A细胞,从而将EGFP细胞分选并富集出来,减少背景细胞带来的错误信息,从而提高m6A信息的可信度。
本研究提供了一个思路,在构建载体时,将EGFP的编码序列插在融合蛋白编码的序列之前(E-YTH),与EGFP插在融合蛋白编码的序列之后相比(YTH-E),YTH-E和E-YTH确认了先前的m6A研究结果即存在RNA的C端。E-YTH具有更强的EGFP表达信号,以及和APOBEC1-YTH融合蛋白存在更清晰的相关性,同时其m6A分布模式更明确且背景信号更低(图A),因此被选用于海马研究。
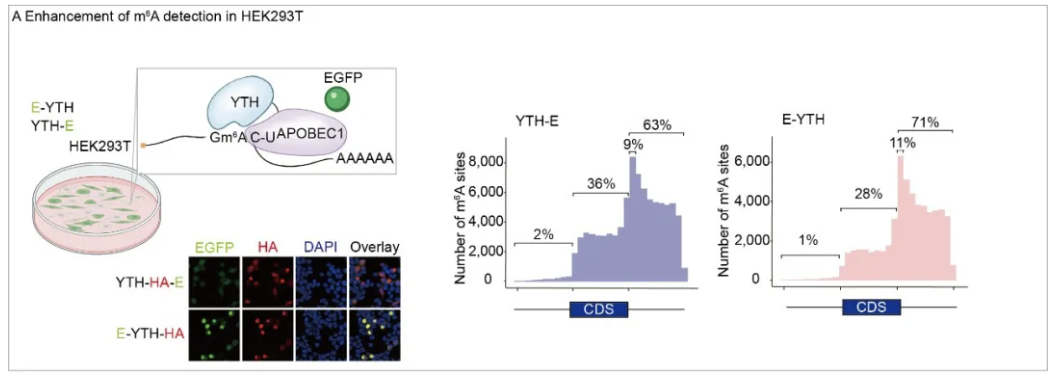
图A Enhancement of m⁶A detection in HEK293T
海马单细胞m6A修饰的图谱绘制
研究者在小鼠海马内表达优化后的融合蛋白E-YTH(对照E-YTHmut、E-APOBEC1),对富集之后m6A细胞进行单细胞测序与分析,他们将海马中的细胞分为五类,包含少突胶质细胞谱系、免疫细胞谱系、神经元细胞谱系、星形胶质细胞谱系、内皮细胞谱系。每种细胞类型中检测到的修饰数量不同,少突胶质细胞谱系含有的m6A位点最多,免疫细胞谱系、神经元细胞谱系、星形胶质细胞谱系、内皮细胞谱系依次减少。这些m6A位点在RNA上的位置分布在不同五种细胞类型中不同,其中在少突胶质细胞谱系与免疫细胞谱系中有代表性的不同,m6A位点在RNA上的位置在少突胶质细胞谱系中更符合经典的m6A修饰的位置分布即在终止密码子附近以及3’UTR区域,而在免疫细胞中,m6A修饰在终止密码子的N端也有富集(图B),不同细胞类型中m6A的丰度和基因分布位置的差异表明未来急需探索m6A在调控不同大脑发育和功能中的作用。
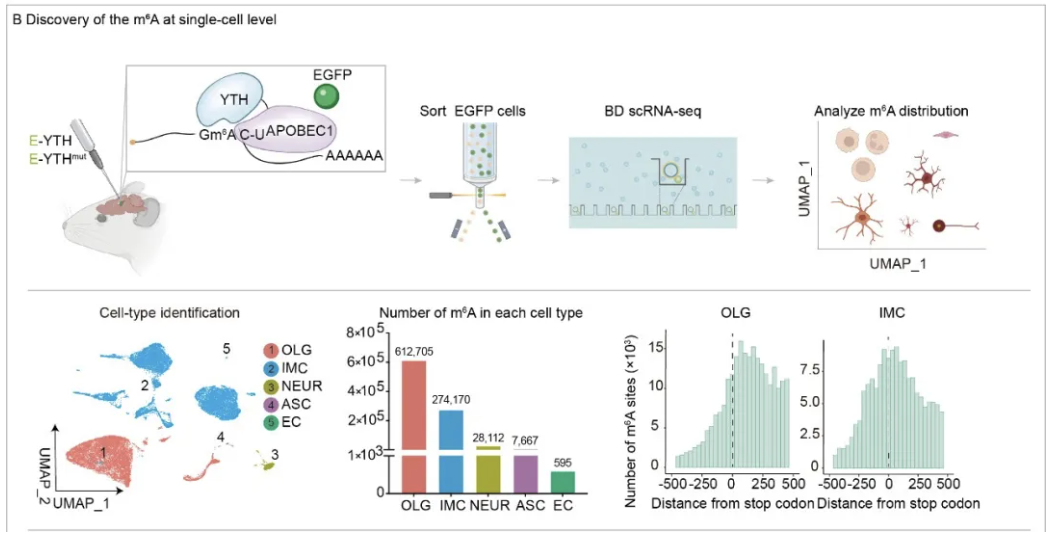
图B Discovery of the m⁶A at single-cell level
阿尔茨海默症相关基因出现高密度m6A修饰
许多疾病基因,如在少突胶质细胞中显著表达的阿尔茨海默病相关基因App,其RNA上具有大量的m6A修饰。因此,冯等人首次揭示了App或其他类似高甲基化转录本可能是m6A调控疾病疗法的良好靶点。这一发现为未来研究m6A RNA甲基化在疾病脑中的调控作用奠定了基础,并为未来靶向药物疗法开辟了新的途径(图C)。
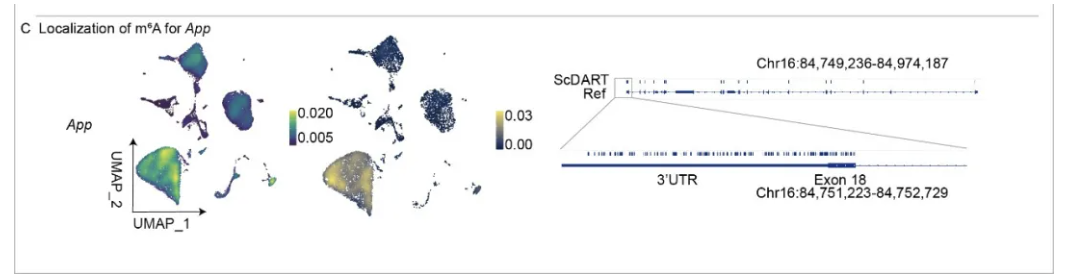
图C Localization of m⁶A for App
Koziol团队在国际上首次在单细胞水平绘制了小鼠海马RNA修饰m6A图谱以及相应基因的表达谱。为了更快速地了解目标基因上的m6A图谱及其对应的基因表达谱,研究者将所有检测到的基因的m6A图谱和表达谱整合到数据库中,并以网站形式提供交互搜索服务。用户只需在https://scm6a.cibr.ac.cn/的搜索框内输入基因名称,即可展示相应的图谱。
参考文献
1. Y. Yue, J. Liu, C. He, RNA N6-methyladenosine methylation in post-transcriptional gene expression regulation. Genes Dev 29, 1343-1355 (2015).
2. Y.-P. Yen, J.-A. Chen, The m6A epitranscriptome on neural development and degeneration. Journal of Biomedical Science 28, 40 (2021).
3. A. Regev et al., The Human Cell Atlas. eLife 6, e27041 (2017).
4. K. D. Meyer, DART-seq: an antibody-free method for global m(6)A detection. Nat Methods 16, 1275-1280 (2019).
作者信息
Shuangshuang Feng1,2,3, Maitena Tellaetxe-Abete4,7, Yujie Zhang2,3,7, Yan Peng2,3,5, Han Zhou2, Mingjie Dong2, Erika Larrea2,3,6, Liang Xue2,3, Li Zhang2, Magdalena J. Koziol1,2,3,8,*
1- State Key Laboratory of Cognitive Neuroscience and Learning, Beijing Normal University, Beijing, 100875, China
2- Chinese Institute for Brain Research, Beijing, 102206, China
3- Research Unit of Medical Neurobiology, Chinese Academy of Medical Sciences, Beijing, 102206, China
4- Intelligent Systems Group, Computer Science Faculty, University of the Basque Country, Donostia/San Sebastian, 20018, Spain
5- Peking University, Beijing, 100871, China
6- Tsinghua University, Beijing, 100084, China
7- These authors contributed equally
8- Lead Contact



