Nat Neurosci | 北京脑所井淼团队揭示具有高度时空特异性的ATP信号Inflare在主动编码和呈递损伤信息中的作用 2024-06-11
中枢神经系统的损伤,包括来源于交通事故、跌落等外源性创伤以及伴随着卒中、病毒感染等造成的内源性病理变化,是目前全球范围内致死致残的首要因素之一,严重影响了人类健康和社会经济发展1,2。遗憾的是,目前治疗创伤的大多数手段侧重于应对创伤源头本身,将其视为相对被动的、由细胞死亡引发的过程,而忽略了大脑内部对损伤信号的主动响应及其编码过程,以及该过程在疾病发生和发展之中的可能贡献。造成该问题的根本原因在于缺乏对于脑损伤内部应答机制的深入理解。
2024年6月11日,北京脑科学与类脑研究所的井淼实验室在Nature Neuroscience杂志上发表题为"Spatiotemporally selective astrocytic ATP dynamics encode injury information sensed by microglia following brain injury in mice"的研究文章,首次揭示了一种具有高度时空特异性的ATP信号——Inflare在主动编码和呈递损伤信息中的重要作用。研究发现损伤附近的星形胶质细胞作为监视器可灵敏地捕捉脑内的损伤信息,并将其以“电报”Inflare的方式进行时空上的放大和传递,从而精确高效的指引小胶质细胞进行迁移和损伤应答。重要的是,异常的Inflare电报发放造成的损伤信息错误传递可直接改变损伤后果,而在小鼠卒中模型中靶向Inflare可挽救异常信息传递并明显改善康复效果。该研究为理解脑内损伤应答信息编码和传递机理及其在疾病治疗中的潜在应用奠定基础。

细胞外ATP(腺苷酸三磷酸, Adenosine Triphosphate)是损伤后高度富集并起到重要生理功能的关键信号分子3。ATP升高可通过激活小胶质细胞(microglia)表达的P2y12受体,引发小胶质细胞向损伤区域迁移,参与炎症反应和细胞清除等修复过程4。由于细胞内外的ATP浓度存在上千倍的差异5,研究者普遍认为ATP信号传导是一个被动过程,即由于细胞死亡造成的细胞膜破裂导致细胞内ATP的泄露,“被动的”引发了后续的损伤修复结果6。然而,近年来对于损伤修复过程的深入理解对ATP信号的释放模式提出了疑问,如由细胞死亡造成的释放如何受到精确调控以实现修复过程和损伤之间的匹配,以及易降解的胞外ATP如何实现长时间稳定的小胶质细胞招募。这都指向了脑内损伤应答相关的ATP信号可能存在更加复杂精确的调控和释放模式。
时空特异性的ATP释放事件Inflare编码内源损伤信号
为了精确地观测大脑内部ATP的时空变化,研究者采用激光聚焦损伤模型 (FLA)精确可控的在活体清醒小鼠皮层引发局部损伤,并使用近期开发的荧光探针ATP1.07对细胞外ATP信号进行实时高灵敏的双光子成像记录。ATP信号在损伤前未出现明显的波动,而在局部FLA后可观测到两类明显的ATP信号:一类位于损伤中心呈现强烈且集中的释放(Burst),另一类为重复性的在整个视野内产生、如同烟花般闪烁的时空特异性ATP释放事件,命名为Inflare (Injury-induced flashing ATP release)。应用不结合ATP的突变型探针,研究者确认了该类信号特异的指示胞外ATP的动态变化,而非细胞死亡造成的自发荧光。同时,应用AQuA软件8可对ATP事件进行高精度的识别和特征提取,并进一步确认Burst和Inflare表现出截然不同的单信号特征,表明其代表不同类型的ATP释放模式。
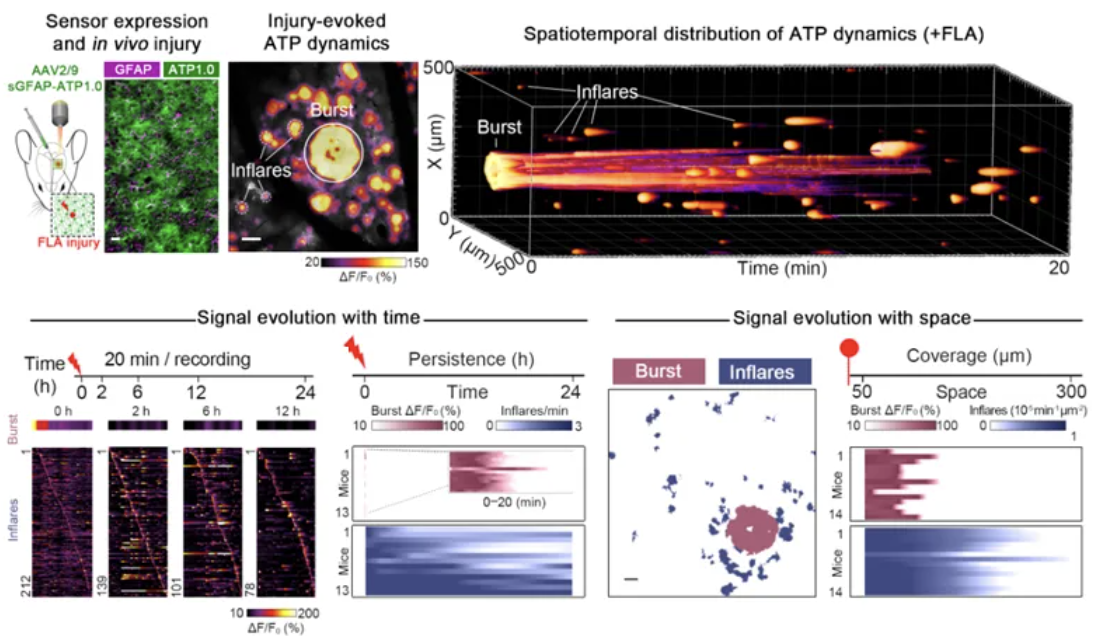
图一 脑内损伤引发的ATP事件的实时灵敏观测
是否其中一类ATP可作为损伤编码的内源信号?以内源小胶质细胞分支向损伤方向的定向延伸作为损伤的应答指标,研究者们首先对激光损伤及其应答的时空特性进行了细致分析。有趣的是,短暂的(2秒)激光照射可以引发持续数小时的小胶质细胞迁移,而小胶质细胞响应的范围(约300微米)远远超过激光所损伤的区域(50微米)。这暗示着,小胶质细胞依赖信号来对损伤进行放大和呈递,且该类信号需要与小胶质细胞响应的时空特性相匹配。基于此,研究者通过长时间大视野的双光子成像对两类ATP释放事件进行了进一步刻画。虽然损伤中心的Burst信号相比于单个Inflare具有更大的面积和更长的持续事件,但其仍然集中在损伤旁100微米的范围内,而无法进行大范围的信号传递,且其在损伤后20分钟内即完全消失。相对的,Inflare在群体上具有更加广泛的覆盖范围,且在损伤20小时后仍然能看到再次出现的Inflare闪烁,表明其在时间上具有极高的持续性。因此,基于对ATP信号的时空特异性的观测和分析,研究者锁定了Inflare这类持久且广泛分布的事件作为潜在的损伤编码和呈递信号。
Inflare通过在时空上的群体频率分布进行损伤的多维编码
Inflare作为一类潜在的信号分子,其可能使用独特的策略对损伤进行编码,如通过增加每个Inflare的大小进行单信号尺度的编码,或通过改变出现数量/频率进行群体尺度的编码。受益于对Inflare信号的灵敏观测和信息提取,研究者可通过比较不同损伤条件下的Inflare特征,尝试破译其编码损伤的密码。在给予不同强度的损伤下,研究者们惊奇的发现单个Inflare的信号特征并未发生明显的改变,其反应幅值、持续时间和影响范围均维持固定,暗示单个Inflare可能作为基础的信号编码单元呈现出“全或无”的特性。相对的,增加脑损伤强度造成了Inflare群体频率的显著增加,且可以通过频率信息对记录的Inflare进行对应损伤强度的分群。为了进一步支持Inflare通过频率编码的机制,研究者们将包含Inflare不同特征的参数用于构建支持向量机的模型,通过赋予每个参数不同的权重尝试反向预测损伤强度。模型成功实现了基于Inflare的损伤强度预测,且单个信号相关的参数均具有较低的权重,而群体的频率对模型的成功预测贡献最大。模型提供的定量关系进一步支持了Inflare通过类似于神经元动作电位的频率调节来进行损伤强度信息的编码。
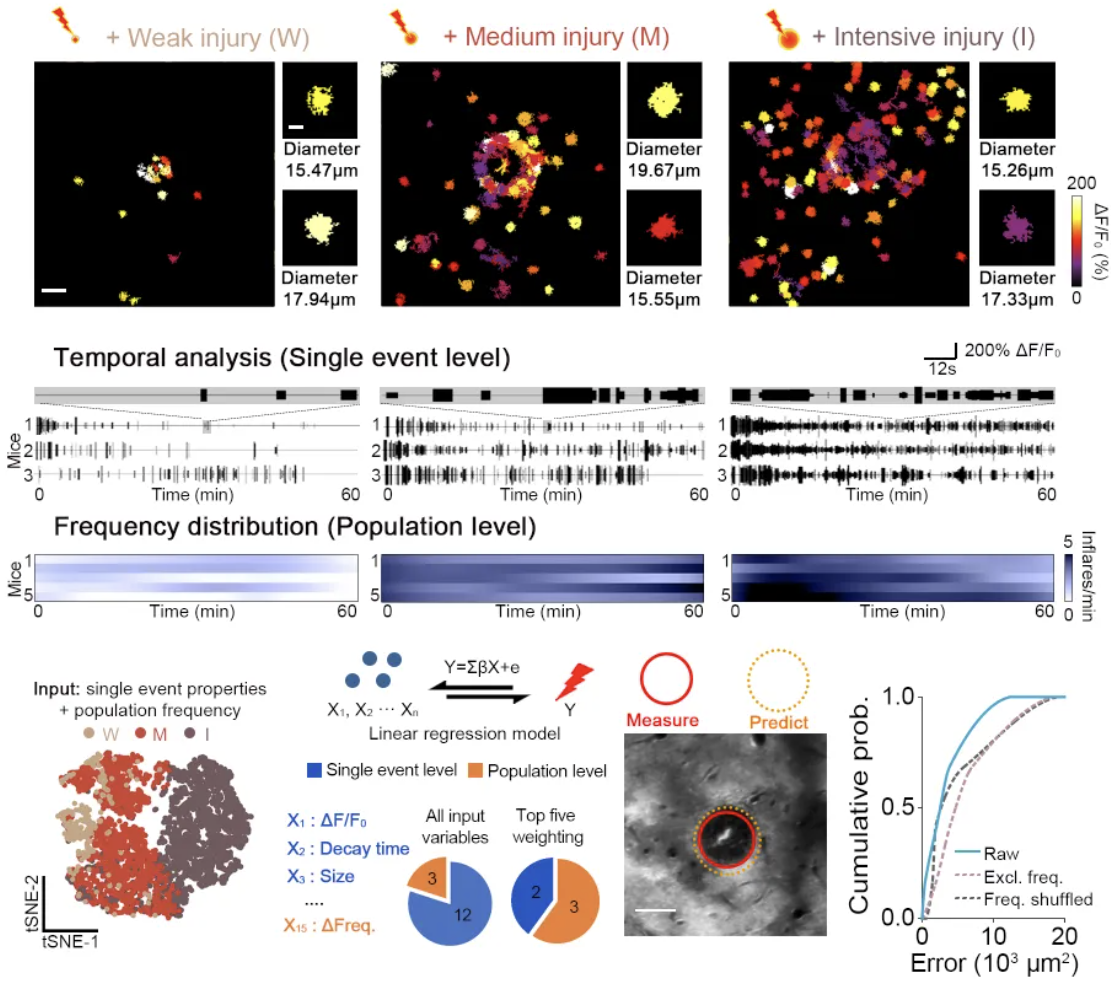
图二 Inflare通过群体频率的变化进行损伤强度的编码
如上所述,脑损伤应答中一个重要的指标为小胶质细胞的定向迁移,该过程长期被认为受到ATP浓度梯度的影响。然而,通过对损伤ATP信号的记录否定了大范围持续性ATP浓度梯度的存在。那么,ATP如何实现对损伤位置的编码呢?由于单个Inflare的持续时间短暂,研究者推测Inflare在空间上也通过群体层面编码损伤的位置信息。研究者们观测到,当将一段时间的Inflare在同一空间上进行投影时,Inflare数目随着损伤中心的距离增加而逐步减少,形成了一种概率密度梯度。该梯度覆盖了超过300微米的广泛空间并能在损伤后维持数十小时,表明其可有效地提供迁移所需的方向性。由于信号梯度在编码相对变化中的优势,研究者比较了在不同损伤条件下梯度的差异,发现虽然给予强弱损伤造成了Inflare数目上接近10倍的差别,但其同样形成了类似斜率和影响范围的概率梯度,表明该梯度可以在不依赖绝对数目的情况下稳定编码方向性。改变损伤发生的空间位置可造成Inflare密度梯度的空间位置改变,且梯度的中心和损伤发生点具有极高的匹配性,表征Inflare在编码损伤空间信息的准确性。通过改变损伤的形状,研究者进一步揭示了该密度梯度还可编码损伤更加复杂的空间特性,从而精巧的指导小胶质细胞的空间定位。
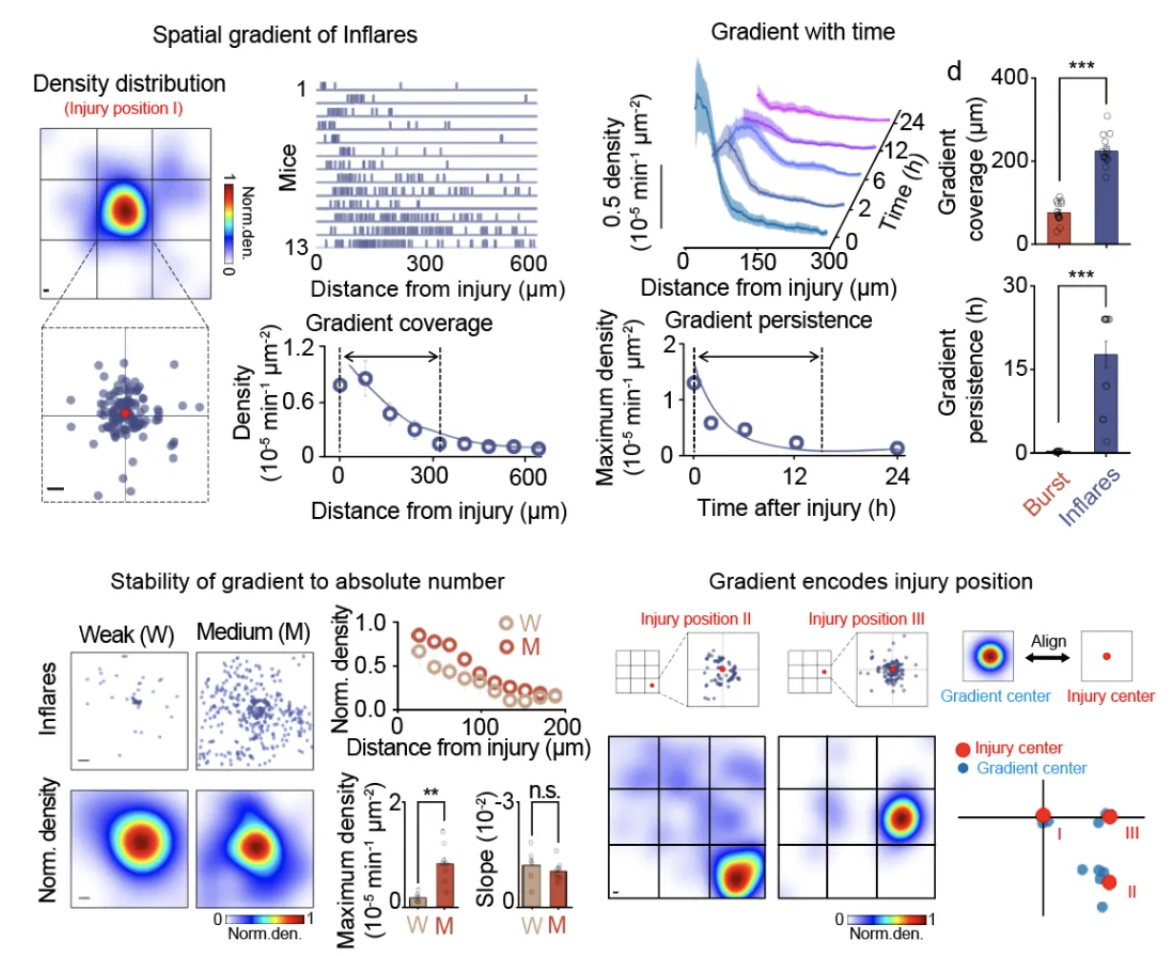
图三 Inflare通过在空间上的概率密度编码损伤位置信息
Inflare以星形胶质细胞钙依赖的方式通过pannexin 1通道释放
Inflare高度特异的时空性质暗示了其为主动释放的过程,为了进一步确认Inflare并非传统认为的细胞死亡造成的ATP泄露,研究者在成像区域注射可标记死亡细胞的染料碘化丙錠,并观测到激光损伤引发的Inflare并不伴随明显的碘化丙錠标记,而损伤中心死亡的细胞可被清晰标记。为了探索释放Inflare的细胞类型,作者结合了特异性药物及遗传学等多种操作,选择性的杀伤或抑制脑内不同细胞类型,并观测在不同处理下激光损伤诱发Inflare的能力。结果表明,当通过注射胶质毒素(L-αAA)或通过胸苷激酶系统清除局部星形胶质细胞后,再次给予激光损伤无法造成明显的Inflare信号升高。相对的,通过表达caspase-3消除局部神经元,或通过化学遗传学(hM4Di + CNO)沉默神经元活性并未影响FLA诱发的Inflare。局部小胶质细胞的清除也未影响激光诱发的Inflare升高。这说明星形胶质细胞是FLA诱发Inflare的最重要细胞来源。为探索Inflare释放的分子机制,作者选择了可能介导ATP释放的潜在蛋白,并在急性脑片体系中检测加入对应分子阻断剂后观测其对Inflare释放的影响。结果发现,多种pannexin 1半通道的阻断剂均有效阻断FLA诱发的Inflare,而对照和其他候选分子的抑制剂则无效。更进一步,作者通过遗传学手段构建了星形胶质细胞特异性Panx1敲除的转基因小鼠,发现星形胶质细胞的pannexin 1通道对于Inflare释放是必须的,而特异性敲除神经元的Panx1则没有影响,支持了星形胶质细胞作为释放细胞来源。对应的,在星形胶质细胞中过表达Panx1可显著增加损伤诱发的Inflare数目。该结果表明星形胶质细胞的pannexin1半通道开放介导了损伤后主动的ATP释放。
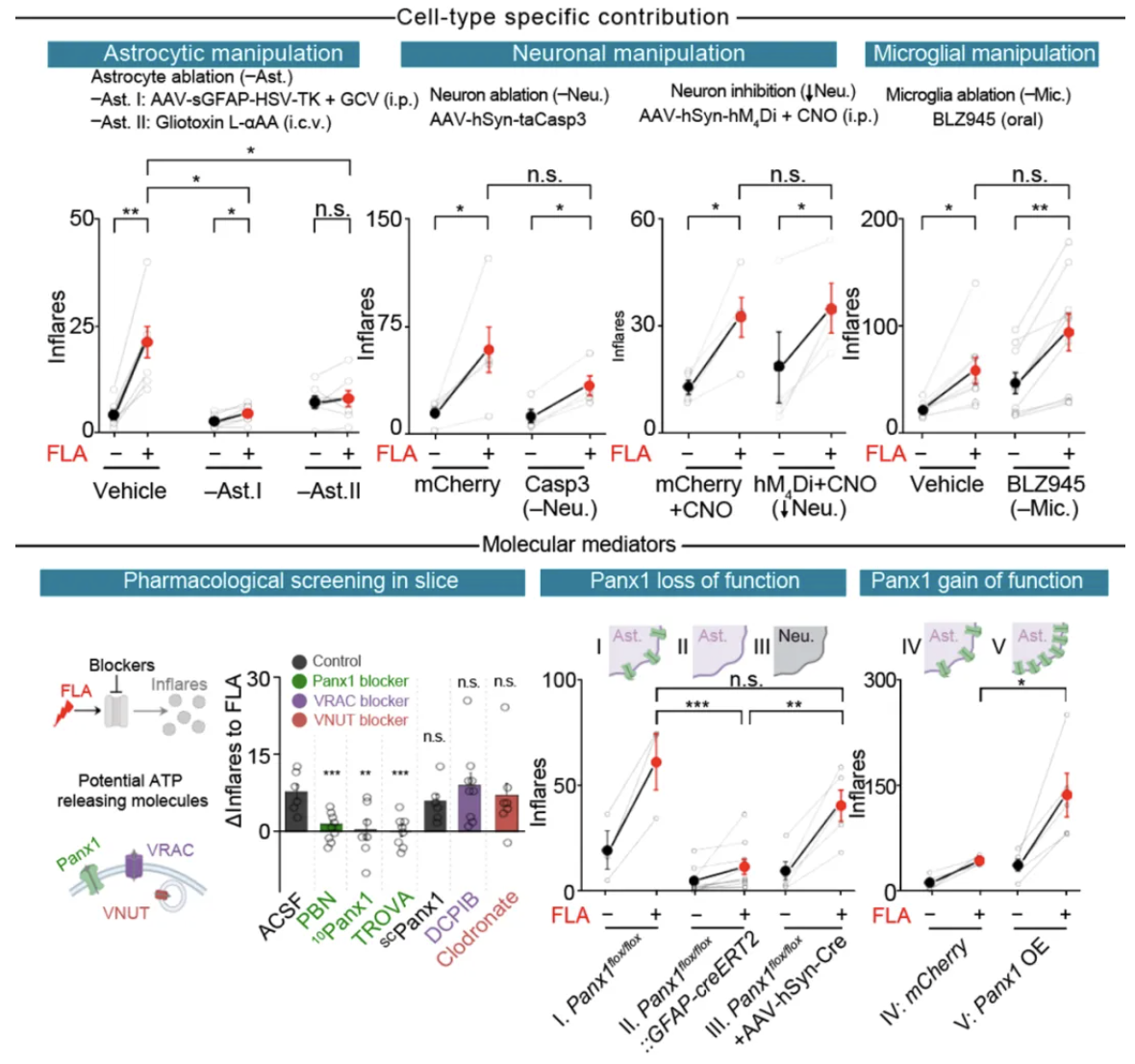
图四 Inflare为星形胶质细胞以钙依赖的方式通过pannexin 1通道释放
小胶质细胞通过解码Inflare信息从而感知损伤
Inflare具备编码损伤信息的能力,并在时间和空间上与小胶质细胞响应过程高度相关。然而,小胶质细胞是否能从Inflare编码的损伤信息中解码这些信息仍需要进一步的实验证明。研究者通过在同样激光损伤背景下,敲除星形胶质细胞Panx1(cKO)以下调损伤编码,或过表达Panx1上调编码,研究后续小胶质细胞应答是否跟随Inflare的编码信息。Panx1条件性敲除小鼠中,小胶质细胞响应损伤的能力被强烈抑制,而在Panx1过表达鼠中该过程则得到了增强。这种小胶质细胞迁移能力与Inflare之间相匹配,而非与原初损伤之间的定量关系说明小胶质细胞具有解码Inflare信息的能力,并且Inflare编码的损伤信息是小胶质细胞感知原初损伤的主要来源。
相似的,研究者们接下来测试了改变Inflare信号编码是否可以影响损伤结果。以局部细胞凋亡作为损伤结果的指标,研究者们发现在星形胶质细胞Panx1敲除小鼠中,FLA诱导的细胞凋亡大大减轻。相反,通过Panx1过表达增强Inflare加剧了FLA后的细胞凋亡。该结果与上述小胶质响应一致,进一步说明损伤结果与Inflare高度相关,其与损伤信息的匹配则依赖正确的Inflare信息编码和呈递。
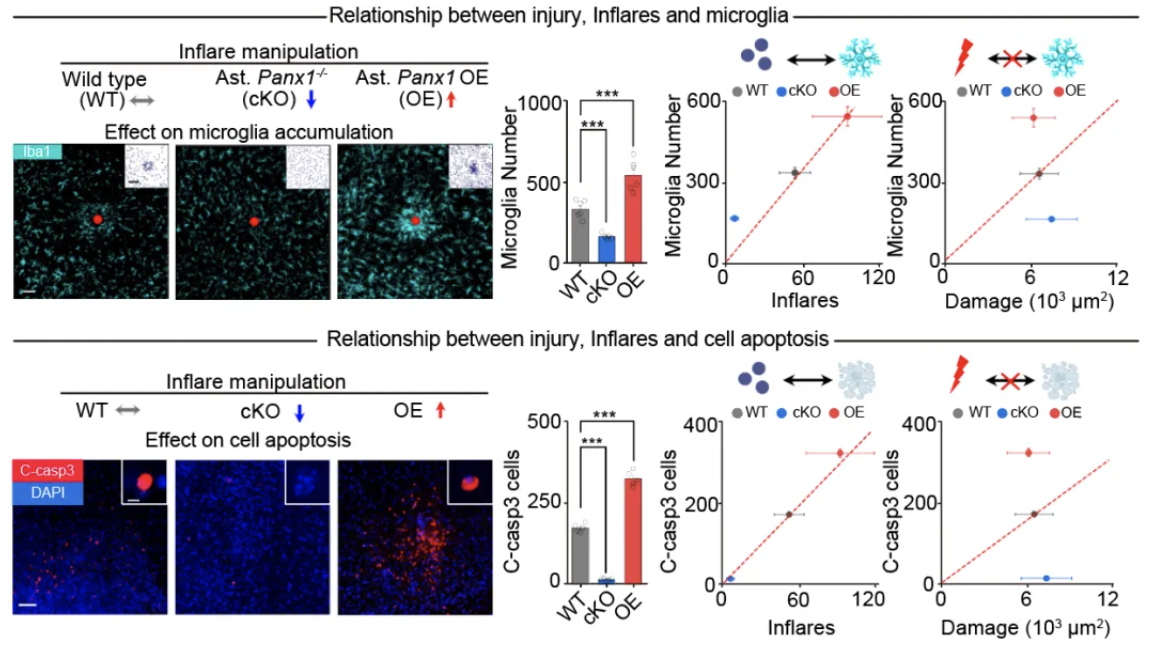
图五 Inflare的信息编码介导损伤和小胶质细胞响应之间的匹配
抑制卒中过程中的Inflare风暴有助于行为康复
为了确定Inflare是否广泛存在于人类疾病相关的多种脑损伤过程中,研究者们应用小鼠大脑动脉闭塞(MCAO)作为卒中(中风)的动物模型,观测其不同时段脑内ATP的动态变化。令人惊奇的是,在卒中的不同阶段Inflare释放体现出特异的变化,其并非随着损伤时间延长而逐渐增高,表明内源损伤编码可能具有更加复杂的调节过程。仅进行假手术的小鼠(Sham)或表达ATP1.0-mut的小鼠在卒中过程中未观测到Inflare的显著上升,而星形胶质细胞Panx1敲除或阻断剂丙磺舒(probenecid,PBN)注射的小鼠中Inflare也显著降低,表明此时的Inflare具有同样的分子机理。在血液再灌注12小时后,研究者们观测到了皮层Inflare的强烈爆发,其相比激光损伤模型中的频率有超过10倍的提升,暗示此时的内源损伤应答很可能处于过度异常的状态,可能伴随着过度损伤反应并引起次发损伤。通过注射丙磺舒抑制Inflare后,发现小鼠由卒中造成的大脑梗死区域显著减少,且在愈后表现出较低的神经功能异常评分和更强的运动和平衡能力。综上所述,该结果表明内源Inflare介导的正确损伤信息编码和呈递对于损伤应答具有重要意义,而其异常很可能作为诱因导致损伤相关疾病的发生和发展。
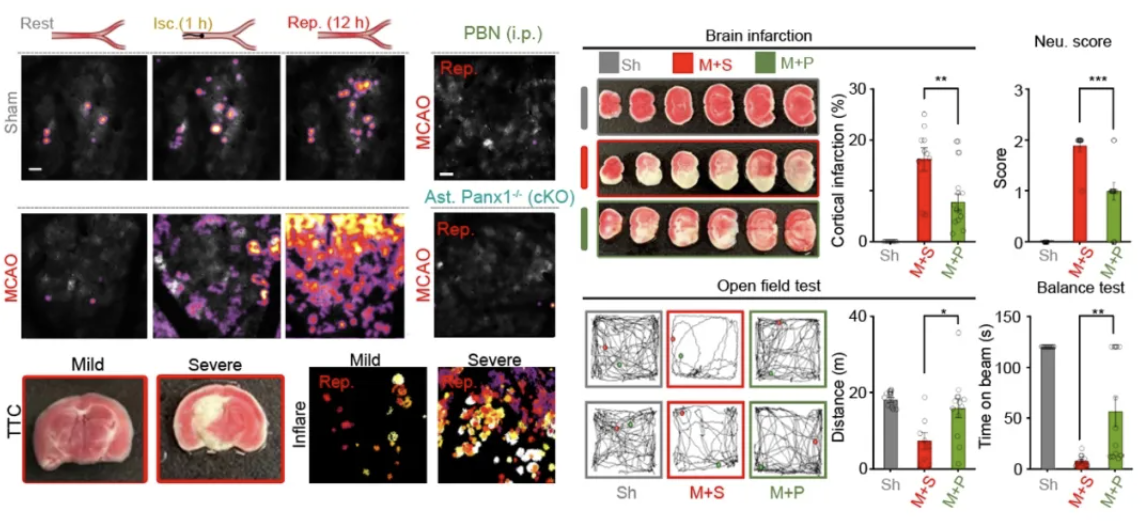
图六 小鼠卒中模型中Inflare的过度应答及其阻断对卒中康复的效果
总结
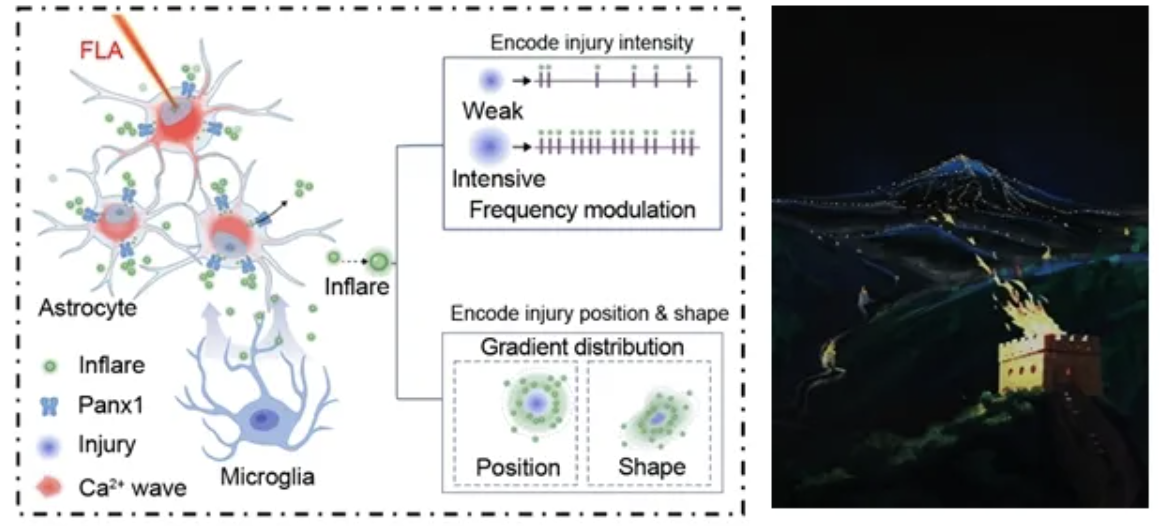
本工作揭示了在内源性损伤中,ATP分子不仅可作为细胞破碎后被动泄露的死亡信号,还可由损伤附近的星形胶质细胞以Inflare的模式主动释放,并以其时空特异性的频率分布,在多维信号空间中对损伤信息进行准确且全面的编码和呈递。脑内应答的小胶质细胞可解码Inflare传递的损伤信息,并基于其指导而进行相应程度的损伤修复及应答。该过程可形象比喻为长城上应对外敌而点燃的烽火台,其中传递信号的烽火就如Inflare一般可长距离高效的指示方向。相应的,异常的胶质细胞互作或其内部信号的改变均有可能造成损伤信号传递的失常,正如长城中未及时点燃烽火,或是烽火戏诸侯(在无外敌的情况下点燃烽火)均会造成错误的应答和严重后果。该信号在疾病模型中的存在及其重要功能提示靶向Inflare的检测和干预有望作为后续损伤疾病的诊断及治疗的新思路。
作者信息
该研究工作由北京脑科学与类脑研究所井淼实验室完成。北京脑科学与类脑研究所科研助理陈阅、博士研究生栾朋伟、副研究员刘娟为该研究论文的共同第一作者,研究员井淼为通讯作者。已毕业硕士生韦叶兰在分子机制探索中做出重要贡献。博士研究生王晨雨和武瑞在相关的分子克隆和质谱检测中做出了重要贡献。论文合作者包括中国科学院遗传与发育生物学研究所的武照伐博士。本工作得到了科技部国家重点研发计划项目“政府间科技创新合作项目”,科技部STI2030重大项目,北京市新星计划及北京市博士后科学基金的大力支持。

参考文献
1. Ghajar, J. Traumatic brain injury. Lancet 356, 923-929 (2000). https://doi.org:10.1016/S0140-6736(00)02689-1
2. Feigin, V. L., Barker-Collo, S., Krishnamurthi, R., Theadom, A. & Starkey, N. Epidemiology of ischaemic stroke and traumatic brain injury. Best Pract Res Clin Anaesthesiol 24, 485-494 (2010). https://doi.org:10.1016/j.bpa.2010.10.006
3. Wang, X. et al. P2X7 receptor inhibition improves recovery after spinal cord injury. Nat Med 10, 821-827 (2004). https://doi.org:10.1038/nm1082
4. Davalos, D. et al. ATP mediates rapid microglial response to local brain injury in vivo. Nat Neurosci 8, 752-758 (2005). https://doi.org:10.1038/nn1472
5. Meyrat, A. & von Ballmoos, C. ATP synthesis at physiological nucleotide concentrations. Sci Rep 9, 3070 (2019). https://doi.org:10.1038/s41598-019-38564-0
6. Rock, K. L. & Kono, H. The inflammatory response to cell death. Annu Rev Pathol 3, 99-126 (2008). https://doi.org:10.1146/annurev.pathmechdis.3.121806.151456
7. Wu, Z. et al. A sensitive GRAB sensor for detecting extracellular ATP in vitro and in vivo. Neuron 110, 770-782 e775 (2022). https://doi.org:10.1016/j.neuron.2021.11.027
8. Wang, Y. et al. Accurate quantification of astrocyte and neurotransmitter fluorescence dynamics for single-cell and population-level physiology. Nat Neurosci 22, 1936-1944 (2019). https://doi.org:10.1038/s41593-019-0492-2
论文链接



