Cell & Bioscience:北京脑中心合作研究员董磊团队发现Smurf1介导p62液滴形成来增强自噬和Nrf2活性
近日,北京脑科学与类脑研究中心合作研究员、北京理工大学董磊教授团队在Cell & Bioscience上在线发表了题为“Enhanced liquidity of p62 droplets mediated by Smurf1 links Nrf2 activation and autophagy”的研究论文。该研究发现E3连接酶Smurf1促进p62液滴的形成和物质交换,并以此增强Nrf2激活、促进自噬。这项研究揭示了Smurf1、p62/Nrf2轴在通过LLPS机制确定Nrf2激活和底物清除中的复杂相互作用,为通过靶向Smurf1抑制GB环境适应力提供理论依据。

近日,北京脑科学与类脑研究中心合作研究员董磊团队在Cell & Bioscience上在线发表了题为“Enhanced liquidity of p62 droplets mediated by Smurf1 links Nrf2 activation and autophagy”的研究论文。该研究发现E3连接酶Smurf1促进p62液滴的形成和物质交换,并以此增强Nrf2激活、促进自噬。这项研究揭示了Smurf1、p62/Nrf2轴在通过LLPS机制确定Nrf2激活和底物清除中的复杂相互作用,为通过靶向Smurf1抑制GB环境适应力提供理论依据。
液-液相分离(LLPS,liquid-liquid phase separation)是指关键分子达到阈值浓度时,与其他蛋白质或RNA等浓缩成密闭的液状隔室或溢出的动态过程。细胞内蛋白质和核酸等生物大分子通过LLPS自发转变为液滴(也称为无膜细胞器),通过控制核功能、调节细胞质量控制和组织生化网络,来维持细胞稳态1。液滴的异常调节导致多种神经退行性疾病和肿瘤发生2-6。p62与自噬起始蛋白FIP200相互作用以驱动大尺寸的自噬体形成,然后被自噬降解7。此外,p62缩合物通过与Keap1竞争性结合来干扰Keap1-Nrf2相互作用,导致Nrf2核易位并上调含有HO1等基因的抗氧化反应元件(ARE)的表达8。p62依赖性液-液相分离协同着聚集体形成与自噬降解来维持细胞内质量控制系统9。然而,调控p62参与LLPS的因素仍不清楚。
在本研究中,作者根据文献中所述的E3连接酶Smurf1是选择性自噬的新介质,推断Smurf1可能与自噬接头蛋白p62存在联系。研究人员发现在应激状态下Smurf1增加选择性自噬接头蛋白p62聚集体的数量和大小。而且这些p62聚集体具有液滴特性,能与周围环境进行分子交换。且Smurf1+p62+双阳性液滴的分子交换能力较p62+单阳性液滴强。进一步研究显示Smurf1对p62相分离的这种促进作用增强Nrf2激活(图1)。
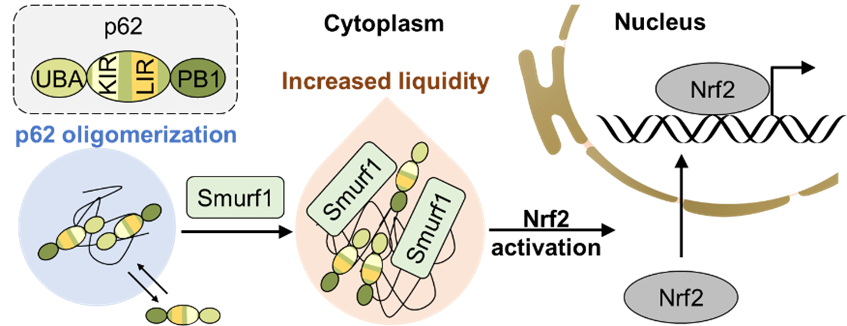
图1 Smurf1过表达增加了p62液滴的形成和物质交换。p62液滴的增加促进了Nrf2核输入。
随后的机制探索实验证明,Smurf1以WW结构域和泛素链接酶活性依赖方式结合p62并促进p62与泛素结合,进而促进p62相分离发生。p62蛋白被证明与自噬接头蛋白NBR1、OPTN和NDP52协同作用10-12。团队发现过表达Smurf1特异性上调p62、NBR1蛋白水平及共定位。团队发现Nrf2是Smurf1和NBR1响应氧化反应的转录因子。应激诱导的Smurf1在Keap1-Nrf2氧化应激反应途径的激活过程中与p62和NBR1协作促进p62液滴的形成以及Nrf2的完全激活。Smurf1还通过p62与LC3结合促进液滴的自噬形成和降解。
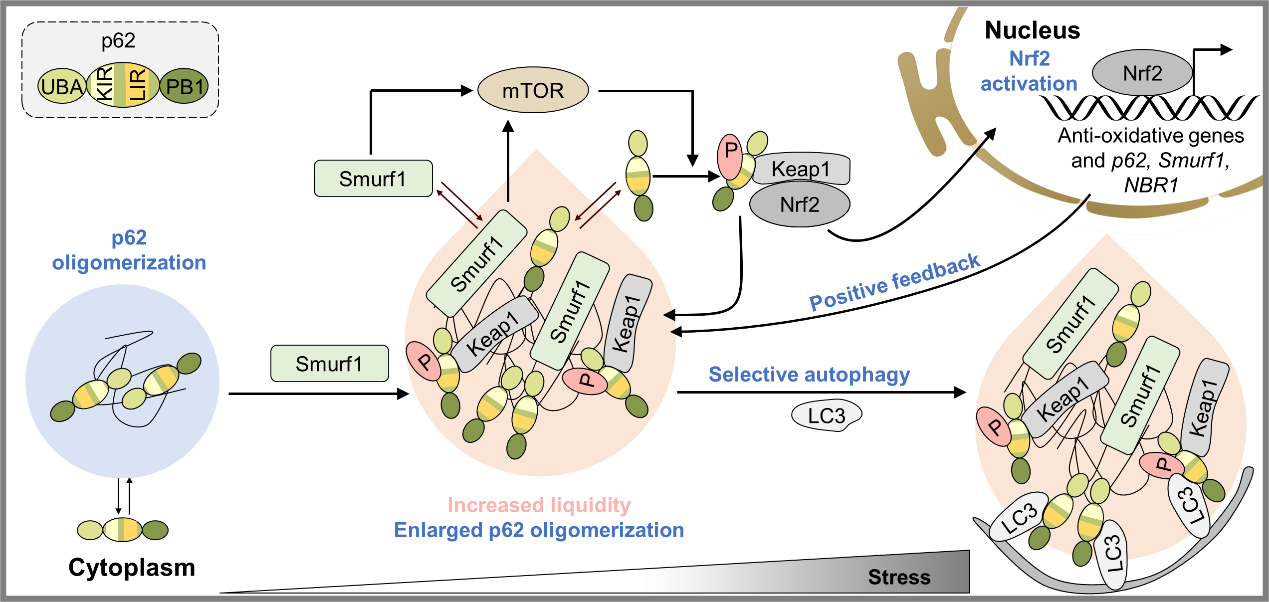
图2 应激导致Smurf1蛋白水平上调,促进p62液滴的形成和物质交换。Smurf1通过激活mTORC1信号通路促进p62的S349位点磷酸化,进而增强p62与Keap1的竞争性结合,诱导Nrf2核易位、促进抗应激蛋白的转录。Nrf2的激活也增加Smurf1、p62和NBR1的mRNA水平,进一步促进p62液滴的形成和扩大。
综上所述,该研究发现Smurf1诱导p62液滴形成和物质交换以激活Nrf2来响应蛋白毒性或氧化应激。激活的Nrf2增加了p62、Smurf1和NBR1的转录,并进一步促进p62液滴的形成和降解。该研究暗示肿瘤细胞中过表达的Smurf1通过激活Nrf2信号通路保护它们免受应激损伤。它还为Smurf1通过LLPS机制参与p62依赖性选择性自噬提供了一种新机制。该研究同时发现Smurf1与p62相互作用并促进p62的泛素化,因此Smurf1是否以及如何直接调节p62以增强p62液滴的形成值得进一步探索。另外,S349磷酸化参与p62与FIP200的相互作用以启动选择性自噬并将液滴转运到溶酶体中7,13。Smurf1是否以p62的S349磷酸化依赖性方式激活选择性自噬需要进一步探索。此外,本研究发现Smurf1的过表达也伴随着p62的S403位点强磷酸化。但Smurf1过表达影响p62磷酸化相关激酶仍需进一步研究确认。
相关信息
北京脑科学与类脑研究中心合作研究员、北京理工大学教授董磊为通讯作者,副教授夏琴和博士生李杨为共同第一作者。
该研究得到了国家自然科学基金(U21A20200和81870123)、北京市自然科学基金(Z190018)、北京理工学院青年学者研究基金项目(XSQD-202110002)、北京脑科学与类脑研究中心科研合作项目(2021-NKX-XM-06)和中国国家青年科学家科学基金(81902545)的资助。
董磊教授与北京脑中心赵瑚实验室合作,开展脑胶质瘤GBM透明化三维影像构建与关键肿瘤分子的三维空间表达与功能分析项目研究,将利用脑肿瘤类器官模型寻找影响肿瘤的关键分子,目前脑机制解析工作在持续推进中,后续成果也会很快产出。
原文地址
https://cellandbioscience.biomedcentral.com/articles/10.1186/s13578-023-00978-9
参考文献
1. So, C., Cheng, S. & Schuh, M. Phase Separation during Germline Development. Trends in Cell Biology 31, 254-268, doi:https://doi.org/10.1016/j.tcb.2020.12.004 (2021).
2. Petronilho, E. C. et al. Phase separation of p53 precedes aggregation and is affected by oncogenic mutations and ligands. Chemical science 12, 7334-7349, doi:10.1039/d1sc01739j (2021).
3. Lu, Y. et al. Phase separation of TAZ compartmentalizes the transcription machinery to promote gene expression. Nat Cell Biol 22, 453-464, doi:10.1038/s41556-020-0485-0 (2020).
4. Tulpule, A. et al. Kinase-mediated RAS signaling via membraneless cytoplasmic protein granules. Cell 184, 2649-2664.e2618, doi:10.1016/j.cell.2021.03.031 (2021).
5. Zhu, G. et al. Phase Separation of Disease-Associated SHP2 Mutants Underlies MAPK Hyperactivation. Cell 183, 490-502 e418, doi:10.1016/j.cell.2020.09.002 (2020).
6. Shi, Q. et al. SPOP mutations promote p62/SQSTM1-dependent autophagy and Nrf2 activation in prostate cancer. Cell Death Differ, doi:10.1038/s41418-021-00913-w (2022).
7. Kageyama, S. et al. p62/SQSTM1-droplet serves as a platform for autophagosome formation and anti-oxidative stress response. Nat Commun 12, 16, doi:10.1038/s41467-020-20185-1 (2021).
8. Jena, K. K. et al. TRIM16 controls assembly and degradation of protein aggregates by modulating the p62-NRF2 axis and autophagy. Embo j 37, doi:10.15252/embj.201798358 (2018).
9. Pohl, C. & Dikic, I. Cellular quality control by the ubiquitin-proteasome system and autophagy. Science 366, 818-822, doi:10.1126/science.aax3769 (2019).
10. Kirkin, V., Lamark, T., Johansen, T. & Dikic, I. NBR1 cooperates with p62 in selective autophagy of ubiquitinated targets. Autophagy 5, 732-733, doi:10.4161/auto.5.5.8566 (2009).
11. Zhang, R. et al. The selective autophagy receptors Optineurin and p62 are both required for zebrafish host resistance to mycobacterial infection. PLoS Pathog 15, e1007329, doi:10.1371/journal.ppat.1007329 (2019).
12. Cemma, M., Kim, P. K. & Brumell, J. H. The ubiquitin-binding adaptor proteins p62/SQSTM1 and NDP52 are recruited independently to bacteria-associated microdomains to target Salmonella to the autophagy pathway. Autophagy 7, 341-345, doi:10.4161/auto.7.3.14046 (2011).
13. Turco, E. et al. FIP200 Claw Domain Binding to p62 Promotes Autophagosome Formation at Ubiquitin Condensates. Mol Cell 74, 330-346.e311, doi:10.1016/j.molcel.2019.01.035 (2019).



