北京脑所陈坚实验室揭示垂体腺瘤治疗新思路:靶向异常剪接位点的ASO核酸治疗 | Theranostics
垂体神经内分泌肿瘤(PitNET)是第二常见的中枢神经系统肿瘤,占所有原发性脑肿瘤的15%。临床上,PitNET的年发病率约为每百万人40例。大约48%的PitNET是大腺瘤(>10 mm),可因占位效应导致视野缺损、头痛或垂体功能减退。PitNET不同亚型之间存在异质性、不同的免疫微环境和临床复发率。PIT1谱系肿瘤约占所有PitNET的40%。药物治疗包括针对泌乳素型PitNET的多巴胺D2受体激动剂和针对生长激素型PitNET的生长抑素类似物或生长激素受体拮抗剂;然而,由于肿瘤耐药性,30-70%的患者最终需要手术干预。肿瘤体积过大或靠近颅底关键结构,尤其是颈内动脉和视神经,是术后复发的独立预测因素。
近日,北京脑科学与类脑研究所陈坚团队与首都医科大学天坛医院贾旺团队的研究人员合作在 Theranostics 上发表文章 "Splicing factor FUS facilitates the progression of PIT1-lineage PitNETs by upregulating MDM2"。研究阐明了FUS蛋白作为PitNET剪接因子的关键功能,使用反义寡核苷酸ASO靶向其介导的MDM2相关的剪接机制可以恢复抑癌蛋白p53表达水平,从而抑制肿瘤的进展。这一发现为PIT1谱系PitNET的临床治疗提供了一种潜在的新颖策略。

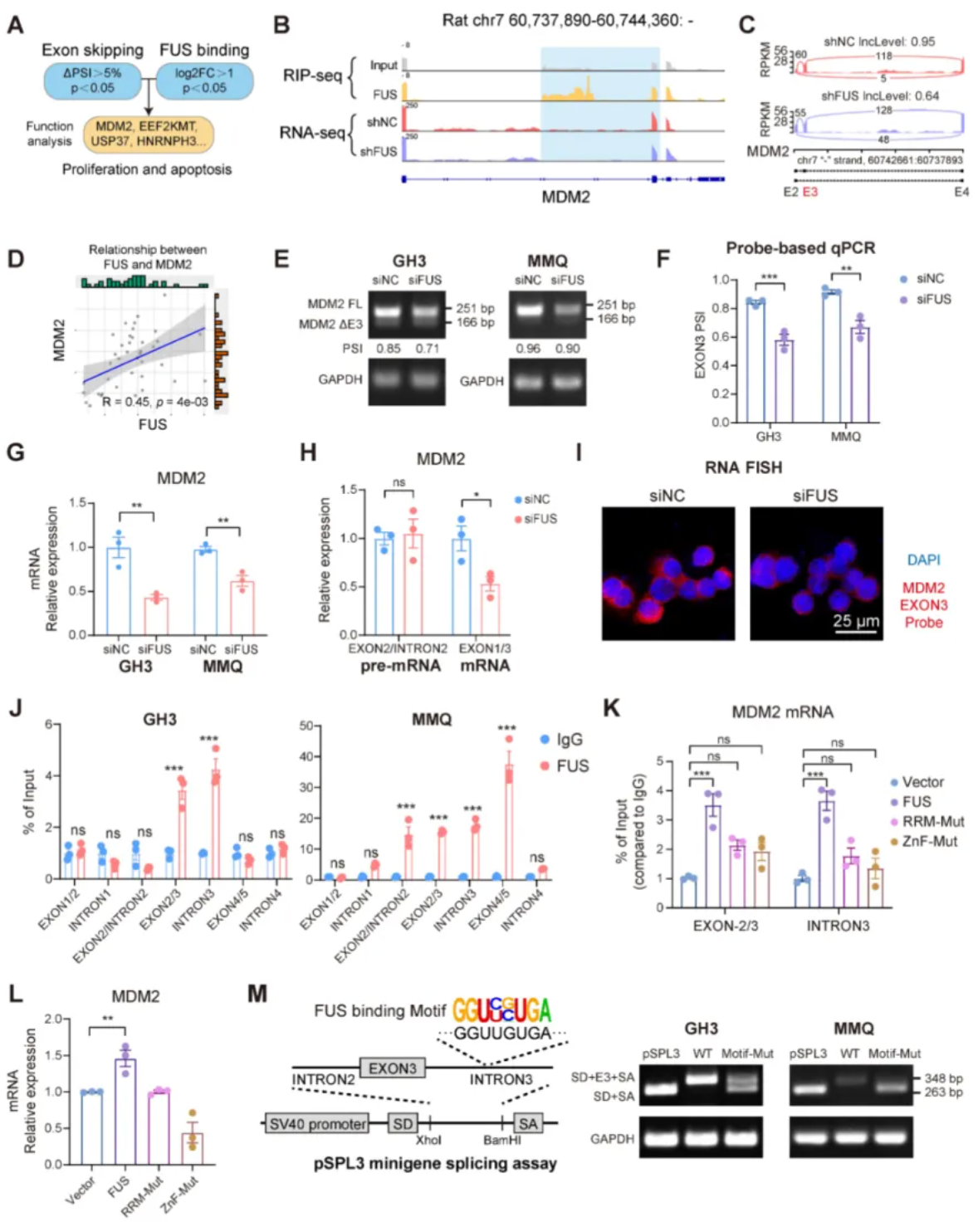
通过对课题组前期建立的垂体瘤样本库和正常垂体样本进行测序,对剪接因子蛋白进行蛋白表达和功能筛选,聚焦到FUS剪接因子的异常功能。敲减FUS蛋白后发现RNA-seq鉴定的差异表达基因与p53通路相关,例如细胞凋亡、DNA修复和细胞周期调节,以及垂体激素分泌相关通路。为了探究FUS作用机制,进行了针对FUS蛋白的RIP-seq,从可变剪接分析结果和FUS结合底物的交集中分析所有候选基因。IGV可视化显示候选基因MDM2外显子和内含子区域内都有FUS蛋白结合,同时FUS的敲低促进了MDM2基因中外显子3的跳跃。设计RIP-qPCR中前体mRNA的不同区域的PCR引物,均检测到FUS与前体mRNA结合。先前研究表明ZnF和RRM结构域介导FUS蛋白的剪接调节。为了分析剪接活性是否依赖于直接的FUS-RNA相互作用,我们创建了具有RRM突变或ZnF的功能域突变体。RRM和ZnF结构域内的点突变阻碍了FUS与MDM2前mRNA的结合,同时消除了其对MDM2表达的影响。随后进行pSPL3 mini基因剪接验证,将MDM2的外显子3和侧翼内含子克隆并插入到pSPL3 mini基因中,在组成型剪接供体(SD)和剪接受体(SA)位点之间具有FUS结合位点的野生型(WT)或突变体(Motif-Mut)序列。FUS结合序列的突变破坏了MDM2外显子3的剪接。综上确定MDM2是FUS的剪接底物,并证明FUS通过外显子3的剪接过程来促进MDM2蛋白的表达。
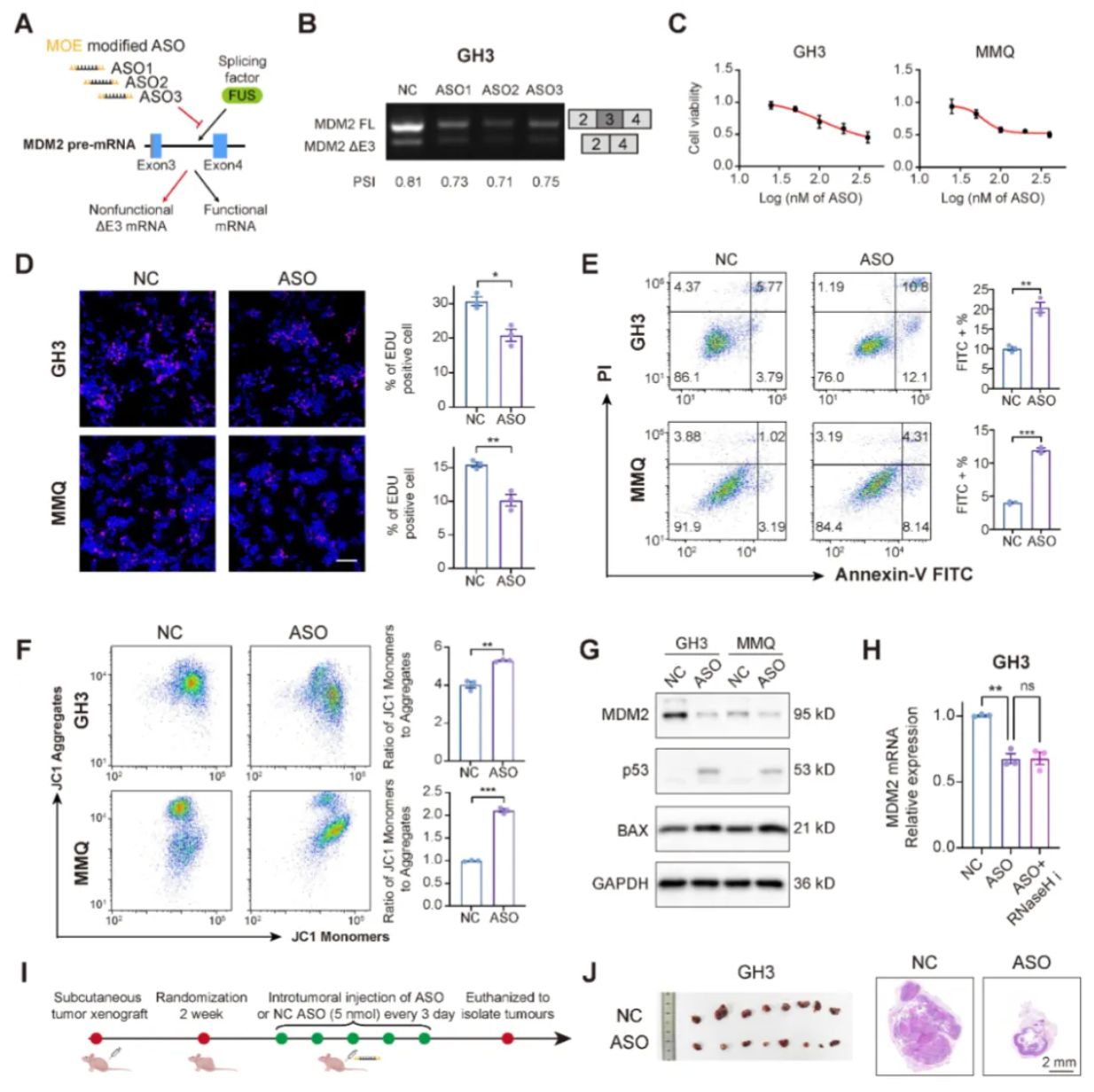
p53蛋白是MDM2的下游经典抑癌蛋白,在垂体瘤中突变率较低,能否抑制MDM2的异常剪接以恢复肿瘤中p53活性,是课题的下一个目标。ASO能够与前体mRNA结合,促进剪接转换或RNA降解,这些机制已被作为与剪接异常相关的各种疾病的治疗策略。为了评估ASO在PitNET中的治疗潜力,设计了针对MDM2前体mRNA的ASO,并结合2'-O-甲氧基乙基(MOE)修饰以增加其稳定性。ASO成功诱导MDM2外显子3的剪接跳跃,以100 nM浓度处理持续48小时可有效抑制PitNET细胞的增殖,促进凋亡并减弱线粒体活性。ASO处理降低了MDM2蛋白水平,进而降低了p53表达并提高了其促凋亡下游蛋白BAX的表达。在皮下异种移植模型中,通过瘤内注射施脂质体包被的ASO,显著减少了肿瘤体积。
进一步地,我们在PitNET原代细胞中证实,特异性ASO可通过调控MDM2剪接异构体抑制蛋白表达,进而发挥抗肿瘤增殖活性。鉴于核酸治疗药物(尤其是ASO)在其他疾病的临床转化成功,针对实体瘤开发的ASO疗法有望突破现有治疗瓶颈,为患者带来新的治疗选择。
论文信息
北京脑科学与类脑研究所访问医师王旭为本文第一作者,北京脑科学与类脑研究所陈坚研究员、北京天坛医院贾旺教授和管修东副教授为共同通讯作者。该工作得到“天坛-北脑”交流项目的重要支持,以及国家自然科学基金、北京市博士后科研活动经费和北京脑科学与类脑研究所的资助支持。



