成体干细胞从何而来?赵瑚团队首次揭示其“诞生与维持”的关键机制|Nature Communications
成体间充质干细胞(Mesenchymal Stem Cells, MSC)是维持组织稳态、参与损伤修复与再生的细胞群体,但其在发育过程中何时、以何种机制形成,仍不清楚。阐明成体干细胞的发育起源及其稳定维持机制,是理解组织再生与干细胞治疗的基础前提。

2025年11月27日,北京脑科学与类脑研究所赵瑚实验室、四川大学华西口腔医院靖军军博士以及北京大学口腔医院杨瑞莉博士合作在Nature Communications发表题为“Autocrine ECM molecules establish MSC quiescence during incisor development by disrupting WNT ligand trafficking process”的研究论文,系统回答了“成体干细胞从何而来、如何稳定存在”的科学问题。牙齿间充质来源于颅神经嵴细胞(cranial neural crest cells),这是一类从神经管迁出的多能性细胞,能分化为颅颌面骨、牙齿、脂肪、神经节神经元、胶质细胞及黑色素细胞等多种组织。研究团队以小鼠切牙这一“终生生长”的模型为切入口,围绕MSCs的发育起源、分子标志与调控机制,展开多层次解析。
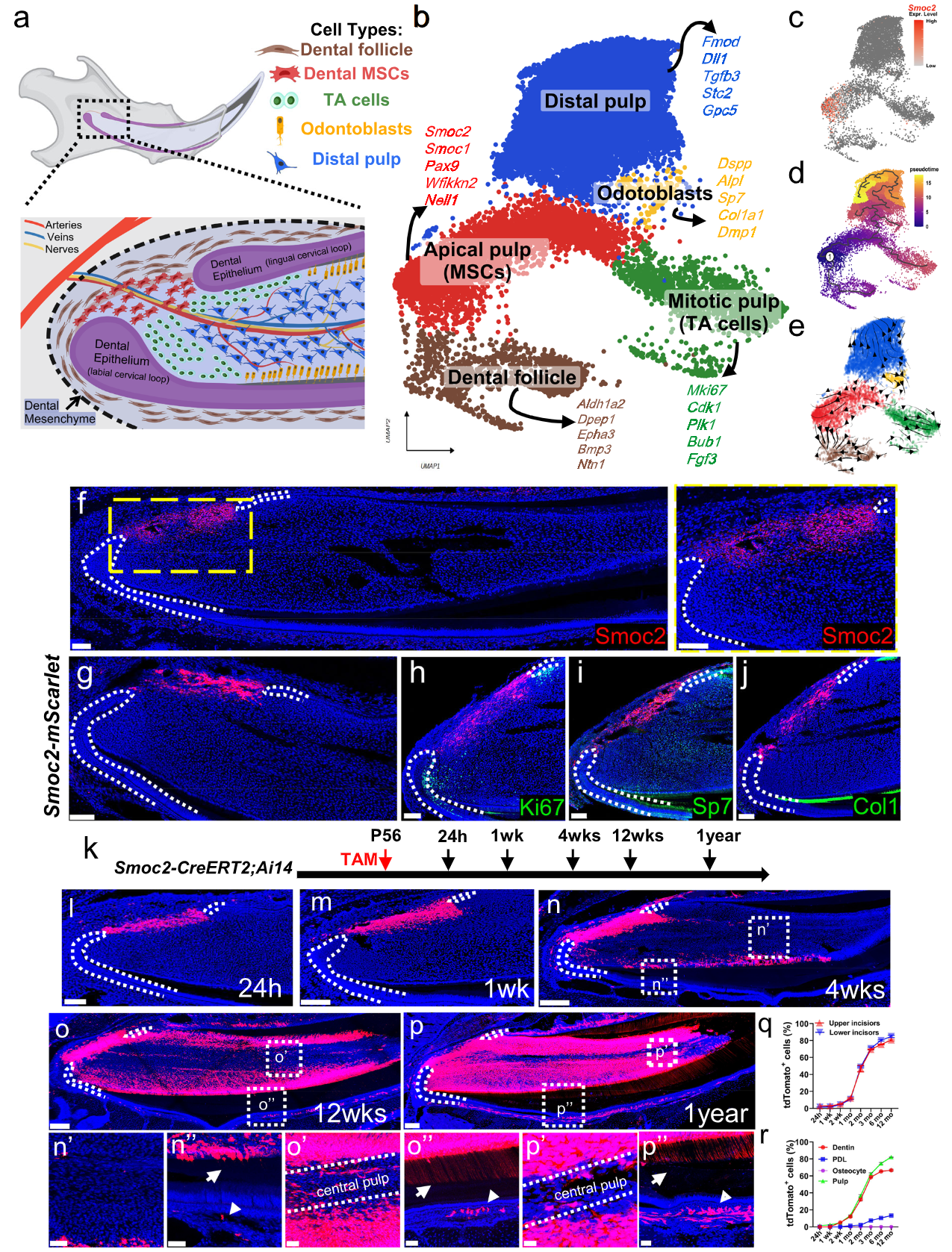
图1 Smoc2+ 细胞是成年小鼠切牙牙髓MSCs
研究团队通过分析小鼠切牙单细胞转录组、构建转基因小鼠并进行谱系示踪、条件敲除与体外实验等多种技术,系统探究了牙髓间充质干细胞从胚胎到成年的完整发育轨迹。研究发现,Smoc2特异性地高表达于切牙牙髓根尖的间充质细胞,谱系示踪实验证实该群体是维持牙齿间充质持续生长的干细胞来源。该发现为精准标记成体切牙MSCs群体提供了可靠分子依据。
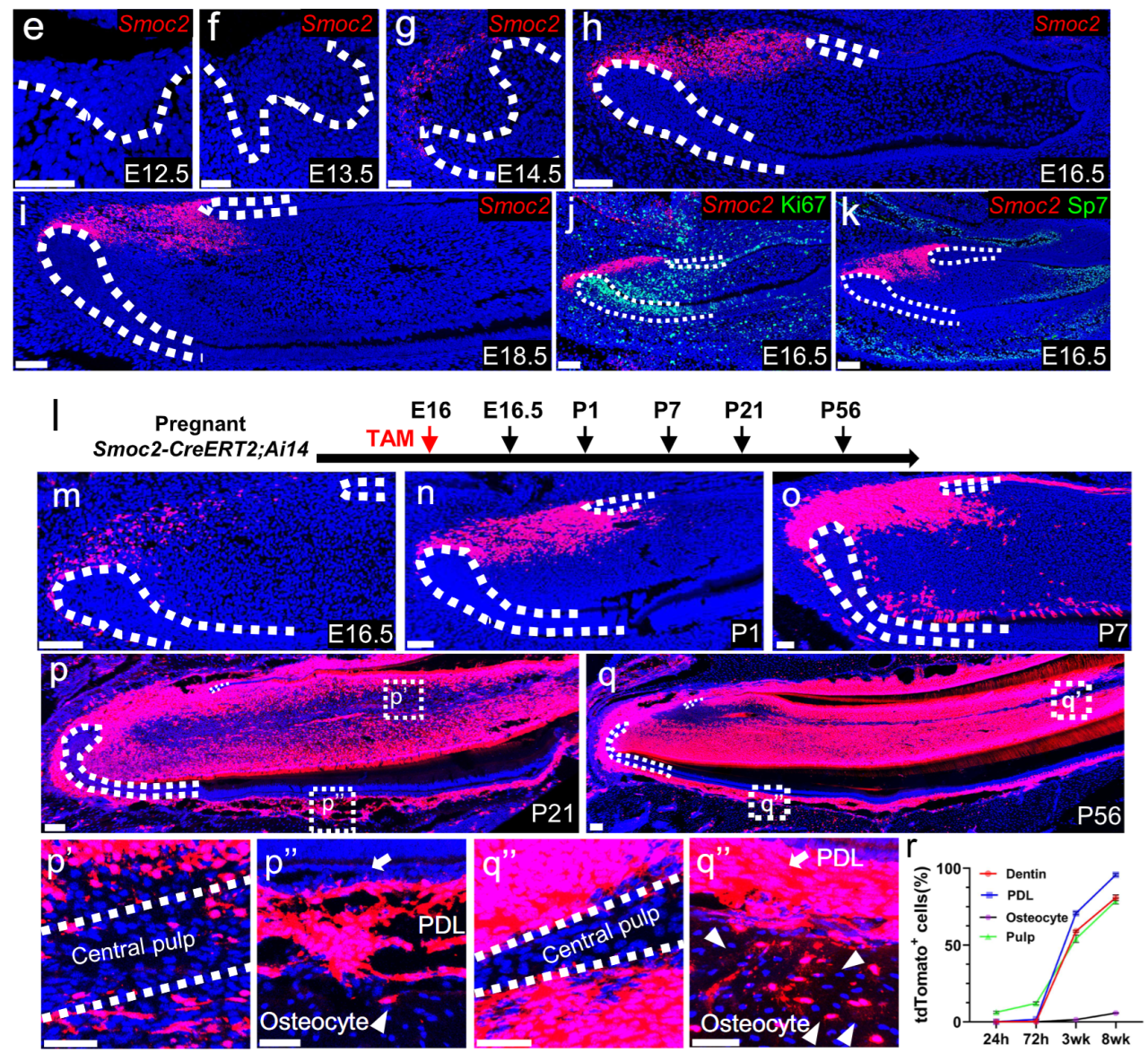
图2 E16.5小鼠切牙Smoc2+细胞是MSCs
研究发现,Smoc2+ 细胞群体的静息态与切牙间充质的层级结构是在小鼠胚胎期E14.5至E16.5之间建立。这将干细胞的内在状态转变与外在的组织结构形成联系起来,为全面理解干细胞身份建立提供了系统性的框架。
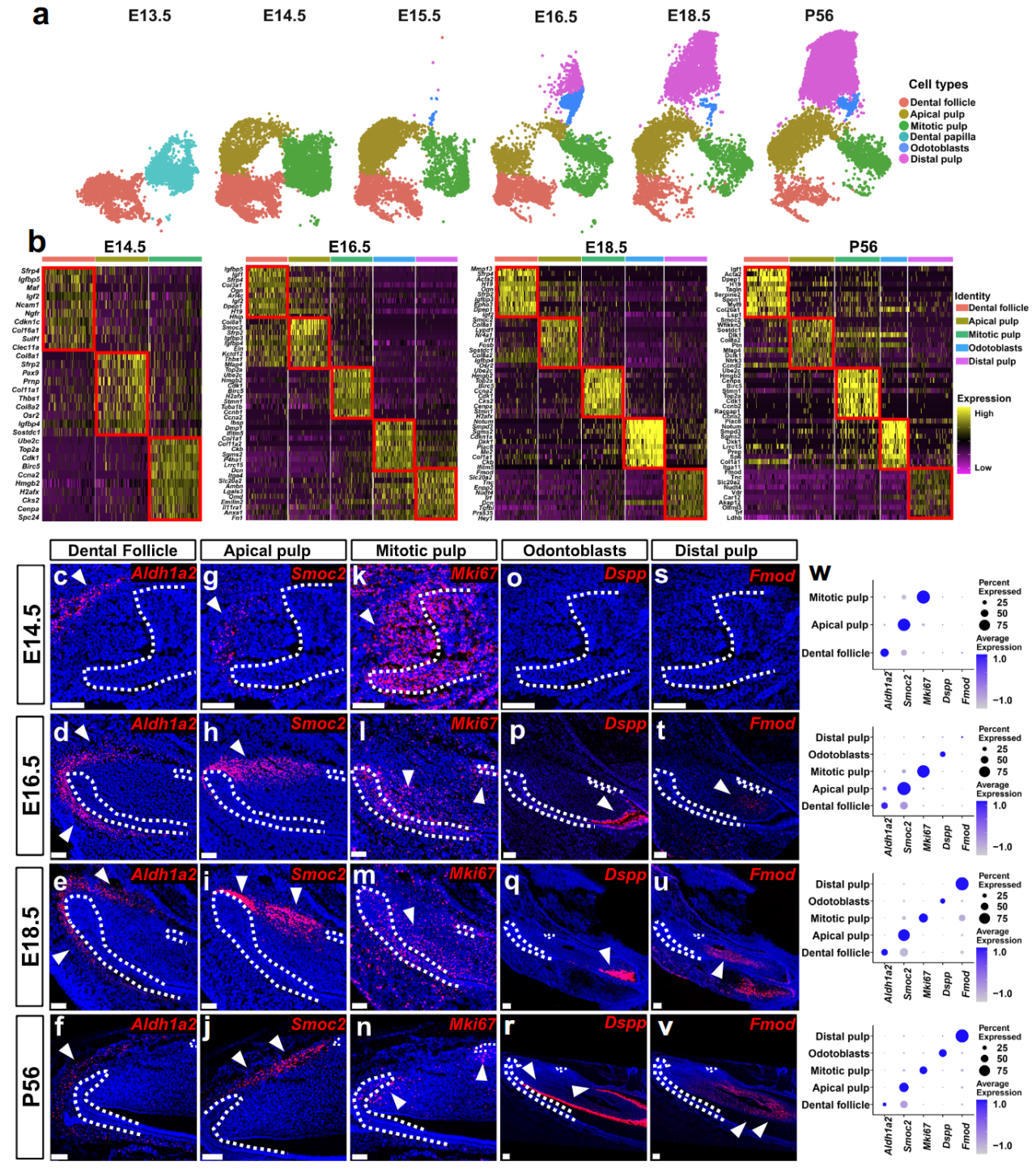
图3 E切牙间充质谱系层级的建立在胚胎期14.5天至16.5天期间形成。
SMOC1/2是SPARC/osteonectin家族的细胞外基质蛋白(ECM)。在缺失SMOC1/2的小鼠牙髓中,Wnt 配体异常进入干细胞区,导致 MSC 失去静息状态并过早激活,最终引发干细胞池耗竭和牙齿发育异常。SMOC1/2可通过竞争性结合Wnt配体的运输载体Glypican,进而抑制了Wnt信号的激活。该机制精确限制Wnt信号空间分布,使其仅在远离干细胞的区域作用,进而促进细胞增殖与分化。
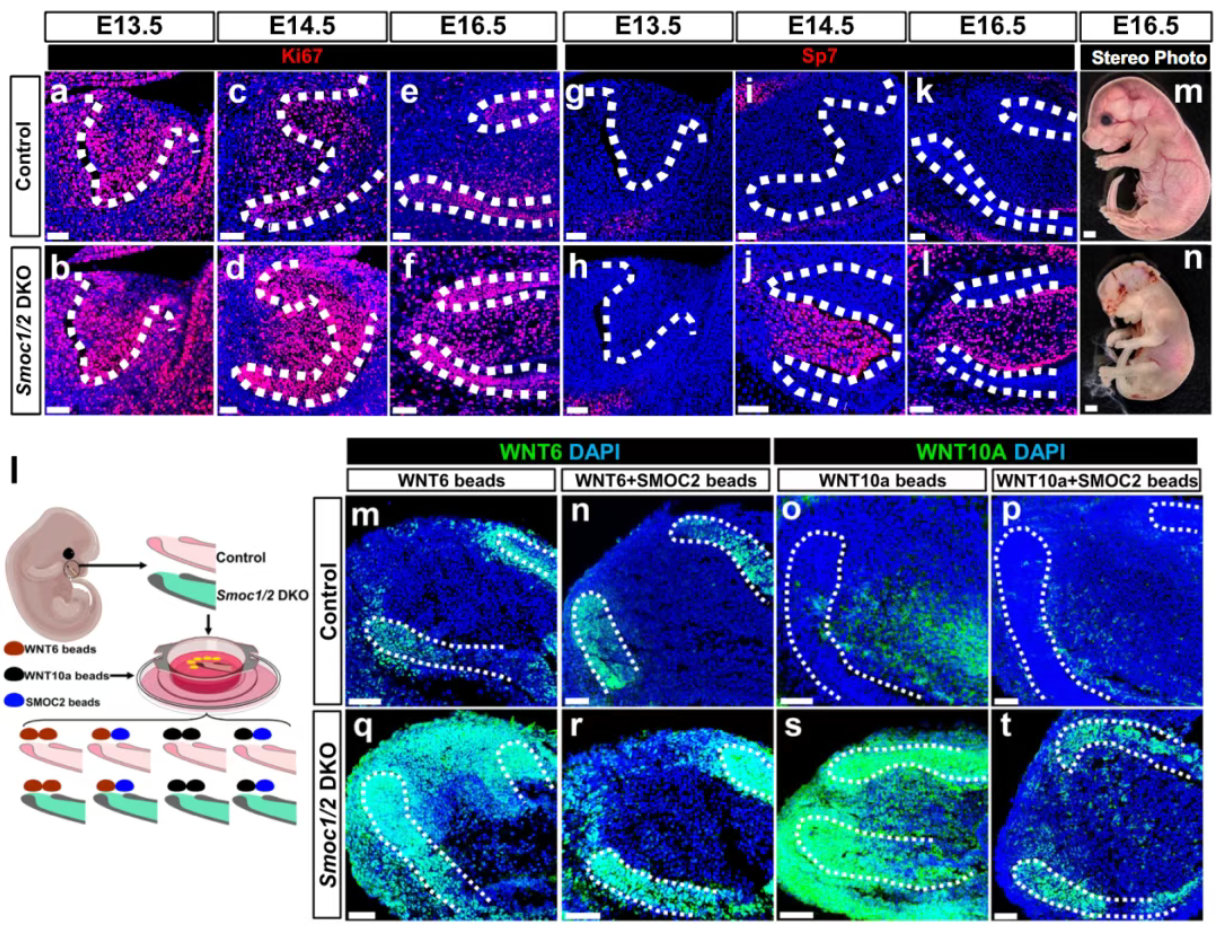
图4 SMOC1/2缺失会导致MSC静息状态丧失和间充质层级结构破坏,SMOC1/2阻止WNT 配体接近间充质干细胞。
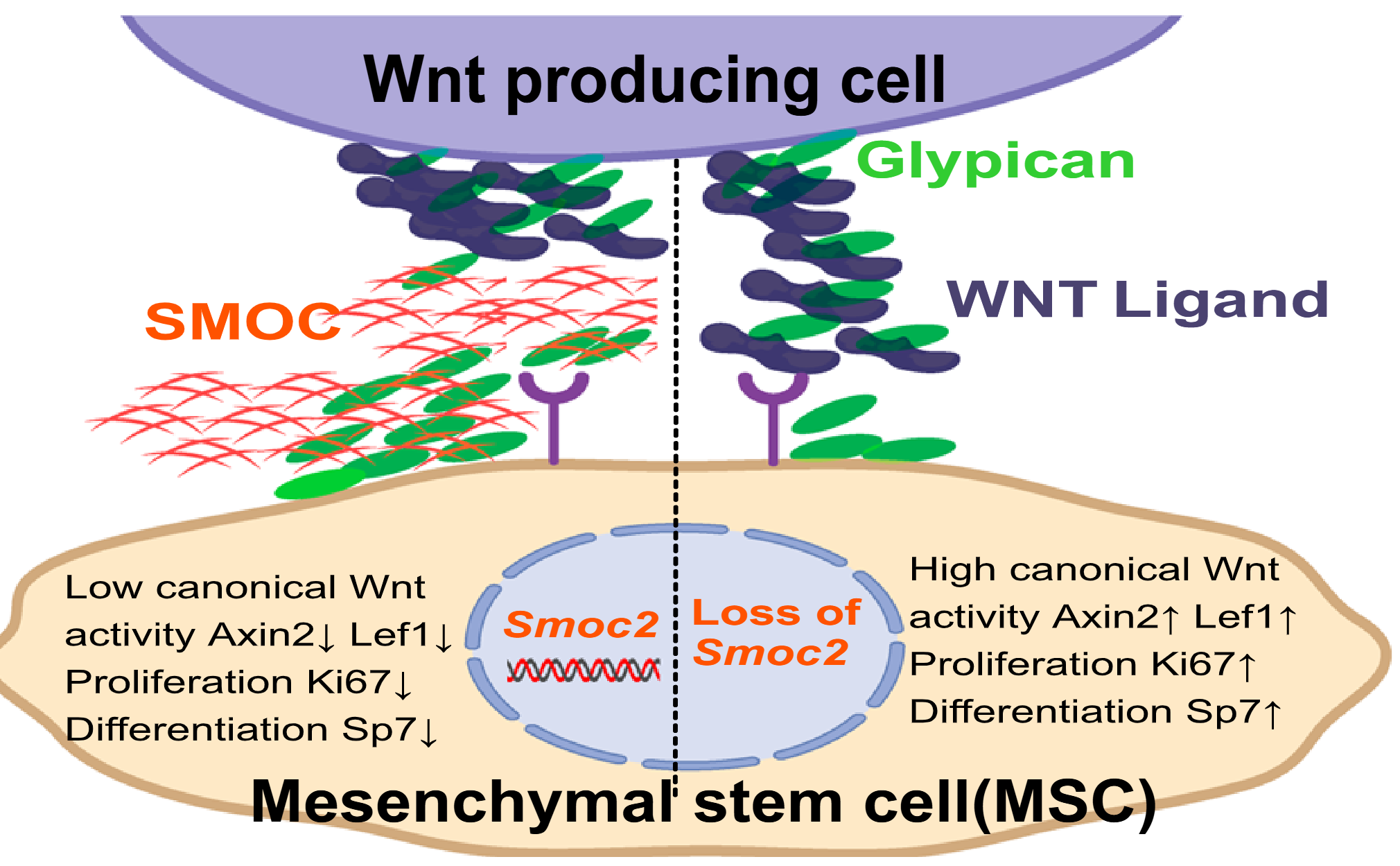
图5 SMOC1/2通过与GPC结合,抑制经典Wnt信号通路的活性
综上所述,该研究揭示细胞外基质并非仅是结构支架,而是参与信号通路空间定位和干细胞命运决定的关键调控节点。在应用层面,这一成果为组织再生、干细胞培养体系优化及组织工程微环境设计提供了关键理论依据,对推动再生医学发展具有重要意义。
论文信息
北京脑科学与类脑研究所赵瑚实验室博士后陈泽希和北京大学口腔医院博士后蔡美莲为该论文的共同第一作者;北京大学口腔医院杨瑞莉博士、四川大学华西口腔医院靖军军博士和北京脑科学与类脑研究所赵瑚博士为本论文共同通讯作者。
原文链接



