北京脑科学与类脑研究所2024年代表性科研成果选编
北京脑科学与类脑研究所成立于2018年3月22日,是北京市政府与中国科学院、北京大学、清华大学、北京师范大学、中国医学科学院、中国中医科学院等单位共建的新型研发机构。宗旨是瞄准世界脑科学前沿和国家在脑科学研究领域的战略急需,通过创新体制机制,整合脑科学领域优势资源,搭建脑科学研究综合性实验和研发平台,汇聚全球顶尖人才和优秀科研团队,开展科技攻关,在脑科学领域产出一批重大原始创新成果,推进国际交流合作,建设成为面向科技前沿的世界一流脑科学研究研发机构。研究所重点聚焦脑认知原理解析、脑重大疾病、神经科学新技术、神经计算与神经编解码等四大研究方向。已建成37个实验室和11个辅助技术中心。2024年6月12日,与中国医学科学院北京协和医学院共建的中国医学科学院北京脑和类脑研究院、北京协和医学院脑和类脑学院正式挂牌。
以下为2024年北京脑所精选的17篇代表性科研成果,包括1篇Nature、3篇Nature Neuroscience、4篇Nature Communications、1篇Neuron等(展示顺序按发表时间排序)。
1. 自主开发新概念透明化技术--TESOS透明化包埋实现单根外周神经全貌重建

赵瑚
北京脑科学与类脑研究所 高级研究员
2024年1月3日,赵瑚实验室在Cell Research发表封面文章“Mapping of individual sensory nerve axons from digits to spinal cord with the transparent embedding solvent system”,报道了基于团队开拓的新型透明化技术--TESOS透明化包埋,在国际上首次实现“从指尖到中枢”单根外周神经全貌重建。
生物医学成像正在由二维走向三维。获取完整的生物组织介观尺度三维结构信息是生命科学基础研究的重要目标。然而,组织的不透明性极大地阻碍了光学成像的深度。其首要原因是光的散射,生物组织中含有水、脂肪、蛋白质、矿物质等多种成分,其不均匀分布会导致光发生强烈的散射,使光无法直接穿过组织。另一方面,机体内的血红蛋白、黑色素等物质可吸收光,限制光线通过。为解决上述两个问题,组织透明化技术由此诞生:一方面,通过脱色技术减少光的吸收,另一方面,利用含有高折射率介质的透明液取代样本中水分和脂质,平衡组织折射率,减少光的散射,从而使组织实现光学透明。
赵瑚团队受牙科临床实践启发,为使大脑样本获得更高的透明度和机械强度,提出并开发了TESOS透明化包埋新技术,该技术是对传统组织透明化及三维成像技术的一种理念革新。其核心概念在于“透明”和“包埋”。“透明”是TESOS与基于超薄切片的大尺度三维成像技术(以fMOST为代表)的最大区别。聚合后的良好透明度保证了成像质量,也使得TESOS技术与包含光片显微镜、共聚焦显微镜等多种成像系统的有机结合成为可能。TESOS包埋形成的有机树脂与其他水性透明化技术中的琼脂糖包埋凝胶截然不同,其良好的机械硬度及切割性能大大提高了操作的稳定性,切削(磨削)后样品变形小,数据拼接及重建具有良好的准确性。这一特性使得TESOS相较于ViSoR2(目前多用于大脑样品处理)有更广泛的适用范围,能够同时适用于中枢及外周的处理与成像。利用该技术,团队挑战了一项高难度任务,对完整成年小鼠实现全身神经均一微米级分辨率的三维成像与重建,这是世界上首次在微米层级看到单个神经元如何与外周连接。
TESOS透明化包埋处理流程清晰,实验试剂易得,兼容AAV标记及免疫荧光染色,在配备有石蜡切片机、共聚焦显微镜的实验室即可实现完整的技术流程,体系灵活性高。TESOS技术必将成为未来生物医学三维成像的有力工具。
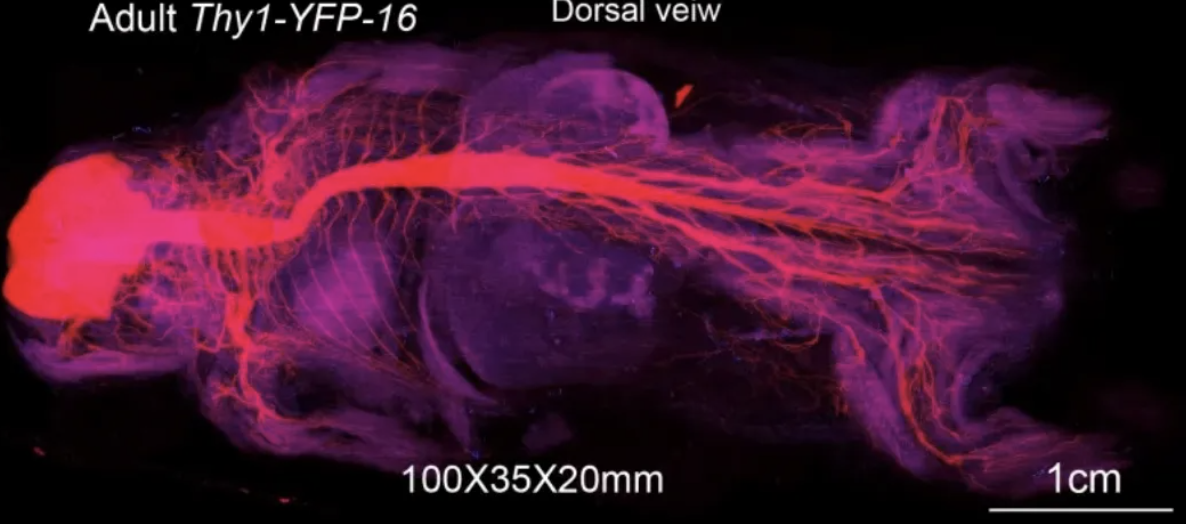
图:TESOS透明化包埋后利用光片显微镜进行成年小鼠全身神经成像
(双通道拍摄,样本总体积100×35×20mm3,总拍摄时长120小时,原始数据量约70TB)
论文链接:
https://www.nature.com/articles/s41422-023-00867-3
2. 开发可重现小脑语言功能局部回路计算机制的类小脑人工智能

Shogo Ohmae
北京脑科学与类脑研究所 研究员
2024年1月31日,Shogo Ohmae实验室在Nature Communications上发表了题为Emergence of syntax and word prediction in an artificial neural circuit of the cerebellum的文章。此研究揭示了小脑复杂的语言认知处理的回路计算机制。
具体来说,右侧小脑外侧部(Crus I/II)参与两项关键功能:预测句子中的下一单词(next-word prediction)和语法处理,尤其是语法结构的处理。为了深入研究小脑在语言处理中的回路计算机制,Ohmae团队开发了一个模仿小脑的人工智能回路(cANN),重现回路计算中的三个要素—回路结构、输入/输出信号和学习机制。就回路结构来说,这是一个三层的RNN网络,通过前馈和反馈路径连接输入层、浦肯野细胞层和输出层,精确反映小脑细胞类型的连接模式并复现小脑的语言功能(图a)。
在预测下个单词的任务中,关于输入/输出信号,小脑可以接收序列单词作为输入信号,然后输出对下个单词的预测。研究结果表明,不仅该回路的输出层获得了预测下个单词 (next-word prediction) 的能力 (图b,红色箭头),并且浦肯野细胞层也自发获得了小脑的另一个语言功能,即语法处理 (图b,蓝色)。 据我们所知,这是第一个与神经科学发现一致的脑模拟人工智能回路,在重现回路计算三个要素的同时复制了复杂的人类特征认知功能。这些结果表明,单一的小脑回路通过预测误差学习获得语言模型,并提取抽象的语言特征,如语法信息。该研究方法和对大脑回路计算细节的阐明可成为显著推进我们对大脑理解的重要工具。
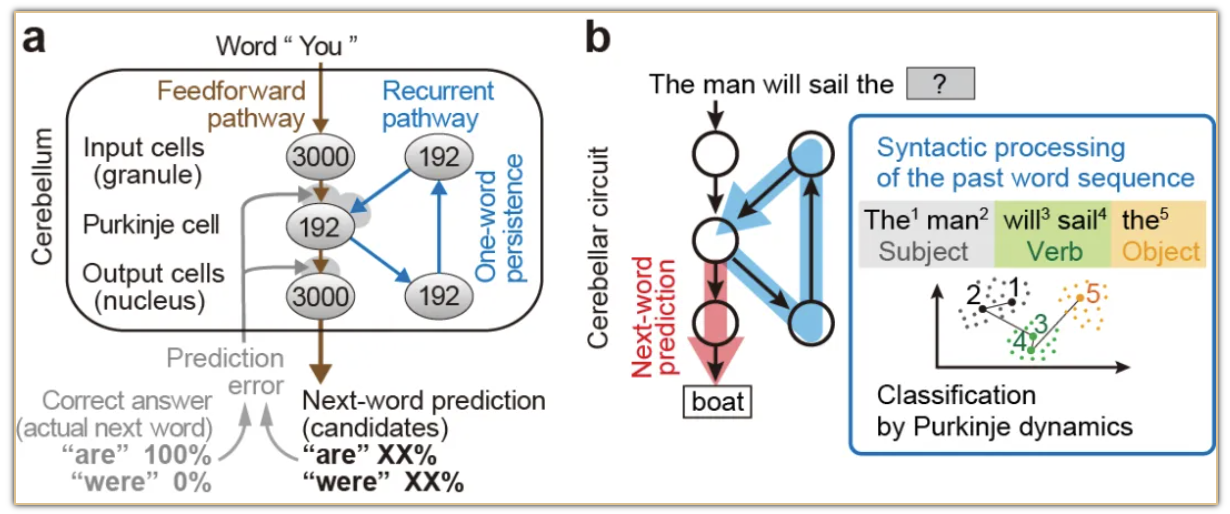
图:a. cANN重建小脑语言功能的局部回路模型(棕色:前馈路径;蓝色:循环路径;灰色箭头:传递预测误差信号以更新浦肯野细胞和输出细胞上的突触权重(灰色阴影))b. cANN提出的两种小脑语言功能回路。
论文链接:
https://www.nature.com/articles/s41467-024-44801-6
3. 合作发现Cdh23基因可变剪接调控毛细胞tip link稳定性

熊巍
北京脑科学与类脑研究所 研究员
2024年2月26日,北京脑科学与类脑研究所熊巍课题组与山东大学生命科学学院徐志刚课题组、上海交通大学陆青课题组合作在《美国科学院院刊》(PNAS)发表了题为“Disruption of Cdh23 exon 68 splicing leads to progressive hearing loss in mice by affecting tip-link stability”的研究论文,报道了Cdh23基因可变剪接调控毛细胞顶连接稳定性。
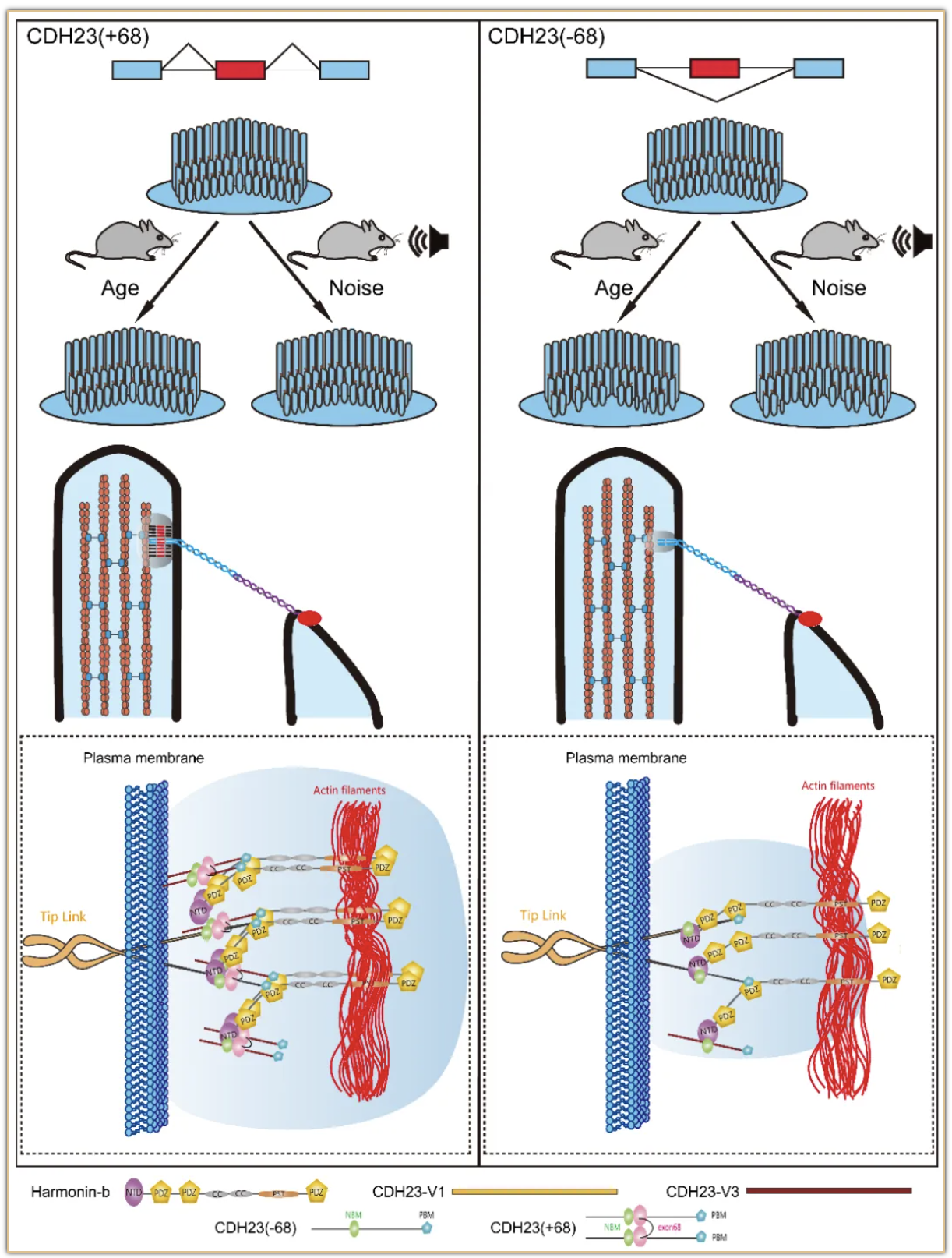
研究显示在大量听觉转导相关基因存在可变剪接的情况,顶连接(tip links)的唯二组成成分之一Cdh23基因即存在可变剪接。Cdh23基因编码一个非典型钙粘蛋白,构成顶连接的上端部分,其胞内段与富含PDZ域的harmonin等蛋白形成蛋白复合体。Cdh23基因含有69个外显子,其中68号外显子受到内耳特异性可变剪接的调控,产生Cdh23(+68)和Cdh23(-68)两种剪接本,其中Cdh23(+68)只在内耳中被检测到。68号外显子长105个碱基对,编码位于胞内段的35个氨基酸,其组织特异性可变剪接的调控机制及生理功能一直以来都不十分清楚。研究团队的前期工作显示Cdh23基因可变剪接受到RNA结合蛋白RBM24等的调控,Rbm24基因敲除小鼠耳蜗中Cdh23基因68号外显子可变剪接几乎完全被阻断,表明RBM24是这一可变剪接过程的重要调控因子。
在本论文中,研究人员对这一可变剪接的生理功能及背后的分子机制进行了深入探讨。研究人员发现敲除Cdh23基因68号外显子并不影响新生鼠毛细胞顶连接的形成和功能。进一步研究显示,随着年龄的增长,成年基因敲除小鼠顶连接数量减少,伴随较低排静纤毛的丢失。与此相应,敲除小鼠表现出渐进性耳聋。此外,敲除小鼠对噪声也更加敏感。这些结果表明Cdh23基因68号外显子可变剪接不影响顶连接形成,但影响其稳定性。最后,研究人员发现与CDH23(-68)相比,CDH23(+68)胞内段更容易自身多聚化,也更容易与harmonin形成复合体,从而影响了顶连接的稳定性。
该研究厘清了CDH23的可变剪切所对应的蛋白功能以及参与听觉转导的个性化机制,为其他听觉转导相关基因的可变剪切的功能解析提供了参考,也为了解功能基因的可变剪切机制提供线索。
论文链接:
https://doi.org/10.1073/pnas.2309656121
4. 脸识别的人类遗传学:脸盲人中发现MCTP2基因突变

饶毅
北京脑科学与类脑研究所联合所长、特聘研究员
北京大学讲席教授
首都医科大学校长
人脸识别,是高级社会认知、也是高级视觉认知。饶毅团队以经典和现代遗传学为基础,辅以人脑核磁共振成像,先后研究了六千多位被试者,其中几个家系中有一个几十人的大家系(含18位脸盲者)。
2024年3月28日,研究成果在Genetics杂志线上发表,题为“Human genetics of face recognition: discovery of MCTP2 mutations in humans with face blindness (Congenital Prosopagnosia)”。

孙芸、门卫伟、Ingo Kennerknecht、方万、郑厚峰、张文霞、饶毅
脸识别对于视觉认知和社会认知都很重要。虽然脸盲(prosopagnosia或face blindness)已经被发现了七十多年,脸特异反应神经元已被发现近半个世纪,其分子遗传学机理不清楚。在此我们报道用经典遗传学和现代基因组学研究17年的结果。从一个含18位在日常生活脸识别困难的先天脸盲(congenital prosopagnosia, CP)成员的家系,我们在MCTP2基因找到完全共分离的独家突变,它编码脑内表达的一个钙结合的跨膜蛋白。在更多CP家族、以及6589人中筛查到的CP中发现更多MCTP2 的罕见突变。14位MCTP2基因移码突变S80fs 的携带者,与19位非携带者在脸识别有显著差别。包括一个家庭有10位成员的6个家庭,显示S80fs与CP的相关性。功能核磁共振成像发现MCTP2突变的CP对个体脸识别的障碍相关于脑内右侧纺锤体脸识别区域对重复脸的重复压制减低。最早发现脸盲的76年后、第一个脸盲病人发现47年后,我们的结果揭示了MCTP2 突变致CP的基因罹患性。这是第一次发现人类高级视觉社会认知所必需的基因。
论文链接:
https://doi.org/10.1093/genetics/iyae047
5. 合作揭示结构变异编码人脑特异发育的新机制

张力
北京脑科学与类脑研究所 基因组学中心主任
2024年4月5日,北京脑科学与类脑研究所基因组学中心张力团队与北京大学未来技术学院李川昀团队合作在Science Advances杂志发表题为Adaptive Functions of Structural Variants in Human Brain Development的研究论文。
在演化历程中,哪些遗传改变使我们成为独一无二的人类?是否存在人类特有的遗传因子,贡献了人脑特异性发育特征?阐明该问题,对深入理解人类高级智能具有重要科学意义。已有研究表明,基因组结构变异(Structural Variants,缩写为SV)是物种特有性状的重要来源。若能在灵长类物种中系统鉴定SV事件并探究其演化规律,将为解答上述问题提供新视角。然而,目前虽然在灵长类研究领域积累了大量的基因组短片段测序数据,但运用短片段数据鉴定结构变异事件仍存在很高的假阳性,限制了其广泛应用。
本研究开发了新的计算流程,实现了仅根据短片段数据对三类主要结构变异事件的准确鉴定。据此,基于1026只自产和公共的恒河猴全基因组测序数据,建立了完整、准确的恒河猴群体SV图谱,探究了结构变异的特征、分布与演化规律,并提出筛选功能性结构变异事件的新策略。基于该策略,鉴定得到75例人类特有的倒位变异事件并对其进行了功能排序(见图),发现排序最高的事件通过介导人类特异的基因表达改变,编码人脑特异性发育特征。
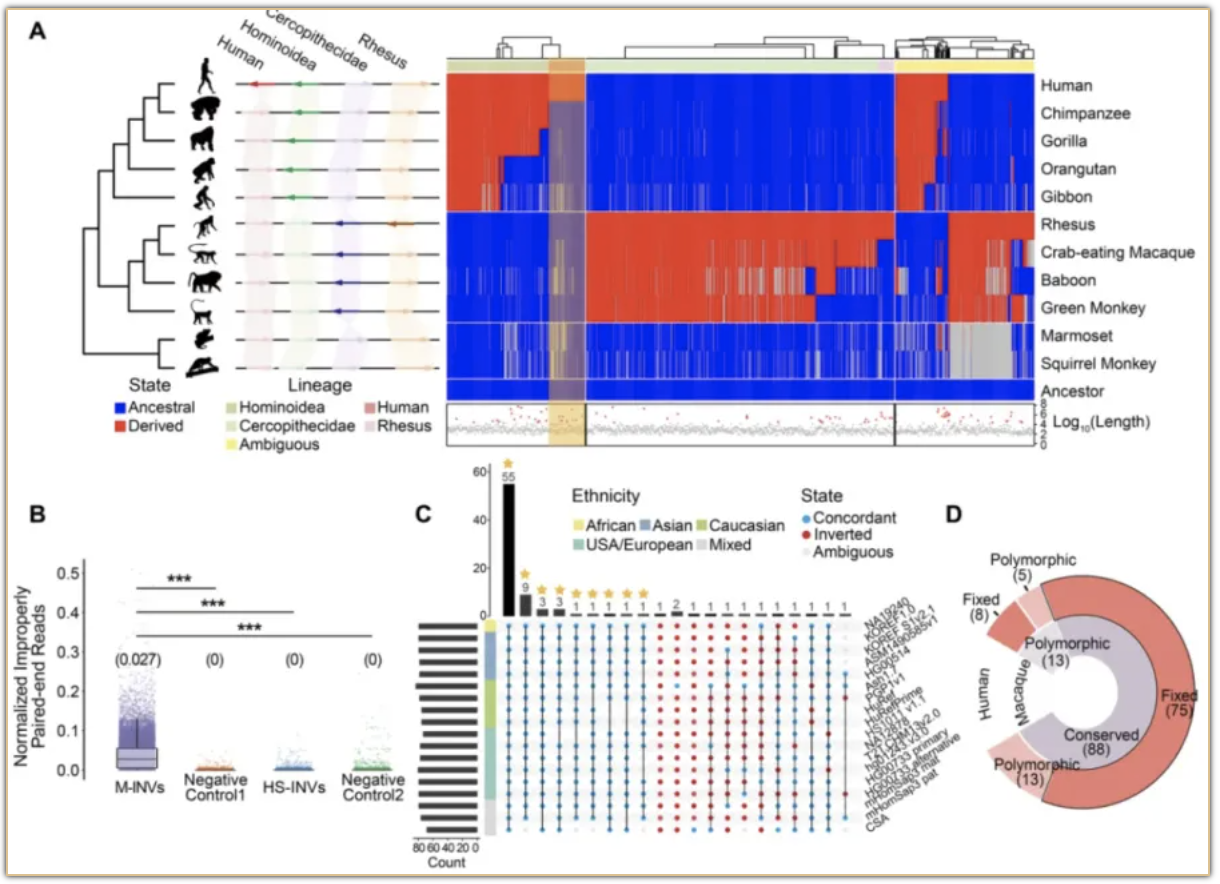
图:人类特异倒位变异图谱
论文链接:
https://www.science.org/doi/10.1126/sciadv.adl4600
6. 发现灵长类运动皮层对序列运动的动态编码机制

崔翯
北京脑科学与类脑研究所 高级研究员
2024年4月11日,崔翯实验室在Nature Communications发表题为Multiplicative Joint Coding in Preparatory Activity for Reaching Sequence in Macaque Motor Cortex的研究长文。
运动皮层长期以来认为是计划和生成运动的核心脑区。大量证据表明运动皮层的神经活动与运动方向、速度、距离和轨迹等多种运动变量相关。然而,这些研究通常采用快速的单元运动,对于包含多个单元的序列运动研究则较少。原则上,一个连续的动作序列由时空上协调的复杂运动单元组成,而不是一系列独立运动单元的简单叠加。然而近期的一项研究(Zimnik & Churchland, Nat Neurosci, 2021)支持了上述的平行编码假说,发现运动皮层在序列运动执行过程中存在两个运动规划过程,而非对整个运动序列的单次运动规划。但是存在两个运动规划过程并不意味着对运动单元编码的独立性,平行编码假说也无法解释序列影响下的线性解码器鲁棒性现象。尽管序列运动对运动皮层神经元活动造成影响的诸多实验结果被报道,其背后的编码机制和作用仍未被探索。
本研究揭示了猕猴运动皮层神经元在序列运动过程中的动态编码机制。对神经元活动模式的回归分析表明,运动皮层在序列运动的全程均编码运动序列信息,在运动准备期以非线性的增益调制编码运动单元之间的互作信息,而在执行阶段以线性叠加方式并行编码两个独立的运动单元。这一结果表明运动皮层对序列运动的编码既非整体也非孤立的,而存在动态变化的互作编码机制。对这一机制的理解,可以帮助我们构建针对复杂运动的解码器和脑机系统。
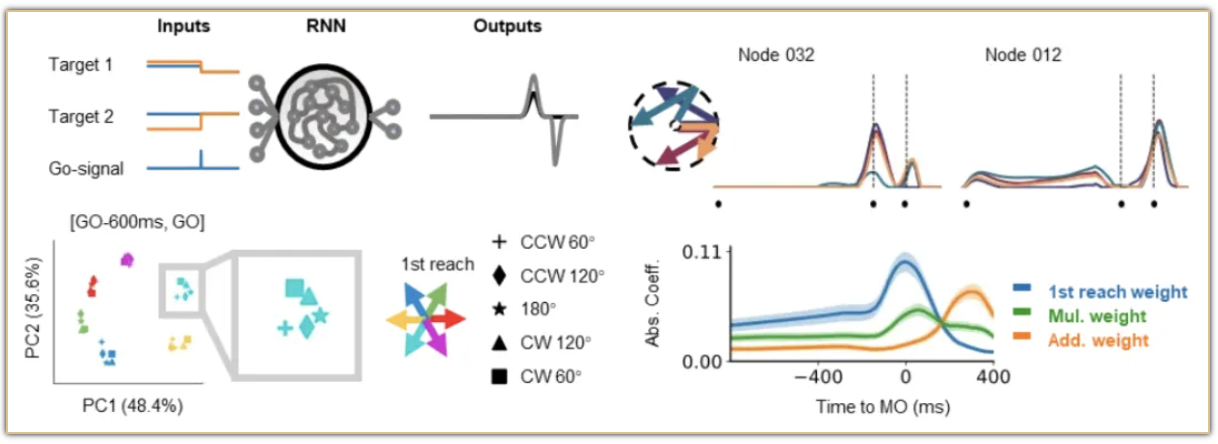
图:循环神经网络模拟序列运动结果
论文链接:
https://www.nature.com/articles/s41467-024-47511-1
7. 合作揭示脑内皮细胞GSDMD的激活是炎症性血脑屏障破坏的关键机制

罗敏敏
北京脑科学与类脑研究所联合所长、特聘研究员
新基石研究员
2024年4月17日,北京脑科学与类脑研究所罗敏敏实验室与北京生命科学研究所邵峰实验室合作在Nature上发表题为Brain endothelial GSDMD activation mediates inflammatory BBB breakdown的研究论文。
血脑屏障是维持中枢神经系统正常功能的重要结构,为脑组织与外周循环系统之间提供了一道天然防线。然而,在病原体感染或系统性炎症的情况下,血脑屏障的功能可能会被破坏。特别是在革兰氏阴性菌感染引起的败血症的情况下,细菌外壁成分脂多糖(也称内毒素或LPS)进入循环系统后,会引发血脑屏障的炎症性破坏,加剧败血症相关脑病的发展。明确革兰氏阴性菌感染如何引起血脑屏障的炎症性破坏具有重要的治疗潜力,但引发这一现象的关键分子及其细胞生物学机制,至今仍不完全明确。
本研究探讨了革兰氏阴性菌感染破坏败血症患者血脑屏障的分子与细胞生物学机制。当发生革兰氏阴性菌感染时,血液循环中的LPS通过LBP-CD14通路被内吞进入脑内皮细胞,并激活胞内的Casp4/11-GSDMD通路。激活的GSDMD在脑内皮细胞上形成孔洞,增加内皮层的通透性,促进中枢神经系统与血液循环之间物质的被动交换。而GSDMD的过度激活会触发脑内皮细胞发生焦亡,进一步导致脑血管的物理破坏。因为这些过程不依赖传统的血脑屏障破坏机制,即紧密连接破坏和转胞吞作用增加,所以GSDMD 孔洞导致的内皮细胞通透性增加以及细胞焦亡共同构成了全新的血脑屏障破坏新机制。这也为未来的血脑屏障破坏相关的神经系统疾病治疗提供了新的理论基础和潜在的治疗靶点。
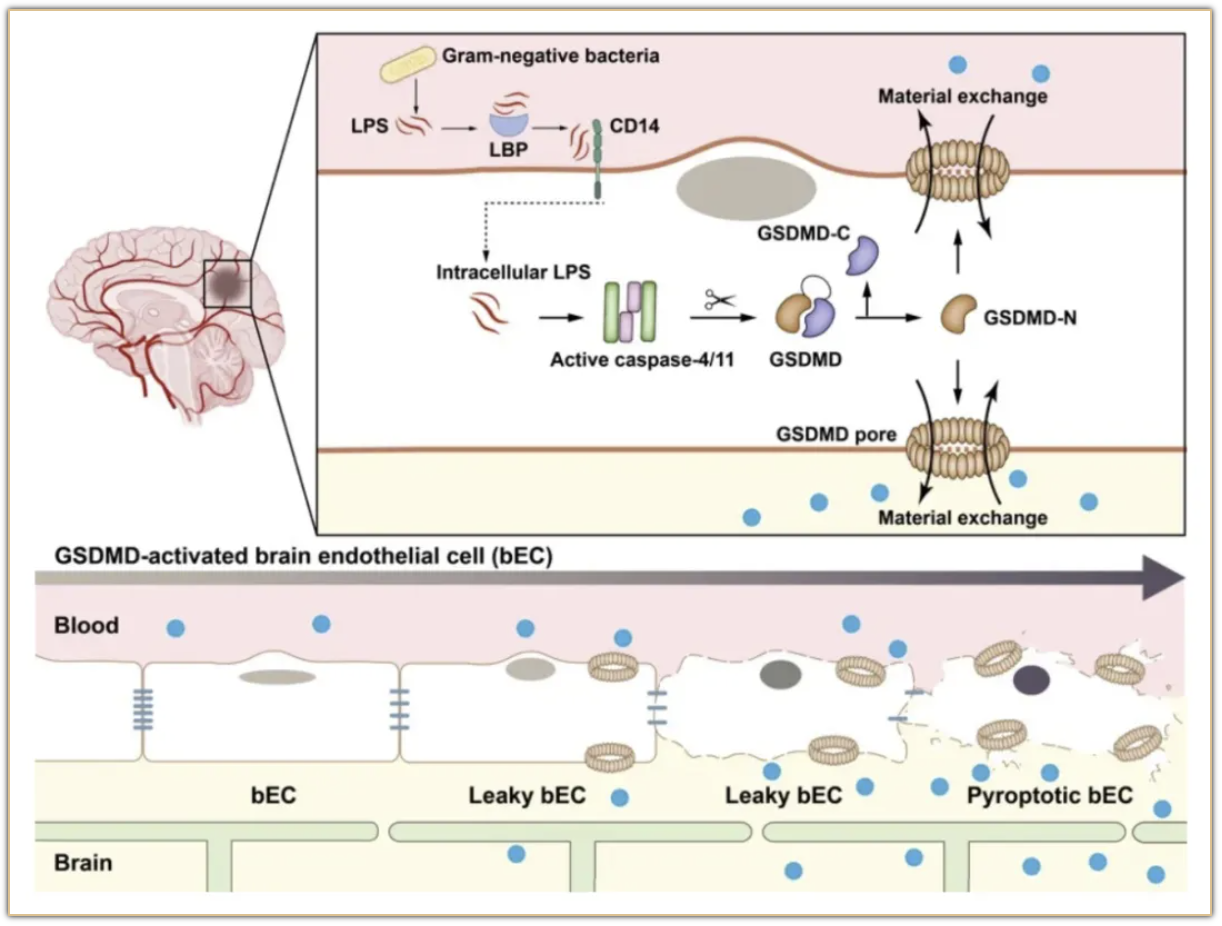
GSDMD破坏血脑屏障模式图
论文链接:
https://www.nature.com/articles/s41586-024-07314-2
8. 开发一种基于基因编辑的脑机接口增强技术

方英
北京脑科学与类脑研究所 资深研究员
2024年5月1日,方英实验室在Advanced Materials在线发表题为“Spatially Precise Genetic Engineering at the Electrode-Tissue Interface”的研究论文。该研究通过构建基于基因工程技术的多功能柔性神经电极,向神经电极周围的脑组织递送基因并对细胞进行特异性的基因编辑,实现了增强型的脑机接口技术。
脑机接口是通过在大脑与外部电子设备之间创建直接的通讯通道,实现人与机器的高带宽信息交换,推动人工智能(AI)与人类智能(HI)的深度融合。神经电极和脑组织之间的界面是影响脑机接口性能的关键因素。该界面决定了信息传输效率,直接影响着脑机接口的灵敏度和精准性。以往的研究主要集中在非生物神经界面技术,即通过改进电极结构或材料来提高神经电极的生物相容性,提高脑机接口的长期稳定性。但目前为止,基于生物工程的生物神经界面技术在很大程度上尚未有报道。
本研究通过多功能柔性神经探针,对神经界面进行精准转染,基于核糖核酸干扰(RNAi)的基因沉默技术,成功敲低了神经界面附近神经元中的蛋白酪氨酸磷酸酶(PTEN)和星形胶质细胞中的聚嘧啶束结合蛋白1(PTBP1)基因。PTEN的沉默能够显著提高神经元细胞的生长能力。研究人员对神经退行性疾病模型小鼠在RNA干扰后的神经活动进行了长期检测,发现下调神经元中的PTEN基因序列可以显著改善神经元的电活动。
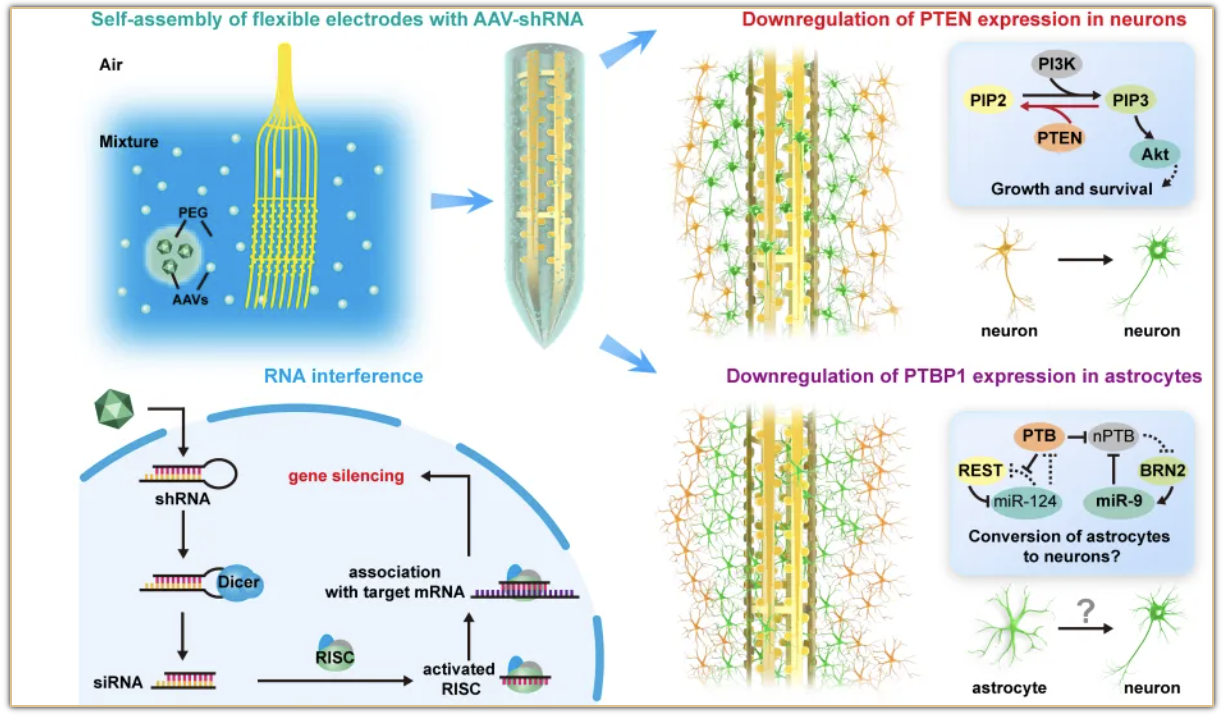
基于基因工程的增强型脑机接口技术
该方法结合了生物工程和非生物工程技术的优势,拓宽了基因工程技术在增强型脑机接口领域的应用,为推动再生神经电子学和下一代脑机接口领域的发展提供了一种前景广阔的工具。
论文链接:
https://onlinelibrary.wiley.com/doi/10.1002/adma.202401327
9. 揭示下联合器在脑发育中的重要作用

2024年5月13日,戈鹉平实验室联合李灵军和孙文智等团队在Nature Neuroscience上发表了文章The subcommissural organ regulates brain development via secreted peptides(下连合器通过分泌神经肽调节脑发育),该研究系统地揭示了subcommissural organ (SCO, 脑下连合器)作为一个脑内腺体通过分泌神经肽在神经元及大脑生长发育中的起重要角色。研究中构建的Sspo-CreER和Sspo-Cre转基因工具小鼠是SCO研究领域的重要进步,同时,这项工作将为今后研究SCO细胞功能发育提供两个珍贵的遗传操纵工具。
研究者通过将Sspo-Cre和Sspo-CreER与DTA小鼠进行杂交,选择性的去除了子代小鼠的绝大部分SCO细胞。他们发现,当小鼠SCO腺体缺失后,它们体型矮小,行动障碍,总体存活率很差。进一步发现,SCO缺陷小鼠的呈现明显脑积水和脑发育缺陷表型。往脑内注射SCO来源的神经肽可以有效地缓解发育表型。这些结果揭示了SCO是在大脑生长发育中扮演重要角色的腺体(见图)。
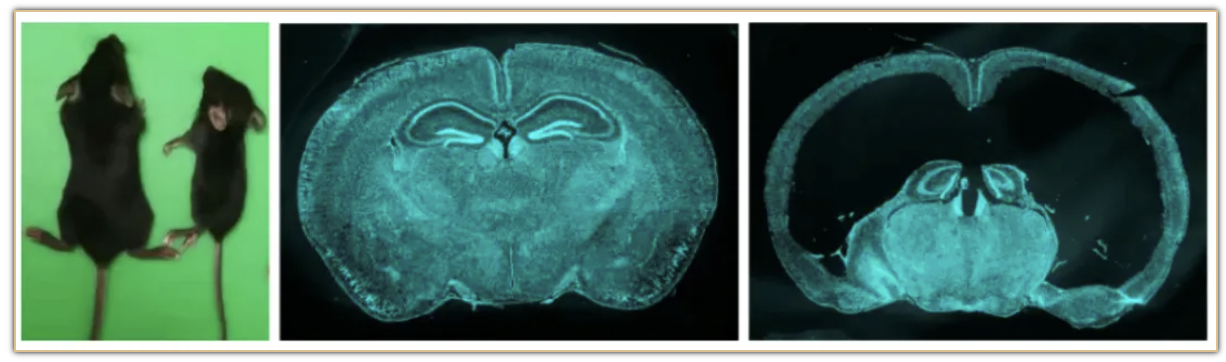
在临床工作中存在很多先天性脑发育畸形伴随脑积水症状的患者,有些患儿在出生后甚至胚胎发育期就存在脑部发育异常,但病因不明。SCO相关的神经肽可能作为药物为这些先天性脑积水或者脑发育异常的患者提供潜在的治疗机会。
论文链接:
https://www.nature.com/articles/s41593-024-01639-x
10. 揭示具有高度时空特异性的ATP信号Inflare在主动编码和呈递损伤信息中的作用

井淼
北京脑科学与类脑研究所 研究员
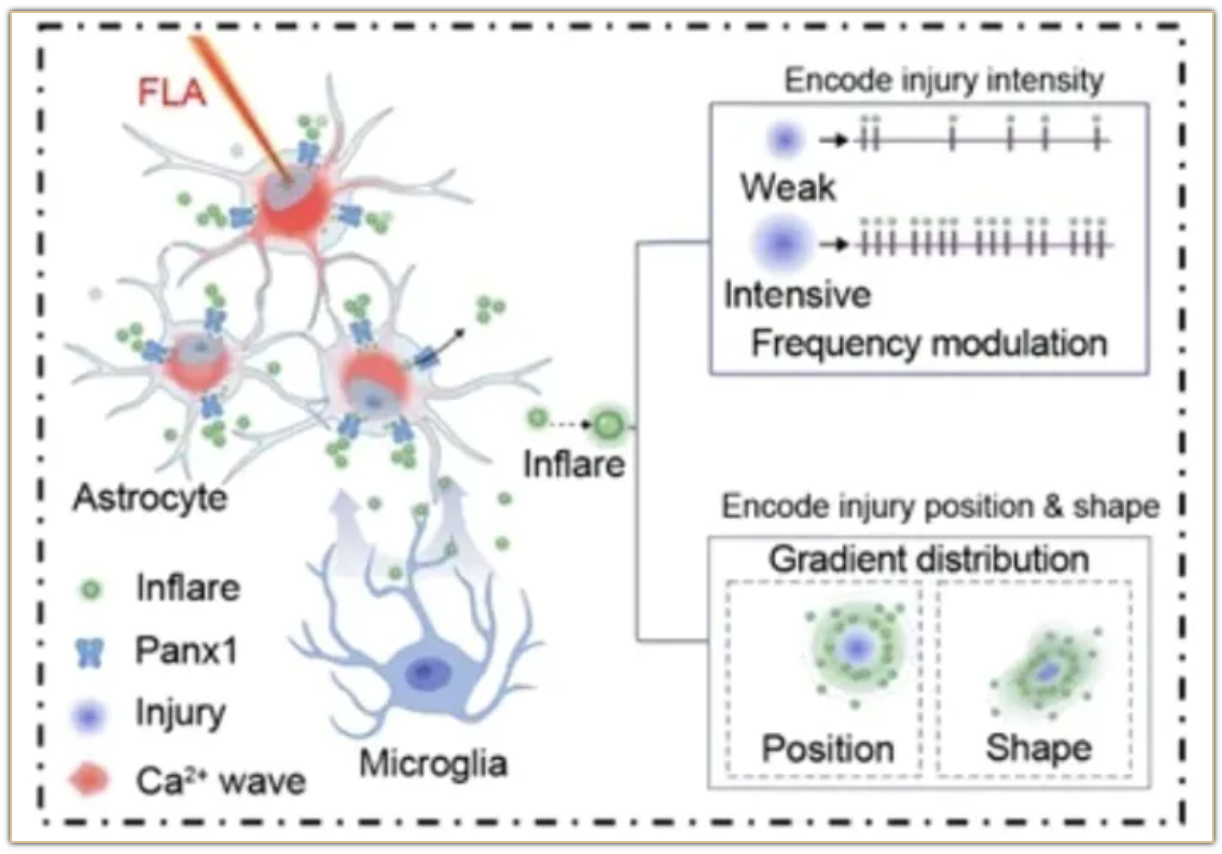
2024年6月11日,井淼实验室在Nature Neuroscience杂志上发表题为Spatiotemporally selective astrocytic ATP dynamics encode injury information sensed by microglia following brain injury in mice的研究文章,首次揭示了一种具有高度时空特异性的ATP信号——Inflare在主动编码和呈递损伤信息中的重要作用。研究发现损伤附近的星形胶质细胞作为监视器可灵敏地捕捉脑内的损伤信息,并将其以“电报”Inflare的方式进行时空上的放大和传递,从而精确高效的指引小胶质细胞进行迁移和损伤应答。重要的是,异常的Inflare电报发放造成的损伤信息错误传递可直接改变损伤后果,而在小鼠卒中模型中靶向Inflare可挽救异常信息传递并明显改善康复效果。该研究为理解脑内损伤应答信息编码和传递机理及其在疾病治疗中的潜在应用奠定基础。
论文链接:
https://www.nature.com/articles/s41593-024-01680-w
11. 发现海马和眶额叶皮层在编码关联结构中的互补作用

周景峰
北京脑科学与类脑研究所 研究员
2024年6月20日,周景峰实验室在Nature Communications发表题为“Hippocampal and orbitofrontal neurons contribute to complementary aspects of associative structure”的研究论文。该研究通过使用钙成像方法,记录头部固定小鼠在整个学习过程中的神经元活动,发现海马和眶额叶皮层在构建和表征环境中感觉信息之间的关联结构中,起到了独特且互补的作用:海马侧重于整合过去和当前的感觉信息,用于表征独特的经历;而眶额叶皮层则侧重于编码共同的任务结构和预期结果,更有助于泛化学习。
该研究通过行为学设计、单细胞钙成像记录和基于模型的数据分析方法,发现在关联学习过程中,小鼠的海马和眶额叶皮层呈现了相似的序列区分信号,它们以独特且互补的方式表征学习到的关联结构的不同方面。海马和眶额叶皮层对于关联学习和记忆至关重要,这些发现扩展了我们对这两个脑区如何以不同方式协同组织关联结构的理解,为进一步探索不同学习和记忆系统的动态相互作用和功能提供了新的研究思路。
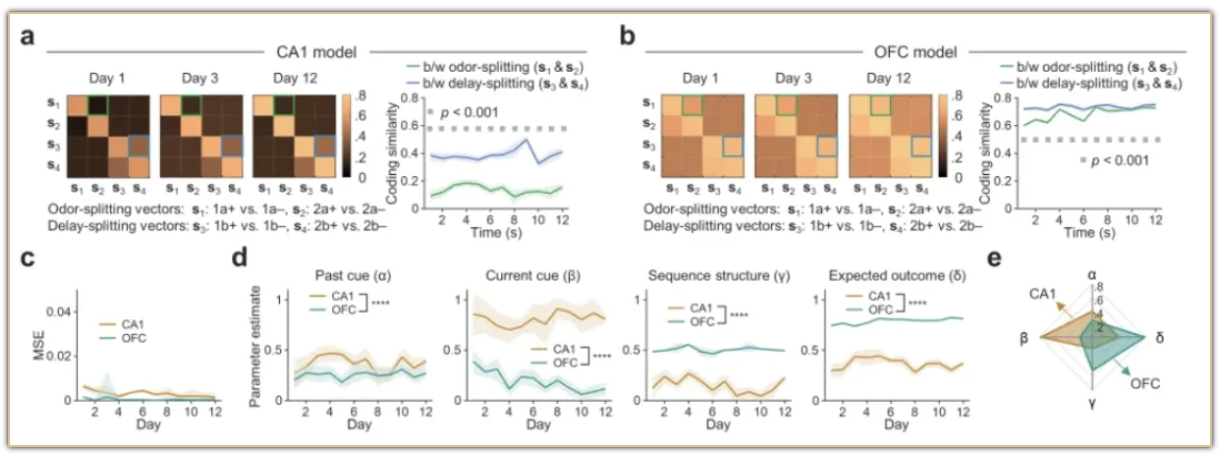
图:模型拟合发现海马和眶额叶皮层中互补的编码内容
论文链接:
https://www.nature.com/articles/s41467-024-49652-9
12. 揭示人类“记忆重现”时的全脑激活模式

柳昀哲
北京脑科学与类脑研究所 研究员
北京师范大学认知神经科学与学习国家重点实验室 教授
2024年8月21日,柳昀哲实验室在Nature Communications上发表了题为“Replay-triggered Brain-wide Activation in Humans”的研究成果。研究团队采用脑电—功能磁共振成像同步采集(electroencephalogram-functional magnetic resonance imaging, EEG-fMRI),研究线索心理模拟任务和清醒静息状态下的神经活动重放及其全脑激活模式。
本研究采用同时记录EEG和fMRI技术,捕捉神经重放事件的时空动态。通过EEG的高时间分辨率,研究能够捕捉到快速的神经重放事件,并借助fMRI定位其在全脑范围内的传播。EEG-fMRI同步采集以及分析流程为研究快速且自发神经活动(包括神经再激活和神经活动重放)及其全脑激活模式提供了一种强大有效的方法。该方法从时间和空间两个方面阐明了人脑的神经再激活和神经活动重放的神经机制,为理解这些现象及其引发的全脑激活模式提供了新的见解。同样的分析流程有助于在不同的研究领域之间架起桥梁,全面理解与人类认知相关的神经重放功能。这为未来的研究开辟了新路径,例如在基于认知地图的计算过程中调查海马神经活动重放和网格状编码(grid-like coding),以及深入理解睡眠期间的记忆巩固。通过这一方法,研究者能够更加深入地理解推理和概括背后的内嗅-海马-前额叶系统。此外,研究结果暗示神经活动重放可能是海马与前额叶皮层之间交流的关键机制,未来找到基于这一机制的生物标志物将是重要的研究方向,有望为调控或治疗提供新的途径。
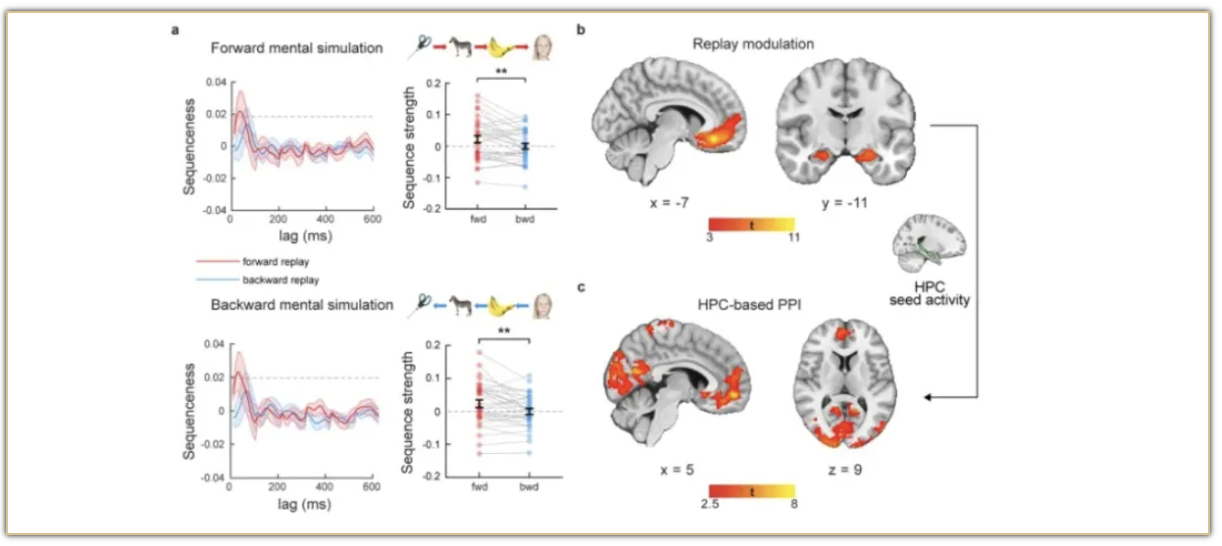
图:在线索心理模拟任务中基于EEG的神经活动重放及其全脑激活模式
论文链接:
https://www.nature.com/articles/s41467-024-51582-5
13. 首次发现大脑中放大厌恶反应的神经环路和调控机制

罗敏敏
北京脑科学与类脑研究所联合所长、特聘研究员
新基石研究员
2024年9月12日,罗敏敏实验室在Neuron上发表题为“A brainstem circuit amplifies aversion”的研究论文。该研究被Nature杂志遴选为“研究亮点”(Research Highlights)。该研究表明,位于脑干的脚间核(Interpeduncular nucleus,IPN)-未定核(Nucleus incertus, NI)环路是大脑中对厌恶反应的放大器(Amplifier),这一发现为情感障碍治疗及阿片类药物复吸预防提供了新的理论基础和潜在的治疗靶点。
研究发现,IPN神经元接受来自MHb和前脑、中脑各区的信息,再通过内部微环路将信息进一步整合,最终传递给其下游NI。IPN-NI环路不仅可以放大恐惧反应,增强回避行为,还参与药物戒断相关的厌恶反应。与杏仁核等相关环路不同,IPN-NI环路并不直接产生厌恶情绪,而是作为厌恶反应的放大器,能够灵活而精确地对外部刺激做出适应性调节,为治疗精神疾病以及药物戒断提供了新的潜在治疗靶点。
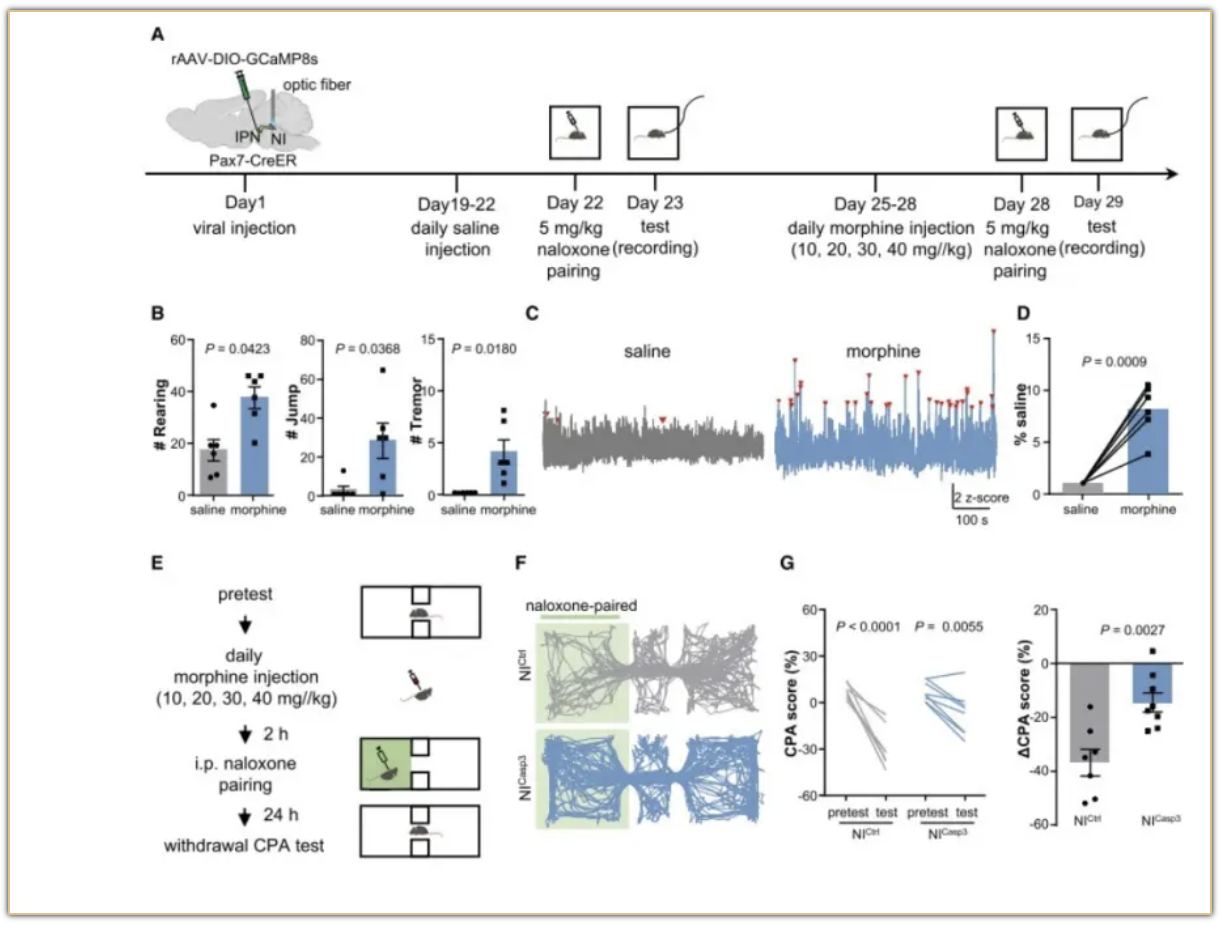
图:IPN-NI通路调节吗啡戒断相关的厌恶反应
论文链接:
https://www.cell.com/neuron/fulltext/S0896-6273(24)00582-8
14. 在可重构感存算一体系统方面取得重要进展

杨玉超
北京脑科学与类脑研究所 双聘研究员
北京大学 长聘教授
2024年11月12日,杨玉超教授团队与北京大学集成电路学院/集成电路高精尖创新中心黄如院士团队在Nature Electronics杂志上发表了题为“Reconfigurable in-sensor processing based on a multi-phototransistor-one-memristor array”的研究论文,在可重构感存算一体集成阵列与硬件系统取得重要进展。
针对现有忆阻器视觉感知神经形态器件在动力学特性和编码功能上的局限以及集成硬件系统算法兼容性不足的问题,首次提出将莫特氧化物异质结结构忆阻器与光晶体管集成,构建了支持多种光图像编码功能的可重构硬件系统。这一系统能够实现光图像的时空、模拟与脉冲编码,并兼容生物启发式和机器学习架构的多种算法,通过与非易失性忆阻器阵列集成可支持多种光学神经网络(如光学卷积神经网络、循环神经网络、脉冲神经网络),从而执行多种计算视觉任务,包括识别静态、运动和彩色图像识别功能,为实现大规模可重构视觉计算硬件系统奠定了关键基础。
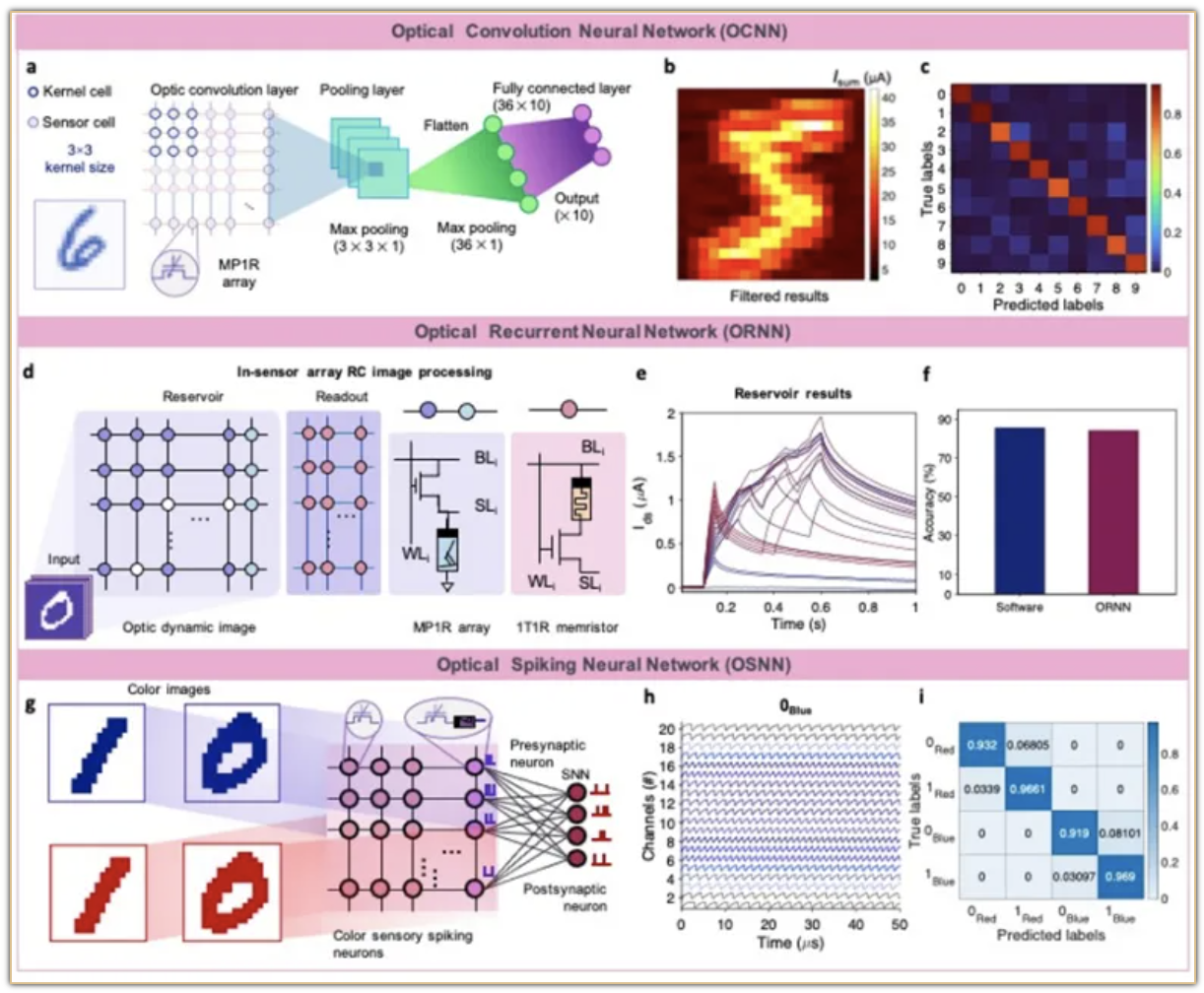
基于可重构感存算一体硬件系统的光卷积神经网络、光循环神经网络与光脉冲神经网络
论文链接:
https://www.nature.com/articles/s41928-024-01280-3
15. 揭示星型胶质细胞释放化学递质的分子机制

罗敏敏
北京脑科学与类脑研究所联合所长、特聘研究员
新基石研究员
2024年11月22日,罗敏敏实验室在Molecular Psychiatry上发表了题为“Astrocytes release ATP/ADP and glutamate in flashes via vesicular exocytosis”的研究论文。该研究首次通过活体全光学方法研究星型胶质细胞释放化学递质的分子机制。

作为大脑中主要的胶质细胞类型,星型胶质细胞具有与神经元明显不同的生理特征,不产生动作电位,也缺乏快速释放化学递质的突触结构和分子机制。然而,星型胶质细胞来源的化学递质(gliotransmitter),如ATP/ADP和谷氨酸等,在大脑生理功能、神经和精神疾病发生中的重要作用日益得到认可。尽管如此,由于缺乏在高时空分辨率上特异且高效地操控星型胶质细胞、检测化学递质释放的工具,其释放的分子机制仍存在巨大争论,且缺乏体内证据。此外,星形胶质细胞与其他胶质细胞(如小胶质细胞)的互作在这些化学递质释放中的作用还不被完全了解。
研究通过本课题组开发的新型光遗传工具cOpn5、遗传编码的荧光分子探针和双光子成像技术,证明星型胶质细胞能够通过囊泡胞吐释放化学递质ATP/ADP和谷氨酸,其中ATP/ADP释放依赖于ATP/ADP的囊泡转运体SLC17A9。ATP/ADP和谷氨酸的释放在荧光闪烁的动力学上有巨大差异,提示两种化学递质释放或胞外清除机制不同。在星型胶质细胞激活过程中,小胶质细胞通过ATP/ADP受体P2Y12快速响应前者释放的ATP/ADP,进一步释放更多ATP/ADP。这一协同释放同样存在于LPS诱导的大脑炎症中。本文为破译胶质细胞的生理和病理功能提供了开创性研究策略,也为相关神经和精神疾病的治疗提供新方向。
论文链接:
https://www.nature.com/articles/s41380-024-02851-8
16. 揭示了协调进食行为的脑-肠神经环路

白凌
北京脑科学与类脑研究所 研究员
2024年12月3日,白凌实验室在Nature Neuroscience杂志在线发表了题为“Parallel gut-to-brain pathways orchestrate feeding behaviors”的研究论文。该研究结合多学科交叉手段,揭示了尾侧孤束核(caudal Nucleus of the solitary tract, cNTS)不同神经元亚群对进食信号的编码情况,并详细解析了两类关键神经元亚型的感觉机制及其对进食行为的调节功能。
研究人员在已发表的单细胞核测序数据集的基础上,利用24色RNAscope技术,系统地鉴定了孤束核内18种遗传异质性的兴奋性神经元亚型,并利用化学遗传学技术,确定了其中9种参与进食调节的群体。在此基础上,研究人员通过改进的光纤记录方法,进一步明确了其中响应进食信号的4种亚型。有趣的是,这4种亚型的活动分别展现出“脉冲型”和“渐进型”两种不同的模式。进一步的功能研究表明,呈现脉冲型活动的Th神经元主要接收迷走感觉神经的输入,表征食道的机械扩张,其活动对于即时维持摄取量的稳定及速率至关重要;而表现出“渐进型”活动的Gcg神经元则编码了来自十二指肠和肝门静脉的营养信息,指导着未来的食物选择。令人惊讶的是,Gcg神经元对营养物质的编码严格依赖于脊髓上行通路,而非领域内传统观点认为的迷走感觉通路。这一发现充分拓展了人们对外周营养感觉信息处理的认识。
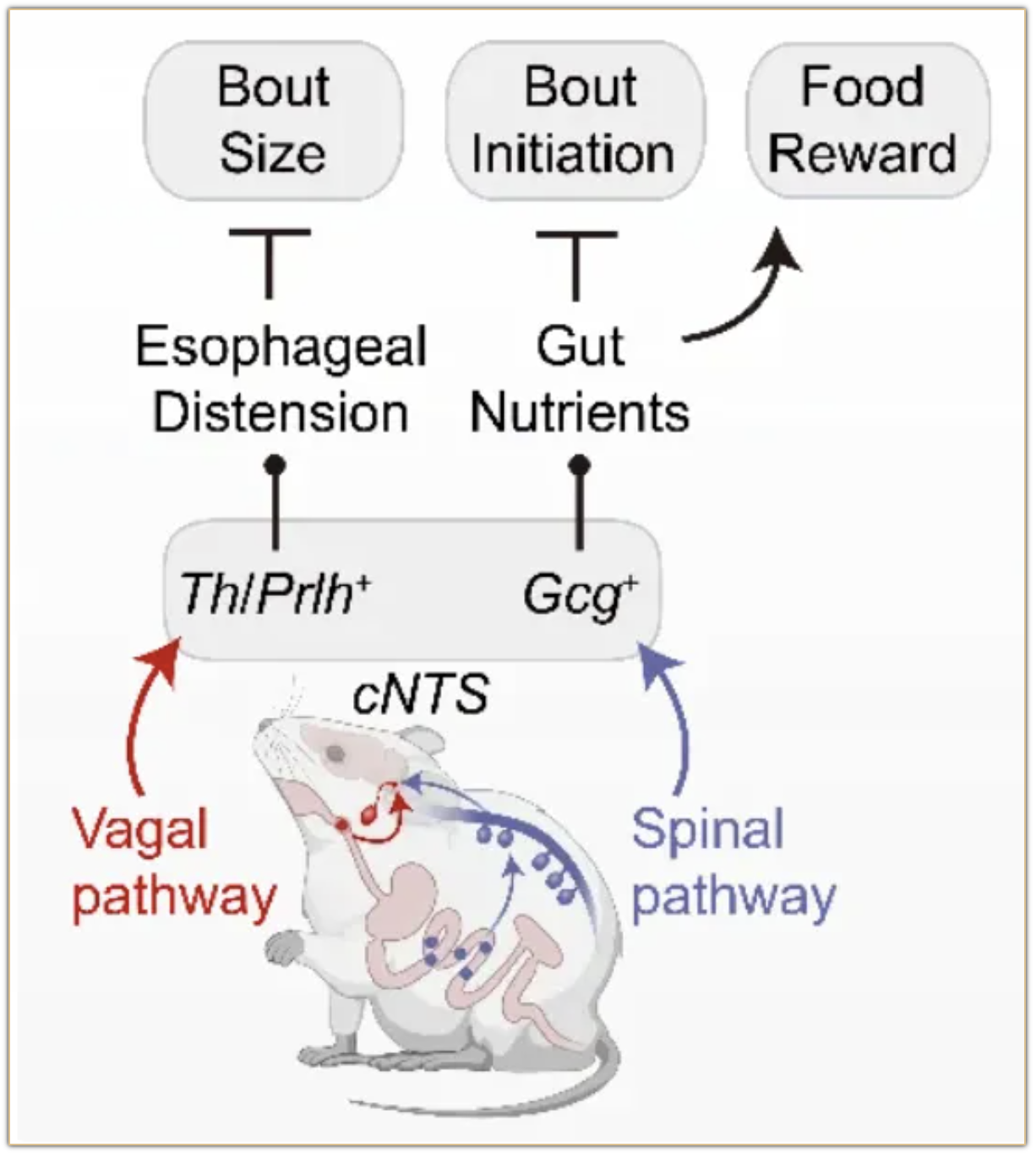
两条平行的肠-脑通路调控摄食的机制图
该研究立足国际脑-体交互领域前沿,系统地阐明了进食信号在初级感觉中枢孤束核的处理逻辑,同时也有望为治疗肥胖、进食障碍等重大疾病提供干预靶点,具有重要的临床转化价值。
论文链接:
https://www.nature.com/articles/s41593-024-01828-8
17. 发现疾病特异抑制性粒细胞参与胶质瘤进程

陈坚
北京脑科学与类脑研究所 研究员
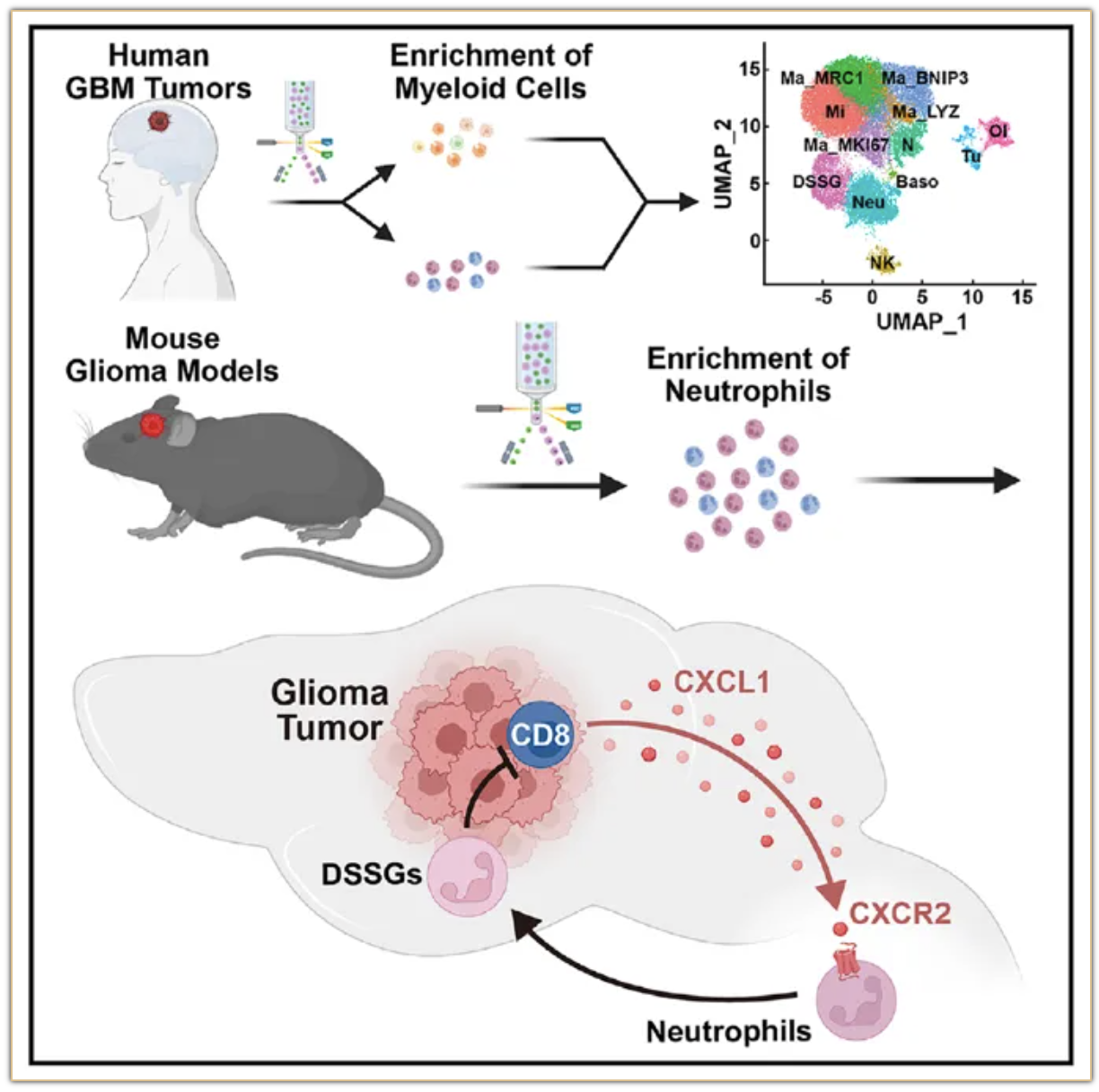
2024年12月24日,陈坚实验室在Cell Reports上发表了题为“Disease-specific suppressive granulocytes participate in glioma progression”的文章。该研究发现仅存在于胶质瘤患者肿瘤中的疾病特异抑制性颗粒细胞(Disease-Specific Suppressive Granulocytes, DSSGs)。等级高的胶质瘤患者的DSSGs的浸润比例高且预后较差。同时发现通过阻断Cxcl1-Cxcr2通路可以有效降低DSSGs的浸润,从而提高CD8+T细胞的比例,延长小鼠的生存。为胶质瘤微环境的探索和胶质瘤患者的治疗提供参考。
胶质瘤是最具侵袭性的肿瘤之一,但是其治疗手段却极为有限,且无法有效地延长患者的生存期。虽然针对胶质瘤的研究较为广泛,但是肿瘤免疫微环境的组成和对胶质瘤进程的影响仍然尚不明朗。本研究通过单细胞转录组测序技术在胶质瘤患者的肿瘤和小鼠的胶质瘤模型中发现了一群相似的疾病特异抑制性颗粒细胞(Disease-Specific Suppressive Granulocytes, DSSGs)。这群细胞仅存在于肿瘤组织中而非外周循环系统。并且相较于其他中性粒细胞,高表达多种免疫抑制性的标志物,例如:CD274和IDO1等。同时借助TCGA和CGGA数据库的数据分析,等级高的胶质瘤患者的DSSGs的浸润比例高且预后较差。依赖小鼠模型,我们发现通过阻断Cxcl1-Cxcr2通路,可以有效的抑制DSSGs向肿瘤中浸润,并且有效延长小鼠的生存。同时我们发现在小鼠模型中降低胶质瘤中浸润的DSSGs,可影响浸润的CD8+ T细胞比例。在胶质瘤患者的DSSGs浸润比例高的肿瘤部位,表达耗竭标志物的CD8+ T细胞的比例较高。另外,我们通过小鼠的联体共生和骨髓移植的实验发现,DSSGs并非全部来源于外周循环系统,而是由颅骨骨髓和脑膜提供并浸润到肿瘤中。借助RNA Velocity analysis和pseudotime trajectory analysis,我们还发现DSSGs是中性粒细胞发育分化的终末期,并且胶质瘤中的微环境会诱导中性粒细胞向DSSGs转变。本研究中,DSSGs的发现以及其来源对胶质瘤抑制性微环境的形成的研究提供了新的思路。
论文链接:



