Nature | 北京脑所罗敏敏团队与北生所邵峰团队揭示脑内皮细胞GSDMD的激活是炎症性血脑屏障破坏的关键机制
2024年04月17日,北京脑科学与类脑研究所罗敏敏团队与北京生命科学研究所邵峰团队合作在Nature上发表题为"Brain endothelial GSDMD activation mediates inflammatory BBB breakdown"的研究论文。该论文深入探讨了革兰氏阴性菌感染或LPS刺激下,脑内皮细胞中的caspase-4/11-GSDMD信号通路的活化导致了脑内皮细胞的膜通透性增加和细胞焦亡,最终造成了血脑屏障的炎症性破坏。这一发现不仅阐明了炎症性血脑屏障破坏的关键分子与细胞生物学机制,也为未来的血脑屏障破坏相关的神经系统疾病治疗提供了新的理论基础和潜在的治疗靶点。

血脑屏障(Blood-brain-barrier,简称BBB)是维持中枢神经系统正常功能的重要结构,由内皮细胞(endothelial cells)、壁细胞(mural cells)、星形胶质细胞(astroctyes)、小胶质细胞/巨噬细胞(microglia/macrophages)以及神经元(neurons)共同构成,是神经血管单元(neurovascular unit)的特殊性质之一。血脑屏障的内皮细胞通常不具备允许物质自由通过的开窗结构(fenestration),却拥有致密的紧密连接体(tight junctions)以及特殊的载体介导的物质转运系统。此外,内皮细胞的转胞吞作用(transcytosis)受到了严格的抑制。血脑屏障为脑组织与外周循环系统之间提供了一道天然的防线,有效阻止了不必要或潜在有害的物质侵入中枢神经系统,同时它还能有选择性地将必需的营养物质输送至中枢神经系统1。然而,在病原体感染或系统性炎症的情况下,血脑屏障的功能可能会受到破坏。这可能促进或直接导致一系列中枢神经系统疾病的发生与发展,如阿尔茨海默病、多发性硬化症、败血症相关脑病等。特别是在革兰氏阴性菌感染引起的败血症的情况下,细菌外壁成分脂多糖(也称内毒素或LPS)进入循环系统后,会引发血脑屏障的炎症性破坏,从而加剧败血症相关脑病的发展。明确革兰氏阴性菌感染如何引起血脑屏障的炎症性破坏具有重要的治疗潜力,但关于引发这一现象的关键分子及其细胞生物学机制,至今仍不完全明确2。
LPS是革兰氏阴性菌细胞外壁的一类重要组成成分,能够被宿主细胞表面的模式识别受体“TLR4/MD2复合体”结合。一旦LPS被TLR4/MD2复合体结合,宿主细胞便通过NF-kB或IRF等关键信号通路,启动下游基因的表达,并诱导多种炎症因子的产生,这对于宿主抵御细菌感染发挥着至关重要的作用3。长期以来,科研界普遍认为LPS通过TLR4介导的转录调控作用是其破坏血脑屏障的主要机制,这可能通过影响包括紧密连接蛋白在内的基因表达,进而增加血脑屏障的通透性。然而,除了在细胞膜表面的识别机制之外,侵入细胞内的LPS还能被小鼠的caspase-11或人类的caspase-4/5识别。这些caspase蛋白在细胞内与LPS结合后发生寡聚化并激活,随后切割其底物GSDMD并释放GSDMD-N端结构域。游离的GSDMD-N端结构域在细胞膜上寡聚并形成孔洞,导致细胞膜通透性增加。最终,GSDMD-N端的强烈激活会引发细胞焦亡。众多研究已经证实,caspase-4/5/11-GSDMD这一通路的异常激活是LPS刺激导致小鼠死亡的主要原因,并且在临床上,它也是革兰氏阴性菌感染引起的败血症导致患者器官衰竭和死亡的关键因素之一。虽然这一通路主要在免疫细胞(如巨噬细胞)中被研究,但近年来的研究发现它在肠上皮细胞等非免疫细胞中也发挥重要作用,这些线索暗示其在非免疫细胞中也可能参与重要的生理或病理过程3。
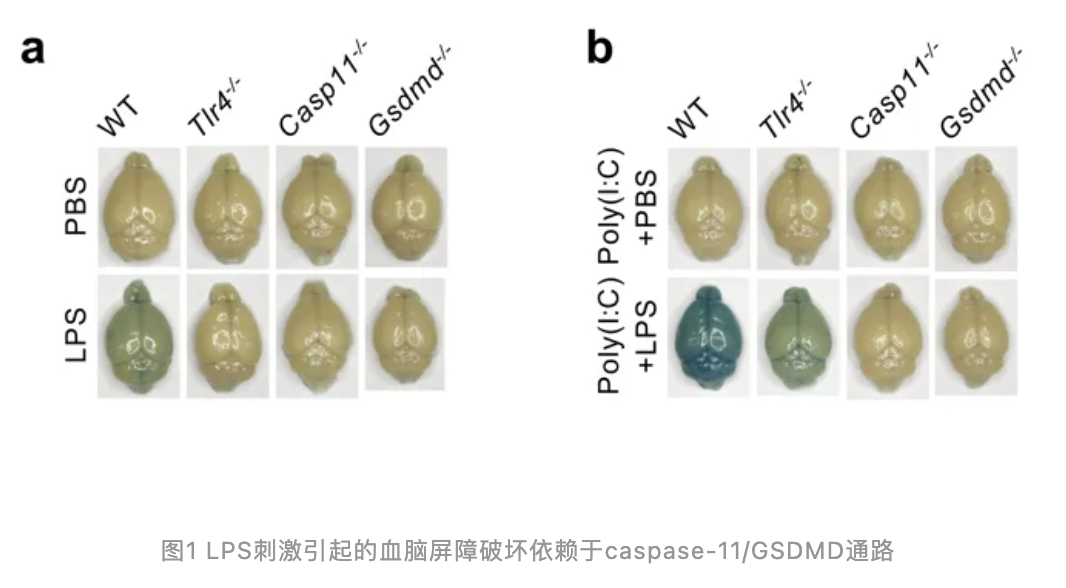
在本研究中,作者首先采用了一种广泛报道的内毒素休克小鼠模型,通过单次腹腔注射LPS来诱导。通过使用不同分子量和化学特性的示踪剂染料(包括~70-kDa Evans blue/albumin、44-kDa HRP、10-kDa TMR-dextran以及433-Da sulfo-NHS-biotin)以评估血脑屏障的完整性,作者观察到LPS刺激能够导致野生型(Wild-type, WT)小鼠的血脑屏障发生显著破坏。然而,在Tlr4基因敲除(Tlr4-/-)、Casp11基因敲除(Casp11-/-)或Gsdmd基因敲除(Gsdmd-/-)的小鼠中,并未发现血脑屏障破坏的明显迹象。尽管在人类细胞中caspase-4是组成型表达的,但在小鼠中,caspase-11的表达受到模式识别受体TLR家族的诱导。因此,作者提前通过腹腔注射模式识别受体TLR3的激动剂poly(I:C),以不依赖TLR4的方式促进caspase-11的表达。令人意外的是,在这种条件下,Tlr4-/-小鼠对LPS刺激引起的血脑屏障破坏表现出明显的反应,而Casp11-/-或Gsdmd-/-小鼠仍然没有血脑屏障破坏的现象。进一步地,作者使用最为灵敏的小分子量示踪剂sulfo-NHS-biotin进行实验,结果显示低剂量(2 mg kg-1)的LPS刺激能够引起poly(I:C) 预处理的WT小鼠血脑屏障的破坏,而Casp11-/-或Gsdmd-/-小鼠则未表现出这种破坏。这些结果表明,caspase-11/GSDMD通路是LPS刺激导致血脑屏障破坏的关键因素。先前的研究表明,血液循环中的LPS首先与游离的LBP蛋白结合,并被呈递给游离的或细胞膜上的CD14受体。CD14不仅能将LPS呈递给TLR4/MD2复合体,启动下游的转录通路,还被报道参与了LPS的细胞内吞作用4。利用poly(I:C)诱导+LPS刺激的内毒素休克小鼠模型,作者发现Lbp基因敲除(Lbp-/-)或Cd14基因敲除(Cd14-/-)的小鼠并不响应LPS诱导的血脑屏障破坏。这一发现暗示,LPS可能通过LBP-CD14转运/内吞通路进入细胞内部,进而激活caspase-11/GSDMD通路,从而导致血脑屏障的破坏。
随后,作者深入研究了caspase-11和GSDMD在小鼠大脑中的表达情况。通过免疫荧光染色技术,作者发现GSDMD蛋白特异性地在小鼠的脑血管内皮细胞中表达,而非血管壁细胞。为了更全面地理解脑内皮细胞在系统性炎症发生时的信号转导变化,作者对WT和Gsdmd-/-成年小鼠的脑运动皮层进行了高质量的单细胞RNA测序分析。有趣的是,他们观察到,虽然脑内皮细胞本底不表达或低表达Casp11和Cd14;在LPS刺激下,Casp11和Cd14的表达却在脑内皮细胞中得到了显著上调。此外,通过mRNA荧光原位杂交(FISH)技术,研究结果进一步证实了caspase-11在脑内皮细胞中的本底表达水平非常低,但在LPS刺激下会出现显著的上调。单细胞RNA测序分析不仅突出了脑内皮细胞是对系统性LPS刺激反应最为迅速和强烈的中枢神经系统细胞类型,还揭示了在这些细胞中,与炎症、免疫反应和细胞因子通路相关的多个基因的表达水平发生了显著的上调。
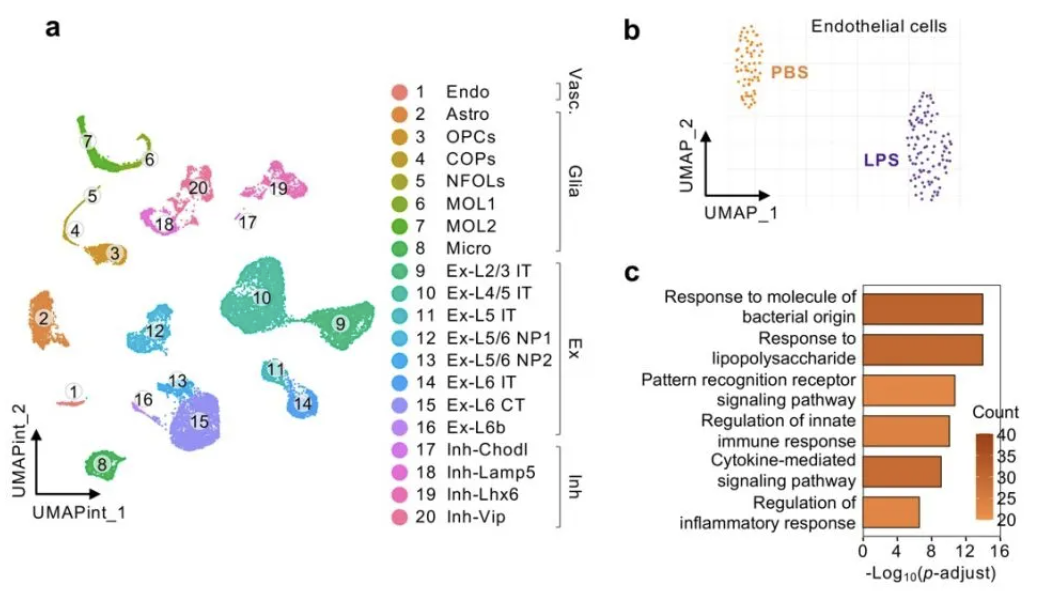
图2 脑内皮细胞强烈响应LPS刺激
接着,作者采用透射电子显微镜对LPS诱导的血脑屏障破坏区域进行了细致的超微结构成像分析。成像结果显示,脑内皮细胞及其周围的血管结构发生了显著的变化,而这些变化依赖于GSDMD的活性。具体来说,受损血管的部分内皮细胞出现了细胞核凝聚和细胞质皱缩的细胞焦亡现象,这些细胞残骸仍然通过紧密连接或其他细胞间连接结构附着在血管壁上。同时,这些受损血管的内皮层从血管的基底膜层发生了脱落,并且邻近的脑实质区域常常伴随着水肿的发生。值得注意的是,在Gsdmd-/-小鼠中,这些超微观层面的结构性破坏并没有被观察到。
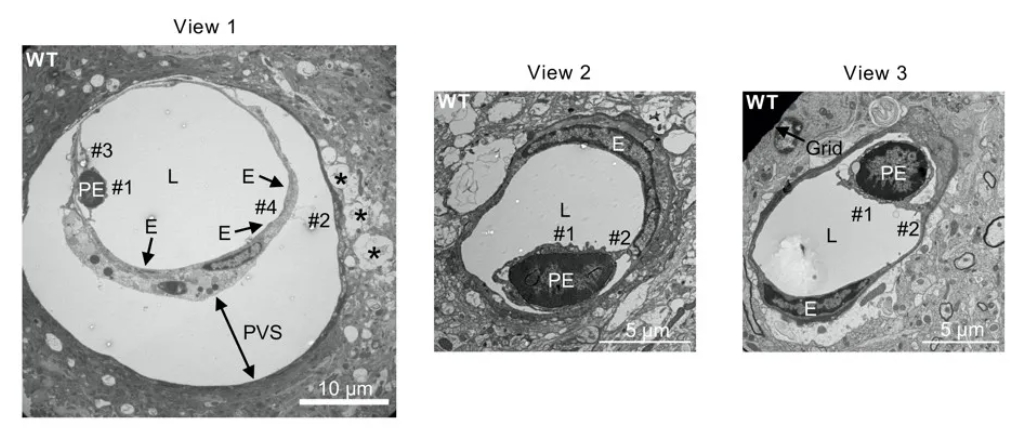
图3 LPS刺激引起WT小鼠的血脑屏障出现超微的结构性破坏
在接下来的研究中,作者采用了由上海分子细胞卓越中心周斌团队开发的Dre-rox和Cre-loxP双重重组酶转基因小鼠5(由Tie2-Dre; Mfsd2a-CrexER构成,简称bEC-Cre小鼠),这一系统能够高效且特异性地在脑内皮细胞中进行遗传操作。通过将bEC-Cre小鼠与Gsdmdflox/flox小鼠杂交,作者成功得到了一种特异性敲除脑内皮细胞中Gsdmd基因的小鼠模型(简称GD-CKO小鼠)。此外,作者还利用特异性靶向脑内皮细胞的AAV-BI30腺相关病毒6(由美国博德研究所Benjamin E. Deverman团队和哈佛大学顾成华团队共同开发),在Gsdmdflox/flox小鼠的脑内皮细胞中表达Cre重组酶,同样实现了高效敲除脑内皮细胞的Gsdmd基因(简称AAV-GD-CKO小鼠)。在预先给予poly(I:C)处理的条件下,GD-CKO和AAV-GD-CKO小鼠均能有效避免LPS刺激引起的血脑屏 障破坏。作者进一步通过AAV-BI30腺相关病毒或另一种靶向脑内皮细胞的AAV-BR1腺相关病毒7(由德国奥格斯堡大学附属医院Martin Trepel团队开发),特异性地恢复Gsdmd-/-小鼠脑内皮细胞中的Gsdmd表达。实验结果显示,只有回补了野生型的GSDMD蛋白,而非切割位点突变型(D276A)的GSDMD蛋白,才能使Gsdmd-/-小鼠恢复对LPS刺激下血脑屏障破坏的敏感性。此外,作者还培育了bEC-Cre; Ai14; Gsdmd+/+小鼠和bEC-Cre; Ai14; Gsdmdflox/flox小鼠,这些小鼠的脑内皮细胞特异性表达tdTomato荧光蛋白,使得他们首次能够在体内条件下观察到因GSDMD依赖性的细胞膜通透性增加而导致的细胞内蛋白的丢失。在bEC-Cre; Ai14; Gsdmd+/+小鼠中,血脑屏障破坏区域的脑内皮细胞显著丢失tdTomato信号,并且这些细胞往往大量摄取sulfo-NHS-biotin示踪剂,而这种现象在bEC-Cre; Ai14; Gsdmdflox/flox小鼠中并未观察到。最后,作者通过AAV-BR1腺相关病毒在Rosa26LSL-mGsdmd-N/+小鼠的脑内皮细胞中特异性表达iCre,从而人为地在脑内皮细胞内表达GSDMD-N端结构域。这一操作无需LPS刺激,即能实现依赖于GSDMD的血脑屏障破坏。以上的实验结果表明:GSDMD的激活引发的细胞膜通透性增加和细胞焦亡是LPS诱导血脑屏障破坏的关键分子和细胞生物学机制。
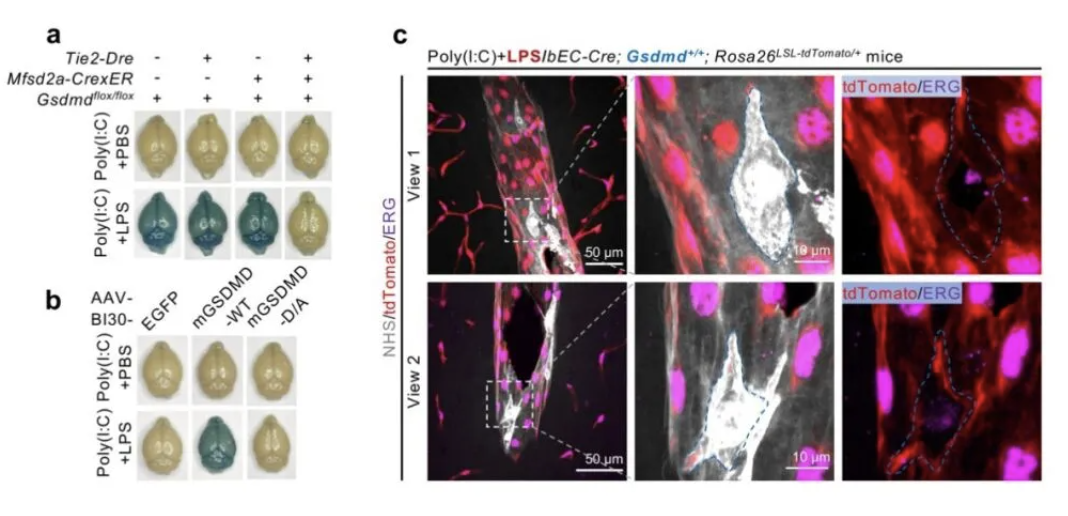
图4 脑内皮细胞GSDMD的激活改变血脑屏障通透性
肺炎克雷伯菌(Klebsiella pneumoniae,简称K. pneumoniae)是一种广泛存在于自然环境中的条件致病菌,它能够感染人类的呼吸系统、泌尿系统、神经系统和血液系统。作为继大肠杆菌之后的第二大导致血液感染的革兰氏阴性菌,肺炎克雷伯菌也是社区获得性感染和医院内感染的常见病原体之一。在本研究中,作者揭示了肺炎克雷伯菌的LPS能够通过CASP4-GSDMD通路,以触发人类上皮细胞系HeLa细胞和人脑内皮细胞系hBMEC细胞发生细胞焦亡。与小鼠相比,人类对LPS的毒性表现出更高的敏感性,这可能归因于几个关键因素:首先,小鼠的caspase-11需要经过感染或/和炎症的诱导才能表达,而人类的caspase-4通常是组成型表达的;其次,小鼠的caspase-11与人类的caspase-4在底物选择性上存在差异;最后,人类的caspase-4相较于小鼠的caspase-11展现出更强的LPS识别能力和底物切割能力。因此,CASP4转基因小鼠模型(CASP4Tg小鼠)对低剂量LPS的毒性表现出更高的敏感性8,这一特性使其成为模拟临床败血症/脓毒症的更加精确的模型。在CASP4Tg小鼠中,不需要预先的poly(I:C)处理,仅仅2 mg kg-1的LPS刺激就足以引起血脑屏障的破坏;而在CASP4Tg; Gsdmd-/-小鼠中,这种破坏并未发生。这提示CASP4Tg小鼠响应LPS刺激引起的血脑屏障破坏仍然依赖于GSDMD。利用AAV-BI30腺相关病毒在WT小鼠的脑内皮细胞中特异性地表达高亲和力的GSDMD抑制型纳米抗体VHHGSDMD-19,10,作者发现,LPS引起的血脑屏障破坏得到了显著的缓解。同样,在感染AAV-BI30-VHHGSDMD-1腺相关病毒的CASP4Tg小鼠中,肺炎克雷伯菌感染导致的血脑屏障破坏也显著减轻。这些发现强调了脑内皮细胞中GSDMD激活在肺炎克雷伯菌感染引起的血脑屏障破坏中的核心作用,并指出利用抑制型纳米抗体靶向脑内皮细胞中的GSDMD可能成为一种有效的治疗策略,以保护血脑屏障免受革兰氏阴性菌感染的侵害。
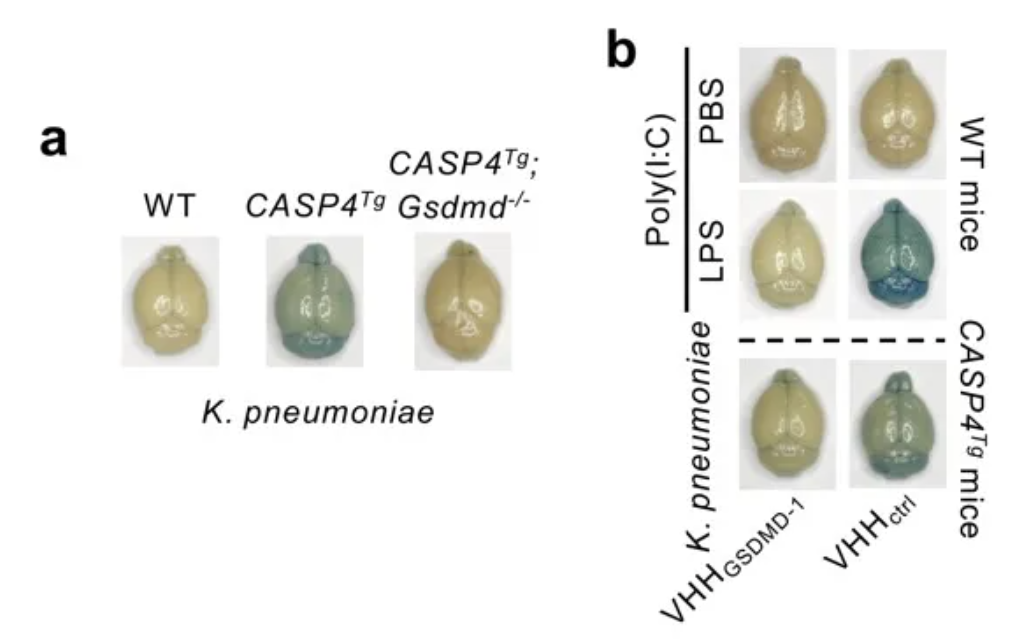
图5 肺炎克雷伯菌通过激活脑内皮细胞的GSDMD导致血脑屏障破坏
本篇论文的研究成果为血脑屏障领域的一个长期悬而未决的问题提供了明确的答案:证实了在系统性炎症环境下,由LPS刺激引发的血脑屏障破坏,主要是由脑内皮细胞中caspase-4/11-GSDMD通路的激活所引起的。激活的GSDMD在脑内皮细胞的细胞膜上形成孔洞,增加了细胞膜的通透性。GSDMD的过度激活触发脑内皮细胞经历裂解性死亡——细胞焦亡。细胞膜通透性的增加和细胞焦亡的发生共同促进了脑与外周循环系统之间的物质交换,这构成了血脑屏障炎症性破坏的新机制。GSDMD的发现无疑为其作为药物靶点提供了巨大的潜力。一方面,针对GSDMD的靶向激动剂设计,可能成为调节血脑屏障通透性的新策略,为跨血脑屏障递送中枢神经系统疾病治疗药物开辟了新的视野。另一方面,通过开发针对GSDMD的靶向抑制剂,我们或许能够在革兰氏阴性菌感染患者需要时,为他们的血脑屏障提供有效保护,减轻中枢神经系统的损伤。综上所述,该论文不仅将GSDMD的研究推进到了神经科学的新领域,而且从分子和细胞层面深入阐释了细菌感染和LPS刺激如何导致血脑屏障的破坏。这些发现不仅丰富了我们对血脑屏障功能的认识,也为治疗与血脑屏障破坏相关的神经系统疾病提供了新的思路和潜在的治疗方向。
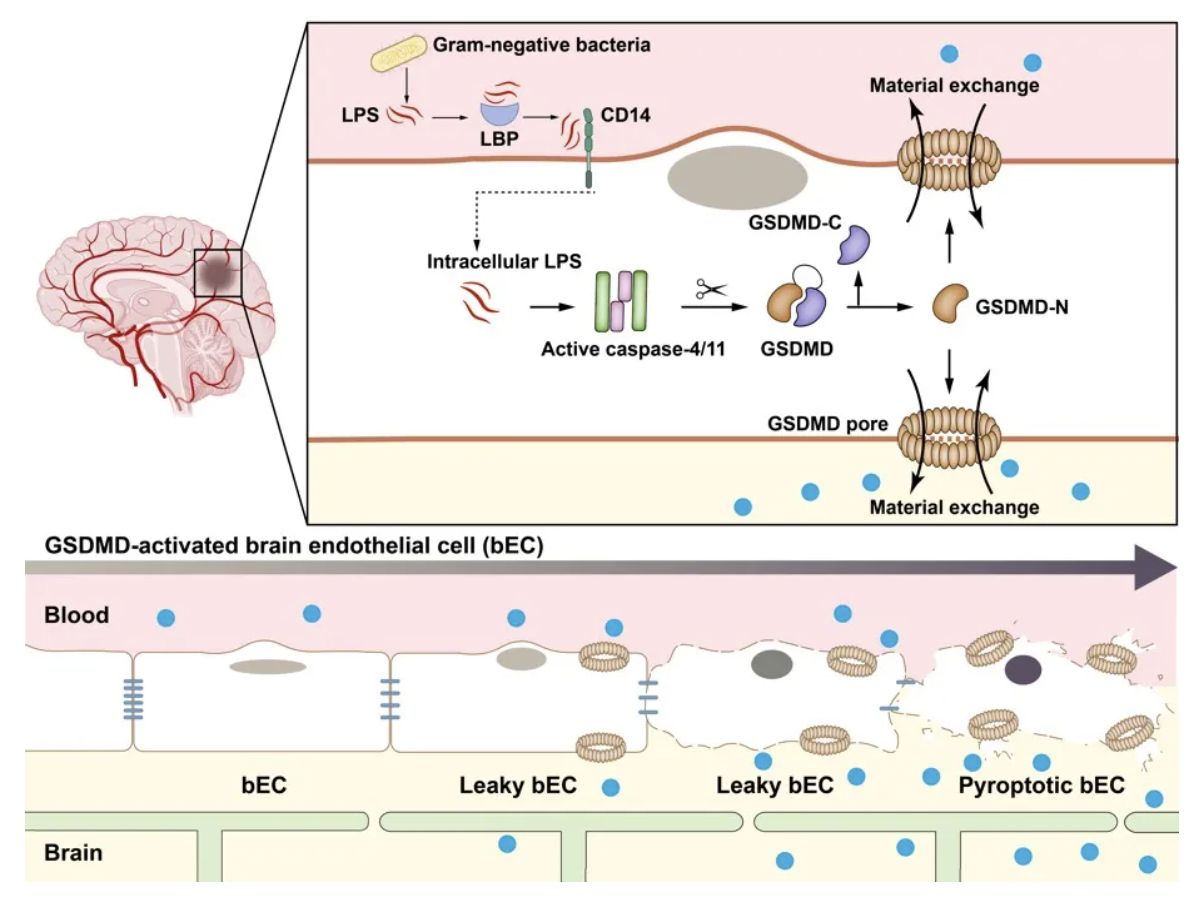
图6 GSDMD破坏血脑屏障模式图
论文信息
北京脑科学与类脑研究所罗敏敏实验室的副研究员韦超博士和北京生命科学研究所邵峰实验室的博士后蒋唯博士为本文共同第一作者。罗敏敏实验室的博士后王睿宇博士完成了该研究的单细胞RNA测序与分析的工作,对本论文有重大贡献。论文的其他作者还包括北京脑所的高辛未、钟诗琳博士、于凤婷、郭青春博士、张力博士;北生所的钟皓宇、何华斌博士;德国波恩大学的Florian I. Schmidt博士、Lisa D.J. Schiffelers;中国科学院分子细胞科学卓越创新中心的周斌博士;以及德国奥格斯堡大学附属医院的Martin Trepel博士。罗敏敏博士和邵峰博士为该论文的共同通讯作者。此外,南京医科大学的韩峰博士和卢应梅博士,华中农业大学的王湘如博士,美国纽约西奈山伊坎医学院的JD Buxbaum博士,北生所的动物中心和电镜中心,以及北京脑所的动物中心、基因组学中心、光学影像中心和载体工程中心,对本论文提供了帮助。本研究由国家自然科学基金基础科学中心项目,国家重点研发计划项目,中科院战略性先导科技专项,中国医学科学院医学创新单元,科技部科技创新2030-“脑科学与类脑研究“重大项目,北京市政府,以及腾讯新基石研究员项目资助,在北京脑所和北生所完成。
参考文献
1. Langen, U. H., Ayloo, S. & Gu, C. Development and Cell Biology of the Blood-Brain Barrier. Annu Rev Cell Dev Biol 35, 591-613 (2019).
2. Peng, X., Luo, Z., He, S., Zhang, L. & Li, Y. Blood-Brain Barrier Disruption by Lipopolysaccharide and Sepsis-Associated Encephalopathy. Front Cell Infect Microbiol 11, 768108 (2021).
3. Rathinam, V. A. K., Zhao, Y. & Shao, F. Innate immunity to intracellular LPS. Nat Immunol 20, 527-533 (2019).
4. Ryu, J. K. et al. Reconstruction of LPS Transfer Cascade Reveals Structural Determinants within LBP, CD14, and TLR4-MD2 for Efficient LPS Recognition and Transfer. Immunity 46, 38-50 (2017).
5. Pu, W. et al. Genetic Targeting of Organ-Specific Blood Vessels. Circ Res 123, 86-99 (2018).
6. Krolak, T. et al. A High-Efficiency AAV for Endothelial Cell Transduction Throughout the Central Nervous System. Nat Cardiovasc Res 1, 389-400 (2022).
7. Korbelin, J. et al. A brain microvasculature endothelial cell-specific viral vector with the potential to treat neurovascular and neurological diseases. EMBO Mol Med 8, 609-625 (2016).
8. Kajiwara, Y. et al. A critical role for human caspase-4 in endotoxin sensitivity. J Immunol 193, 335-343 (2014).
9. Schiffelers, L. D. J. et al. Antagonistic nanobodies reveal mechanism of GSDMD pore formation and unexpected therapeutic potential. bioRxiv, 2023.2004.2020.537718 (2023).
10. Kopp, A. et al. Pyroptosis inhibiting nanobodies block Gasdermin D pore formation. Nat Commun 14, 7923 (2023).
论文链接
https://www.nature.com/articles/s41586-024-07314-2
视频链接
https://mp.weixin.qq.com/s/BGjB3WTW7Kc5HlmJ9yodlQ



