Brain-body interface: Sympathetic regulation of energy balance and brain-body communication
2026年3月18日,北京脑科学与类脑研究所邀请清华大学基础医学院曾文文教授,开展了一场题为“Brain-body interface: Sympathetic regulation of energy balance and brain-body communication”的学术报告,系统介绍了其实验室近年来关于交感神经系统参与脑与外周器官之间双向调控的一系列研究工作。报告由陈坚研究员主持。

曾文文博士
清华大学基础医学院教授
曾文文教授 2002 年于清华大学获生物科学与技术专业学士学位,2009 年获美国德克萨斯大学西南医学中心博士学位。2009-2011 年在美国基因泰克公司从事博士后研究,2011-2014 年于美国洛克菲勒大学完成博士后训练。2014年入职清华大学,现任基础医学院教授。
曾教授团队长期聚焦脑 - 体界面的交感神经调控机制,以脂肪、肠道等外周代谢器官为核心模型,系统解析交感神经如何作为中枢与外周的关键桥梁,双向介导脑-体通讯并精准调控机体能量平衡,同时深入揭示交感神经支配在代谢稳态维持中的可塑性规律,以及其通过调控肠道内分泌信号、血糖代谢进而影响中枢认知功能的跨器官通路。
自建组以来,曾教授团队以小鼠为模型系统绘制了脂肪、肠道等外周器官的交感神经支配图谱,率先在单细胞纤维分辨率下揭示脂肪组织交感神经支配的结构基础与可塑性调控机制,阐明交感神经通过调控肠道内分泌信号影响血糖稳态与大脑认知功能的跨器官通路,并深入解析神经-免疫互作在代谢与炎症疾病中的关键作用,相关原创性成果发表于Cell、Neuron、Cell Metabolism等国际权威期刊,同时开发新型免疫调节分子与疫苗佐剂并推动转化应用,为脑-体通讯、神经代谢与神经免疫领域的理论创新和临床干预提供了核心支撑与全新方向。
报告开始,曾文文博士首先对交感神经系统的基本功能进行了概述。传统观点认为,交感神经系统是机体在应对外界刺激和压力时启动“fight-or-flight”反应的关键执行通路,在调节心率、血压、血糖、脂肪动员及能量分配等方面发挥重要作用。然而,随着近年来神经科学、免疫学和代谢生物学的交叉发展,交感神经系统已不再被简单理解为一种应激反应装置,而被视为连接中枢神经系统(central nervous system, CNS)与多种外周器官的重要调控通路。基于这一背景,曾教授团队长期关注的核心问题是:中枢神经系统如何通过交感神经影响外周代谢器官和免疫组织,而外周组织又如何反向作用于脑功能与整体稳态。
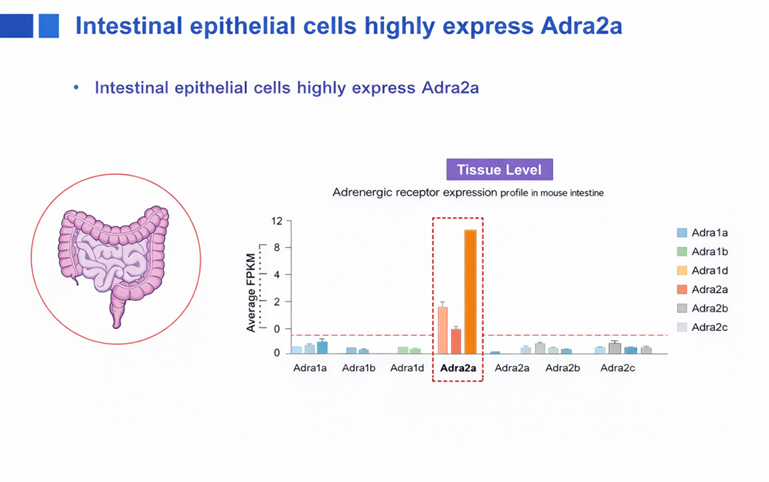
首先,曾教授介绍了其团队围绕肠内分泌L细胞(enteroendocrine L cells)与肠道交感神经之间功能联系所开展的研究。肠道不仅是营养吸收的重要器官,同时也是神经、内分泌与免疫信号整合的重要场所。其中,L细胞能够分泌胰高血糖素样肽-1(glucagon-like peptide-1, GLP-1)等肠促胰素,在葡萄糖耐量、胰岛素分泌及食欲调控中发挥重要作用。团队发现,Adra2a在肠道上皮细胞中高表达。利用基因敲除小鼠模型揭示了一条新颖的“肠-脑轴”通路:交感神经活动增强时,释放的去甲肾上腺素作用于肠道Adra2a受体,抑制肠道L细胞分泌GLP-1。GLP-1释放减少导致血糖升高,同时大脑葡萄糖摄取降低,进而损害认知功能。敲除Adra2a可解除该抑制,增加GLP-1释放,改善血糖水平和认知能力。这揭示了交感神经在应激状态下通过优先分配能量至外周器官(如心脏、肝脏),而非大脑,以应对即时需求的生理逻辑。
接下来曾教授聚焦于脂肪组织,尤其是白色脂肪组织(white adipose tissue, WAT)和棕色脂肪组织(brown adipose tissue, BAT)中的交感神经支配。曾教授指出,脂肪组织并非仅是被动储存能量的场所,而是接受丰富神经支配、能够主动参与全身代谢稳态调节的重要器官。团队通过高分辨率成像技术,首次清晰展示了白色脂肪组织中存在密集的交感神经支配,颠覆了其“仅受激素调控、无直接神经输入”的传统认知。
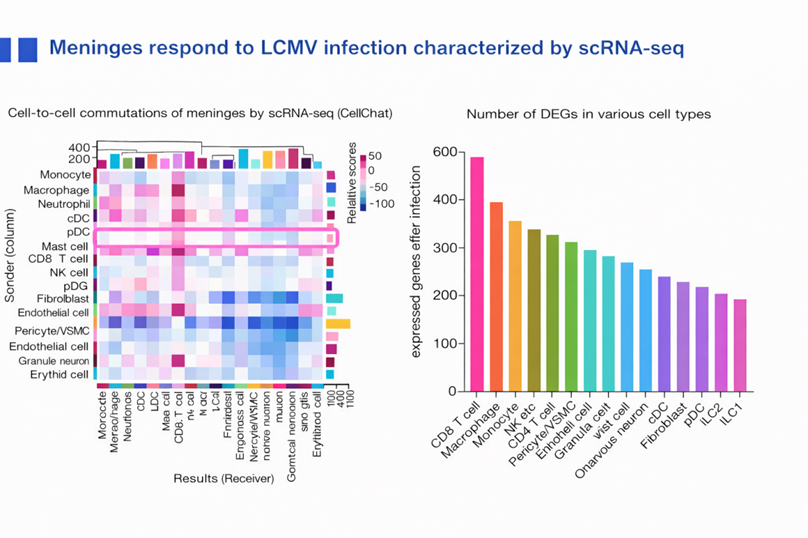
报告最后转向中枢边界结构,重点介绍了脑膜在免疫监视中的作用。曾教授指出,脑膜并非传统意义上单纯起机械保护作用的被膜结构,而是一个包含丰富免疫细胞和基质成分的活跃界面组织。在这一组织中,免疫细胞能够监测来自循环系统和中枢微环境的信号,并在感染、炎症或损伤状态下作出快速反应。在脑膜免疫细胞中,曾教授团队重点研究了肥大细胞。团队开发了新型遗传工具——Tpsb2-CreERT2小鼠,特异性标记脑膜中的结缔组织型肥大细胞,发现其数量远超既往认知,是脑膜中仅次于巨噬细胞的第二大免疫细胞群。在感染模型方面,团队利用淋巴细胞性脉络丛脑膜炎病毒(lymphocytic choriomeningitis virus, LCMV)感染模型研究脑膜免疫变化,感染后脑膜的细胞组成、转录状态及细胞间通讯关系均发生明显重塑,其中肥大细胞表现出较为突出的应答特征,在感染过程中上调了多种与干扰素反应、抗原呈递及感染应答相关的分子程序。在机制层面,曾教授重点介绍了脑膜中一个关键的信号通路,即白细胞介素-33–ST2信号轴(interleukin-33–ST2 signaling axis):肥大细胞高表达ST2(interleukin 1 receptor-like 1, IL1RL1),而白细胞介素-33(interleukin-33, IL-33)则主要来源于脑膜中的Prrx1阳性基质细胞(Prrx1-positive stromal cells)。感染发生后,脑膜局部IL-33水平发生变化,提示基质细胞可能在脑膜免疫反应的早期阶段发挥信号发起作用。脑膜肥大细胞对于抗病毒细胞免疫的建立是必要的,感染后肥大细胞可通过转录重塑和脱颗粒反应促进CD8⁺ T细胞的募集及功能发挥,从而有助于病毒清除。相反,当肥大细胞被耗竭或其关键信号通路受损时,脑膜局部的抗病毒免疫能力下降。由此可见,脑膜作为脑与外周之间的重要边界,不仅是结构屏障,更是一个具备主动免疫调控能力的功能界面。
在提问环节,现场师生与曾文文教授进行了热烈的互动交流,主要围绕其研究的核心机制、潜在应用及技术细节展开。提问聚焦于交感神经调控代谢与免疫的具体分子通路、其在阿尔茨海默病等神经退行性疾病中的角色,以及如何将“脑-体交互”这一基础研究发现转化为针对肥胖、糖尿病或免疫相关疾病的干预策略。此外,师生们也对研究中使用的特异性遗传工具(如Tpsb2-CreERT2小鼠模型)的开发与应用、神经免疫回路研究的未来方向,以及该领域与分子靶向治疗等前沿技术的交叉可能性表现出浓厚兴趣。
撰稿人:郭思源、姜文轩