Sexual Dimorphism of Neuroimmune Regulation
2026年3月25日上午,北京脑科学与类脑研究所邀请北京大学生命科学学院杨竞教授作题为“Sexual Dimorphism of Neuroimmune Regulation”的学术报告。

杨竞博士
北京大学生命科学学院研究员
杨竞教授于2003年毕业于北京大学生命科学学院,获理学学士学位;2004年至2009年师从诺贝尔奖得主Michael Brown和Joseph Goldstein教授于美国得克萨斯大学西南医学中心获得生物医学博士学位,2009年至2015年师从Marc Tessier-Lavigne教授先后在美国基因泰克公司和洛克菲勒大学从事博士后研究,2015年入职北京大学生命科学学院担任博士生导师。现任北京大学博雅特聘教授,北京大学第三医院双聘教授及北京协和医院名誉教授。
杨竞教授长期致力于生物医学前沿交叉领域研究,整合临床资源、动物疾病模型、先进成像技术、多组学分析等跨学科手段,致力于生物医学前沿交叉方向,探索神经系统、免疫系统、代谢系统、循环系统等互作调控,在分子、细胞、器官、机体等不同层面开拓神经免疫(neuroimmunology)、神经代谢(neurometabolism)、肿瘤神经生物学(cancer neuroscience)等创新概念和视角,鉴定并验证神经系统疾病、代谢疾病、恶性肿瘤等重大人类疾病的全新诊疗策略和药物靶点。
本次报告中,杨竞教授重点介绍了神经免疫调控中性别二态性(Sex Dimorphism)方面的最新研究进展围绕视神经脊髓炎(Neuromyelitis Optica Spectrum Disorder, NMOSD)、肝纤维化及过敏性哮喘三类疾病模型,系统解析了中枢神经系统与外周神经系统中神经免疫互作受性别差异影响的分子调控机制。
中枢神经系统:NMOSD中的雌激素促炎作用
NMOSD是一种具有明显女性发病倾向的疾病。利用星形胶质细胞水通道蛋白-4(AQP4)抗体构建的NMOSD模型显示,与雄鼠相比,雌鼠表现出更严重的神经免疫反应和脱髓鞘损伤,具体表现为小胶质细胞中神经免疫应答相关转录因子PU.1(又称SPI1)和IRF8表达上调,以及成熟髓鞘少突胶质细胞数量减少。对雌鼠进行卵巢切除、对雄鼠进行去势手术并外源性补充雌激素后,NMOSD模型的性别二态性特征被显著逆转。由此表明,AQP4抗体介导的NMOSD模型中的女性易感性与高水平的雌激素密切相关。
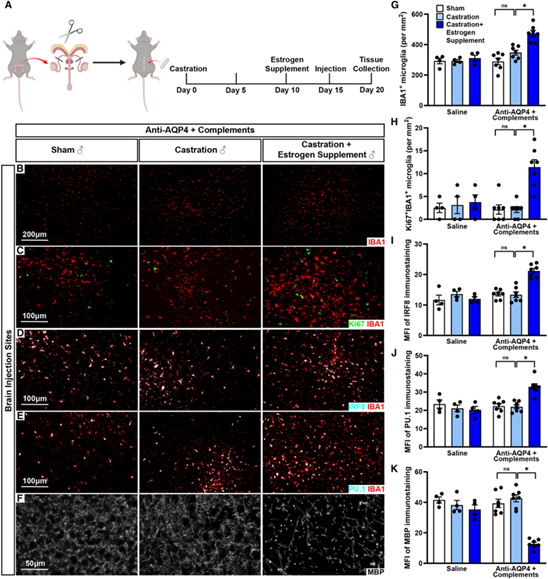
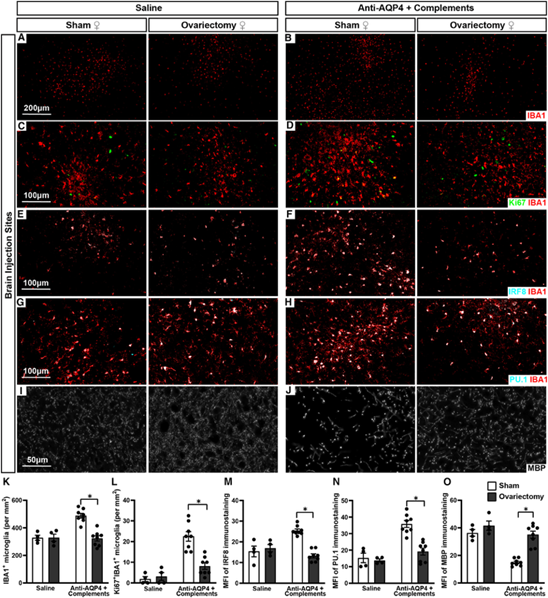
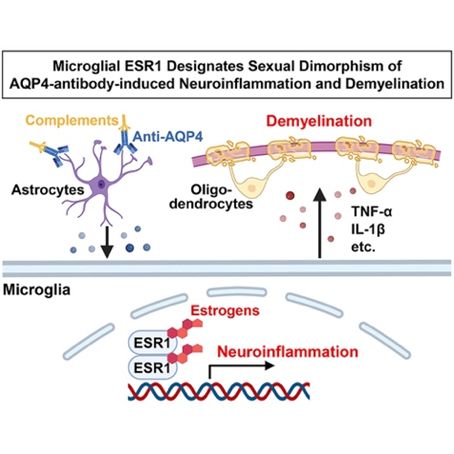
雌激素信号主要通过雌激素受体1(Esr1,又称ERα)和雌激素受体2(Esr2,又称ERβ)介导。单细胞测序数据显示,雌性小鼠小胶质细胞中 Esr1表达水平显著高于雄性,而Esr2及雄激素受体则无明显性别差异。进一步利用小胶质细胞特异性Esr1敲除小鼠(Cx3cr1CreER; Esr1flox/flox)证实,小胶质细胞中的Esr1信号通路介导了NMOSD模型中神经免疫及脱髓鞘反应的性别二态性。值得注意的是,FDA批准的乳腺癌药物氟维司群(ESR1拮抗剂)可显著缓解模型小鼠的病理损伤,为该疾病的临床转化治疗提供了新路径。
外周组织:肝纤维化中雌激素的保护作用
在外周组织层面,杨竞教授的研究进一步揭示了性激素调控非免疫细胞参与免疫反应的机制。以肝纤维化为例,绝经前女性发病率和病变程度通常低于男性,而绝经后则迅速加重。杨竞教授团队使用蛋氨酸-胆碱缺乏的特殊饮食(Methionine-Choline Deficient diet, MCD)构建小鼠肝纤维化模型,并在雌鼠及雄鼠模型中分别使用性腺切除术及性激素补充方案以探究肝纤维化性别二态性的性激素调控功能。研究发现,雌鼠中卵巢切除后明显加重肝纤维化病变,而雄鼠中睾丸切除术后外源性补充雌激素可明显缓解肝纤维化进程。
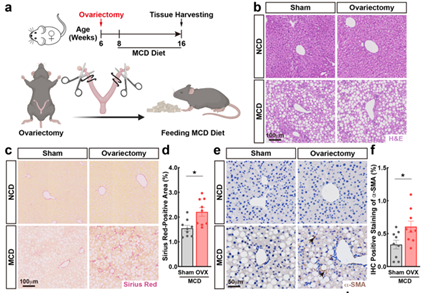
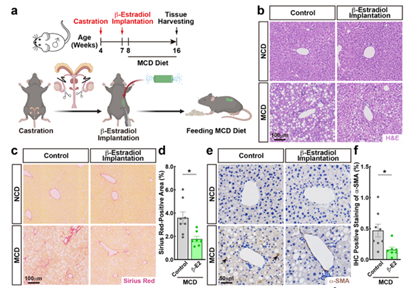
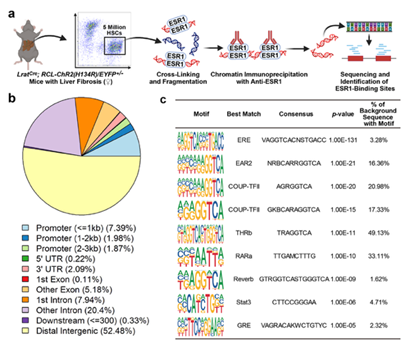
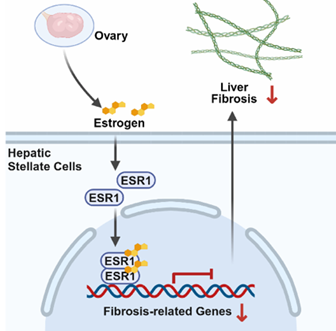
进一步研究发现人类与小鼠肝星状细胞(Hepatic Stellate Cells, HSC)中特异性表达Esr1,介导调控雌激素相关肝纤维化的性别二态性。雌激素通过ESR1直接抑制HSC中纤维化相关基因的表达,从而抑制肝纤维化进展。这一发现揭示了雌激素在外周组织器官中作为抑制因子的角色,与其在中枢神经系统中的促炎作用形成鲜明对比。
屏障组织:过敏性哮喘中雄激素通过交感神经发挥保护作用
针对呼吸道等屏障结构,杨竞教授阐述了局部神经免疫环路中性别二态性的精细调控机制。临床研究显示,过敏性哮喘在青春期后表现出明显的男性保护效应。利用屋尘螨构建的小鼠哮喘模型中,雌性小鼠呈现更严重的气道炎症反应,伴随哮喘相关炎性因子IL-5和IL-13表达升高。性腺切除术未影响雌性小鼠的哮喘表型,却特异性加重了雄性小鼠的气道炎症反应。进一步机制研究表明,雄激素通过其受体(Androgen Receptor, AR)直接促进肺部交感神经的物理生长与投射;交感神经末梢释放的去甲肾上腺素作用于2型天然淋巴细胞(Innate Lymphoid Cell 2, ILC2)上的β2肾上腺素受体,抑制致炎因子IL-5和IL-13的产生,从而形成抗炎屏障。
综上所述,神经免疫交互在不同解剖部位展现出截然不同的性别依赖性,这种对局部环路的精细解析为性别差异化治疗奠定了科学基础。
报告最后,听众对报告内容进行了深入友好讨论,问题主要包括针对交感神经在哮喘中保护性作用的功能性研究及针对性别二态性相关疾病的临床差异化治疗等,杨竞教授对以上问题分别进行详细解答。
撰稿人:石一星