Tony Wyss-Coray:年轻血液助大脑“返老还童”?

讲者 | Tony Wyss-Coray 斯坦福大学神经病学和神经科学教授
听译 | 袁雅宁
文字内容仅供参考,详情请见讲座原视频:https://oir.nih.gov/wals/2020-2021/young-blood-old-brains
本文发布已得到讲座主持人(Dr. Chuan Wu, National Institutes of Health, NIH)授权,未经许可请勿转载。
我们实验室的研究兴趣在于理解大脑是如何衰老的,以及该过程中大脑如何变得更易受认知功能障碍、神经变性以及阿尔茨海默病(Alzheimer’s disease, AD)等疾病的影响。当前,这是一个全球性问题,人类非常幸运地享受着日益提高的医疗和营养水平,平均寿命不断增加,然而越来越多与年龄相关的疾病问题也随之而来。老年疾病最残酷的一面在于,病人一旦开始丧失认知功能,他们将逐渐忘记身边所有人,忘记生命中所做过的一切。
影响生物体生理功能的决定性因素
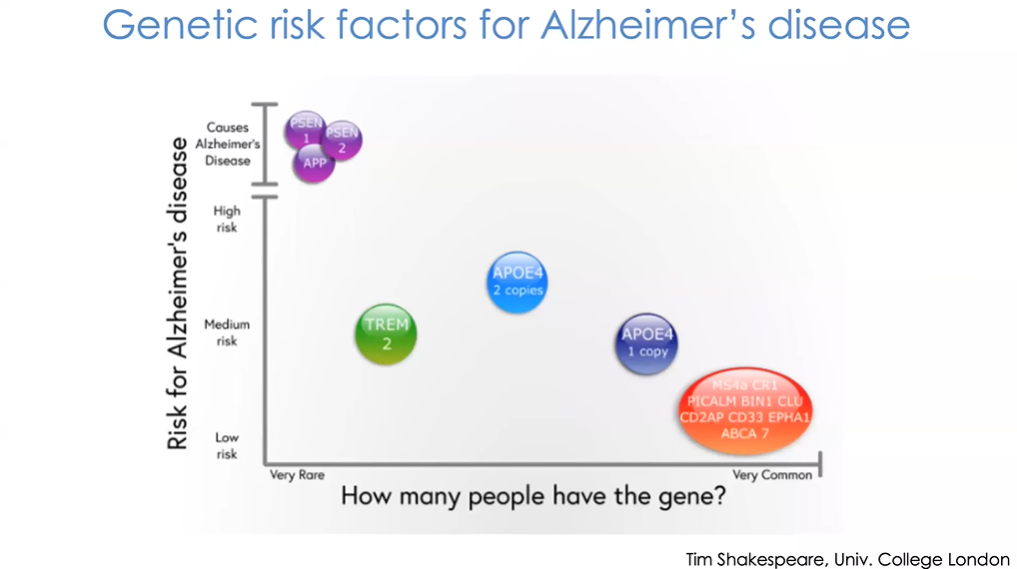
图1 阿尔茨海默病遗传风险因子
图1展示的是一个阿尔茨海默病遗传学示例,也同样适用于其他疾病类型。目前,我们掌握了一些会影响个体对某些疾病(如阿尔茨海默病等)易感性的遗传信息。已知导致显性遗传性阿尔茨海默病的突变非常罕见,具有该突变的人群可能在20、30、40岁就会开始发病。此外,先前的研究也证实,还有许多较弱的遗传因素也会增加或降低患病风险。
APOE基因就与阿尔茨海默病之间存在关联性,个体如果具有2个数量的APOE,其65岁时患病的风险将增加约12倍。然而,就阿尔茨海默病而言,真正容易被忽视的关键致病因素其实是年龄。无家族遗传史的散发性阿尔茨海默病患者占总患病人数的99.5%甚至更高,其最主要的风险因素显然是个体年龄的增长。因此,想要应对此类疾病,我们首先需要理解衰老问题。
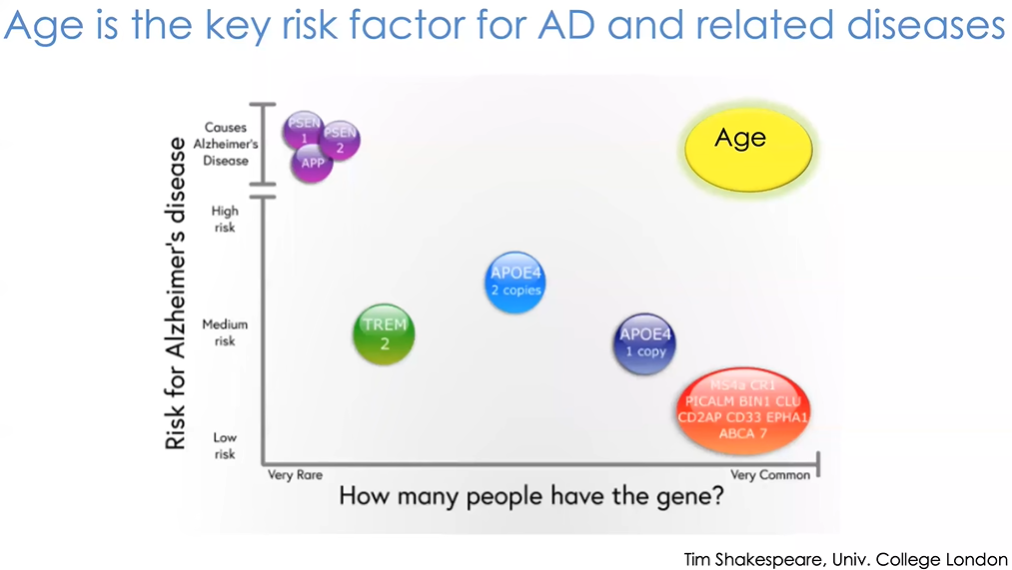
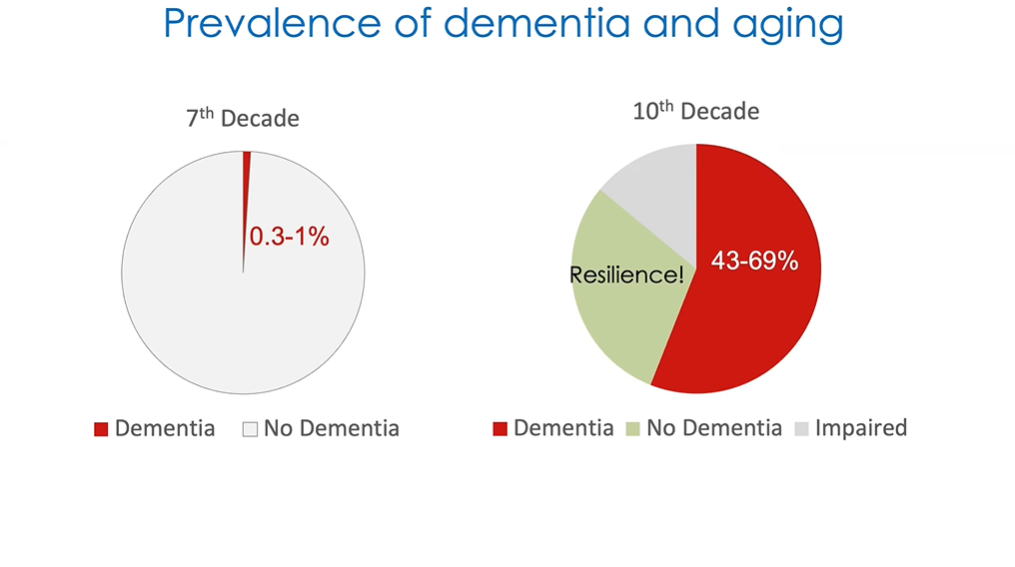
图2 痴呆症患病率与年龄
图2展示了另一个例子。目前大多数发生在老年群体中的痴呆症均为阿尔茨海默型,但此处展示的并非特指阿尔茨海默病,而是广泛意义上的认知功能下降和痴呆。可以看到在70岁的受试者中,出现痴呆的比例最高为1%;到100岁该比例大幅上升,有至少一半人都出现了痴呆症状。而从研究的视角看,却有另一个非常有趣的发现,那就是研究中约有三分之一的百岁老人仍拥有完好的认知功能,他们的表现与50岁甚至更年轻的人群无异。由此可见,人类的大脑功能是有可能持续到生命晚期,甚至直到生命尽头的。
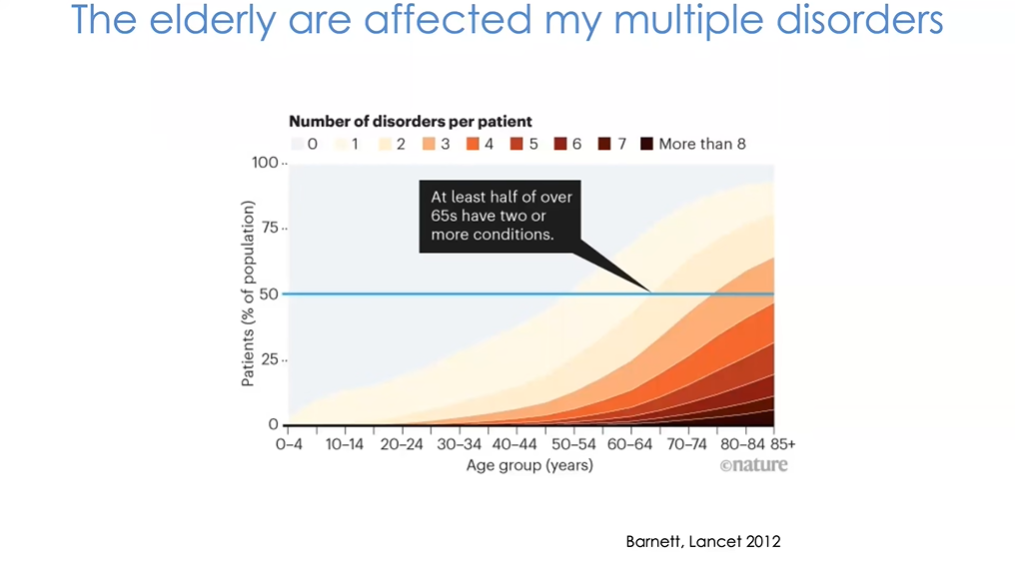
图3 随着年龄的增长,人们所患的老年疾病也会逐渐增加
然而人体器官中不仅仅只有大脑会受到年龄的影响。研究表明,随着年龄的增长,人们所患的老年疾病也会越来越多。图3中的每种颜色代表了个体所患疾病的数量,研究显示65岁左右人群中约有一半人患有两种老年疾病;随着年龄的增长,患有多种老年疾病的人数也在持续增加。这一结果引发了领域内许多研究者对此类疾病——如心血管疾病、关节炎、癌症(许多癌症与年龄相关)、神经退行性疾病等——治疗思路的讨论:单独治疗某一种老年疾病是否有意义?是否能够针对衰老过程本身进行研究,从分子和细胞层面理解衰老机制?是否能够像人们常说的“返老还童”一样,减缓甚至逆转衰老过程,进而从根本上一次性解决老年疾病问题,而非逐个击破?(图4)
图4 大脑能否“返老还童”?
年轻血液助小鼠“返老还童”

图5 研究者可以通过年龄相关干预措施对衰老动物进行治疗,以减缓其衰老过程、延长寿命,甚至在分子功能或细胞水平上逆转衰老。
就我个人来看,至少在动物模型,特别是那些采取多种不同干预方法的模型中,“返老还童”并非痴人说梦。不同水平的生物学研究已经表明,研究者可以通过年龄相关干预措施对衰老动物进行治疗,以减缓其衰老过程、延长寿命,甚至在分子功能或细胞水平上逆转衰老。其中一些措施包括代谢干预(热量限制、运动、小分子)、衰老细胞清除,以及近年来非常热门的衰老细胞表观遗传重编程(Transient Epigenetic Reprogramming)——通过尝试移除细胞中加速衰老的表观遗传标记和DNA来延缓衰老。而我们一直以来重点关注的是年轻血液与脑脊液对于减缓或逆转衰老的作用。在近期发布的成果中,我们通过向年老小鼠输入年轻小鼠的脑脊液,改善了其大脑功能,在多种水平上使其年轻化。
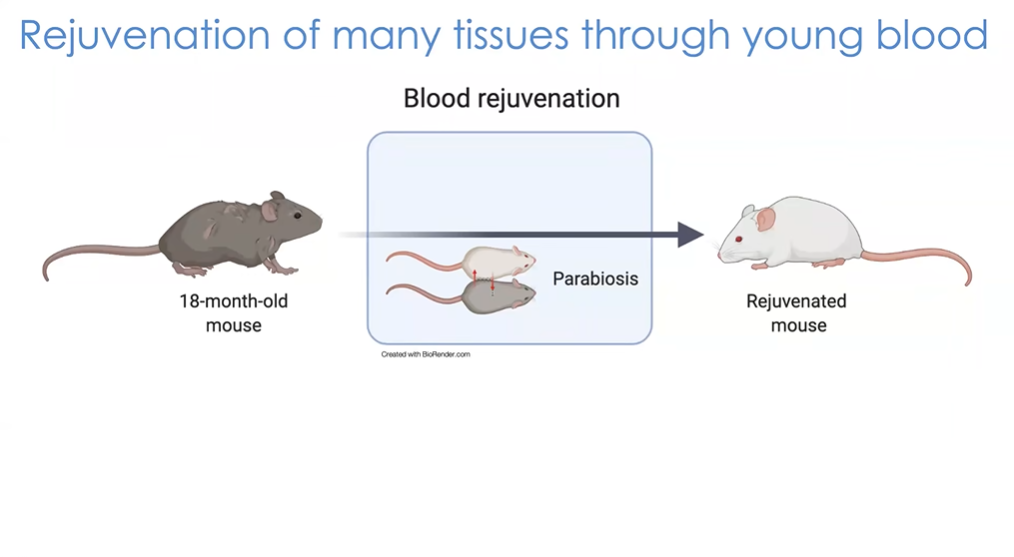
图6 小鼠“异体共生(parabiosis)”模型
该领域突破性发现依赖的最主要模型之一是由Thomas Rando提出的。他目前就职于加州大学洛杉矶分校干细胞研究中心,对于肌肉衰老,特别是肌肉干细胞衰老具有浓厚兴趣。他关注的问题在于:干细胞的衰老是由细胞内在机制还是外在环境导致的?针对这一问题,他采用了一种被称为“异体共生(parabiosis)”的早期实验范式。实验通过外科手术的方式将两只动物的循环系统进行连接,从而实现二者之间的血液互换。共生实验中连接的两只动物不一定存在年龄差异,即所谓的“异时性”,而可以是小鼠基因模型的任意不同组合,比如同为年轻小鼠或同为年老小鼠。这一模型在免疫细胞迁移等免疫学相关研究中已得到充分应用。
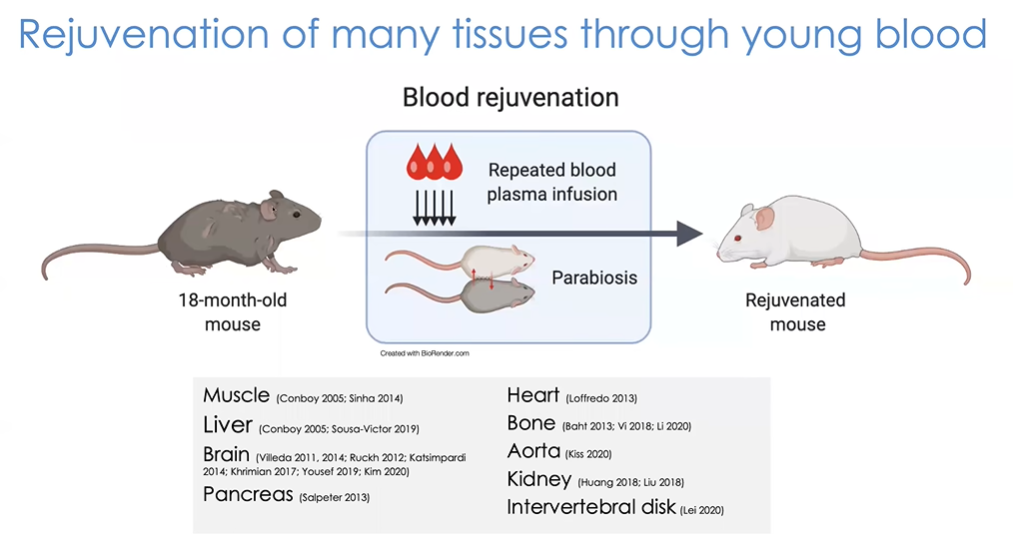
图7 研究表明年轻血液可使小鼠体内多种组织恢复活力
在加州大学伯克利分校科学家Irina和Michael Conboy 2005年的开创性研究中,Thomas所做的工作表明年老小鼠的肌肉干细胞可以再生和恢复,进而生成与年轻小鼠非常相似的全新肌肉组织。这是一个极具突破性的进展,此后很多研究都证实其结果在其他多种组织中均成立(图7)。Thomas在肝脏中也发现了类似的再生效果,并且发现了大脑中细胞的增殖。这正是他与我们实验室合作的开始。
在相关研究中,异体共生确实是一种有效的实验范式,但我们也可以通过从年轻或年老小鼠身上采集血液,或提取血液中的液体成分即血浆,然后进行反复输注来复制这些效果(图7)。

图8 Saul Villeda等团队研究明确了年轻血液对年老小鼠大脑功能的积极作用(Villeda 2011, Villeda 2014; Ruckh 2012; Katsimpardi 2014; Khrimian 2017; Yousef 2019; Kim 2020)
这位是加州大学旧金山分校副教授Saul Villeda(图8)。他所做的工作证实了我们确实能够从年轻小鼠身上采集血浆,并通过在几周内输入年老小鼠体内来实现类似效果。实验中他每3天或3周向小鼠注射总血量5%的血浆,结果显示小鼠大脑中的干细胞活性增强,与学习和记忆相关的突触可塑性增加,此外大脑炎症也得到了减轻。这或许解释了年轻血液环境影响衰老的关键机制。最重要的是,在功能层面上年老小鼠的记忆力得到了改善。
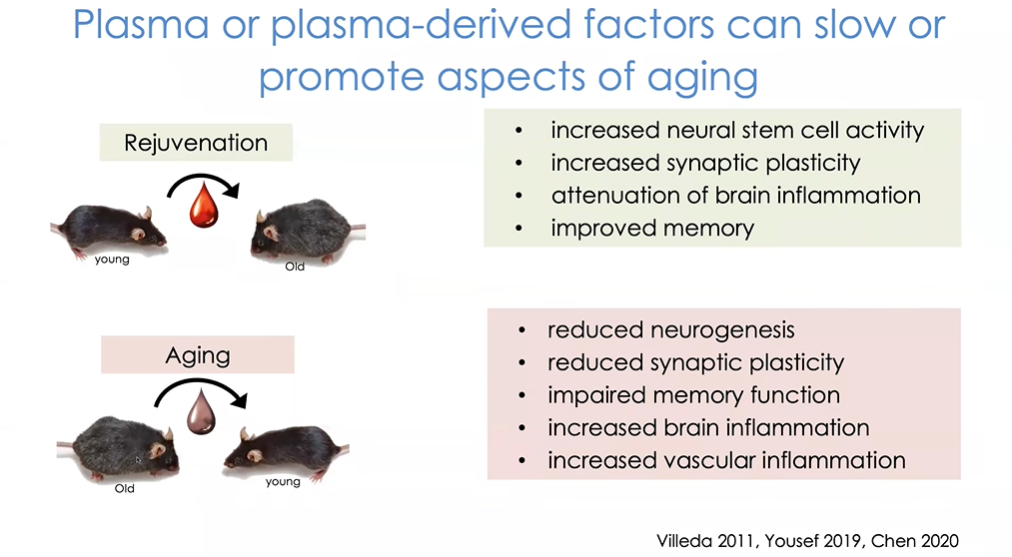
图9 异体共生不仅可以实现“返老还童”,同样也可以加速衰老过程
同时,Saul也首次证明异体共生不仅可以实现“返老还童”,同样也可以加速衰老过程(图9)。反复输注年老小鼠血浆或暴露于共生模型中的年轻小鼠,具有较少的神经发生,因此产生的新神经元更少;其突触可塑性下降,记忆功能减退,血管等炎症增多。这些表现或许能够解释大脑连接以及其如何对系统环境做出反应。
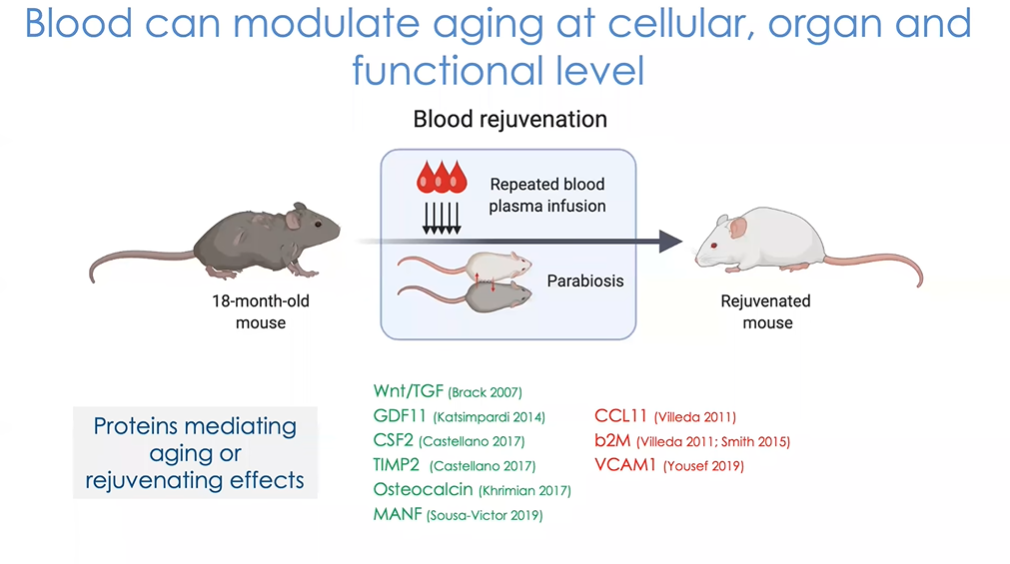
图10 血液能够在细胞、器官及功能水平上调节衰老
目前几个课题组已经发现了一些可能发挥作用的因子,但据我所知数量并不多,这里简单列举了一些有利和不利因子(图10)。不同细胞可能以有益或有害的方式对不同蛋白质做出反应,约有几十甚至上百种蛋白质参与其中,找出其中的关键成分将会是非常有趣的过程。
血液疗法在人类疾病治疗中的潜力
在大自然创造的所有化合物中,我认为血液是最强效的。想要利用各种因子合成血浆非常复杂,然而血浆是可输注的。全球每天会发生成千上万次输血,用于在外科手术中挽救因事故等原因失血过多的患者。此外输血也可以用于疾病治疗,比如特定蛋白质缺乏或过多的患者,都可能接受血浆置换疗法。
因此我们成立了Alkahest公司,公司近期已由Grifols收购。像Grifols这样的公司是做什么的呢?他们每天都会采集大量血浆,产出满足临床需求的不同成分。
目前我们在Alkahest进行了一系列临床试验,我们收治轻度认知障碍或早期阿尔茨海默病患者,给他们注射来自年轻献血者的血浆成分。这些实验仅用于概念验证性的安全性与剂量研究,但已经在阿尔茨海默病和帕金森病的治疗中展现出前景。
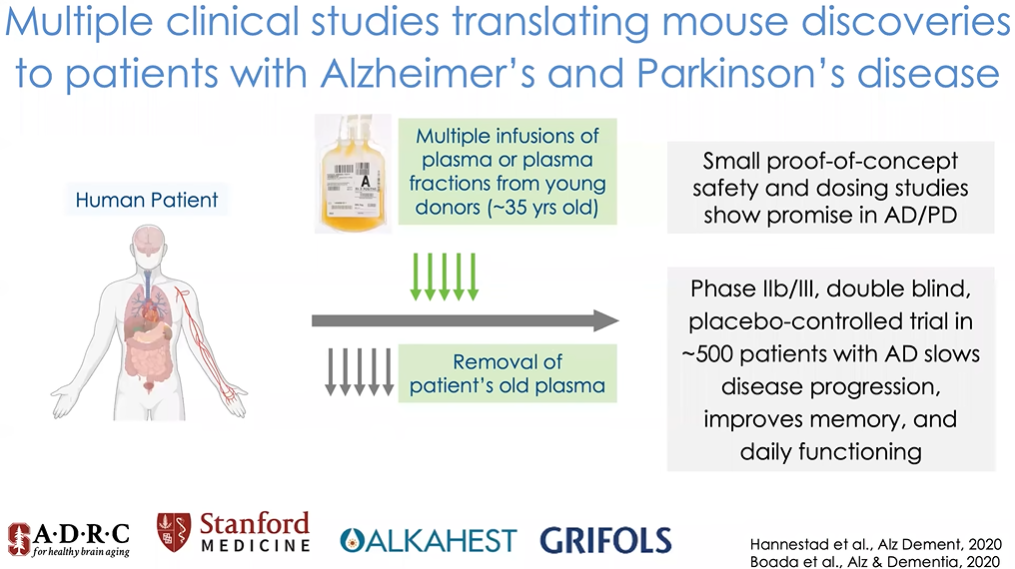
图11 血液疗法在阿尔茨海默病及帕金森病治疗中的探索
随后Grifols在研究中引入了血浆置换(图11),他们首先从阿尔茨海默病患者体内抽取出原有血浆,然后再向其输注正常血浆(正常血浆的献血者平均年龄为35岁)。Grifols在500名患者中进行了Ⅱb/Ⅲ期双盲安慰剂对照实验,实验结果显示患者的疾病进展减缓,记忆力与日常生活功能得到改善。这表明我们在小鼠身上实现的效果是有可能作用于人类患者的。当然现在要得出这个结论还为时尚早,目前许多课题组已经开始通过对人类的对照研究来进行验证。这个是一个非常激动人心的趋势。
年轻血液如何逆转衰老
那么“返老还童”具体是如何实现的呢?我们第一次提出这些观点的时候,人们都会用怀疑的眼光看着我:“怎么可能有这种好事?”,或者觉得我们是那种从事疯狂实验的科学怪人。既然人体中存在能够阻止血液因子进入大脑的血脑屏障,那么利用血液让大脑“回春”要如何实现?公众存在这些质疑非常正常,因为相比血液置换带来的惊人效果,这整个过程看起来确实过于简单了。
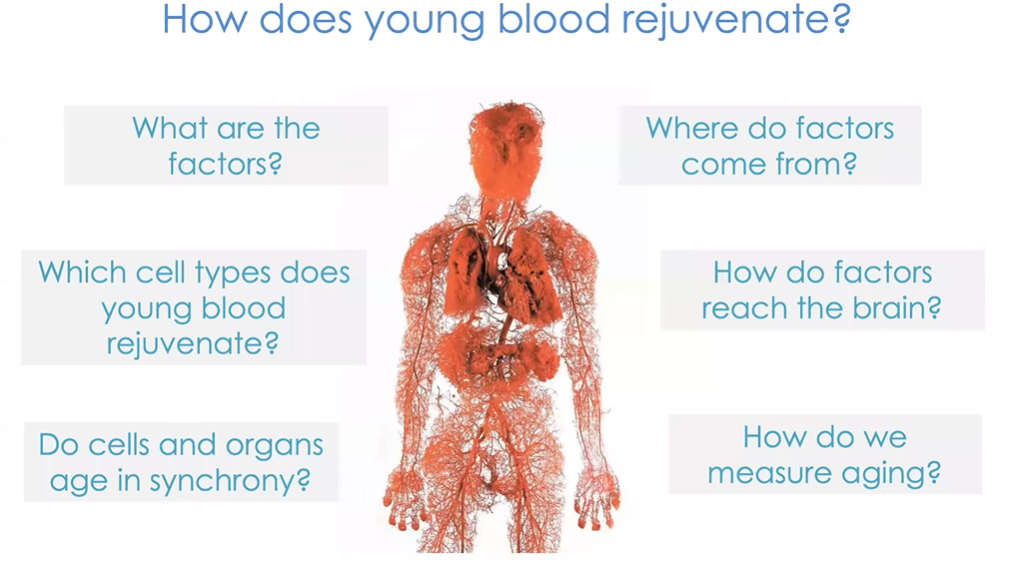
图12 有关血液疗法的常见问题:影响衰老过程的因子有哪些?这些因子从何而来?身体中哪些细胞会产生有益或有害因子?血液会逆转或加速哪些细胞类型的衰老?这些因子要如何在大脑中内皮细胞层的阻隔下触达大脑组织?细胞和器官是同步老化的吗?如何衡量衰老?
那么影响衰老过程的因子有哪些?这些因子从何而来?身体中哪些细胞会产生有益或有害因子?血液会逆转或加速哪些细胞类型的衰老?这些因子要如何在大脑中内皮细胞层的阻隔下触达大脑组织?细胞和器官是同步老化的吗?这些问题既与衰老过程本身有关,也与我们如何衡量衰老有关。这里我特别强调这个问题,是因为如果我们在动物实验中取得的发现能够用于干预人类衰老过程,那么我们就需要能够测量出人的相对年龄,而非出生证明上显示的实际年龄,这样才能知道身体相对实际年龄的衰老速度。

图13 Nick Schaum和Steve Quake
接下来我会简单阐述其中几个问题。为了明确这些因子从何而来,当时实验室的研究生Nick Schaum采取了一种比较原始的办法。想要知道这些参与逆转或加速衰老的蛋白质来自何处,一种方法就是观察身体不同器官的基因表达谱(gene expression profile)。很幸运的是我们得到了Steve Quake的帮助,他在核酸检测领域具有开创性贡献,他创办的公司及开发的检测方法能够实现规模化的核酸检测。Steve当时担任陈-扎克伯格生物中心(Chan Zuckerberg Biohub)联合主任,他的实验室致力于开发单细胞RNA测序方法。他对我们的研究非常感兴趣,他建议我们放弃预想的Bulk测序,直接采用单细胞RNA测序。
随后我们在斯坦福招募了十几个实验室,总人数至少有一百人。我们用了5周的时间处理小鼠,然后把组织分配给各实验室进行处理。我们对其进行了测序,得到了一些非常有价值的资源,比如Tabula Muris数据库,其中收集了小鼠主要组织及细胞类型的基因表达数据。同时我们记录了小鼠转录组随其年龄的变化情况。我们同时结合了Bulk测序和单细胞测序,Bulk测序提供统计功效,单细胞测序提供分辨率。
我们与许多生物信息学者和计算机专家进行了卓有成效的合作,得到了非常激动人心的新发现。其中一个重要发现是:生物体的衰老过程开始得很早。这并不是一个全新的发现,但却是首次通过实验实现规模化证明。这是一个非线性过程。我们可以监测到在什么年龄能够开始看到基因表达的显著变化。
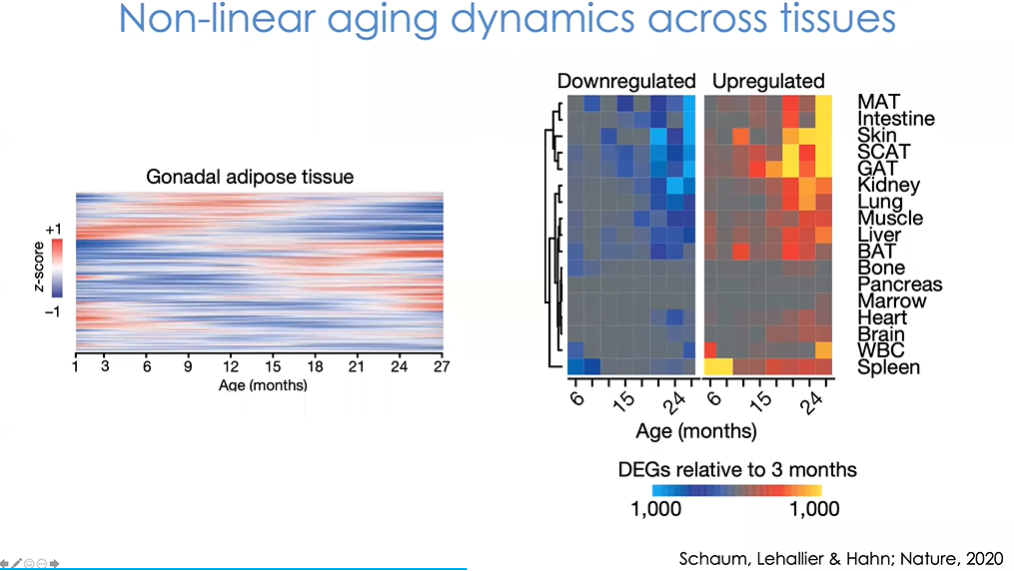
图14 在12-15个月龄左右,多数组织的基因表达开始出现显著变化,特定基因型出现上调或者下调。同时也能够看到哪些细胞类型率先出现与年龄相关的变化,这证明了在组织和细胞水平上衰老是一个异步过程。
观察所有主要组织,我们能够看到在12-15个月龄左右,多数组织的基因表达开始出现显著变化,特定基因型出现上调或者下调(图14)。图中展示了这些基因,同时也能够看到哪些细胞类型率先出现与年龄相关的变化,这证明了在组织和细胞水平上衰老是一个异步过程。这就意味着我们无法判断一个生物体是加速还是减速老化,而只能判断该生物体中的哪些组织和细胞发生了加速或减速老化,因为这不是一个同步进程,它们都有自己的轨迹。换句话说,并不是所有组织和细胞类型都会同时开始衰老。这也有力地反驳了认为年龄是DNA一部分的观点。最有可能的解释是,这是一个随机的过程,会受生物体所处环境影响。这与对秀丽隐杆线虫、苍蝇及图中列举的其他生物研究结果相一致(图15)。

图15 其他生物体研究成果
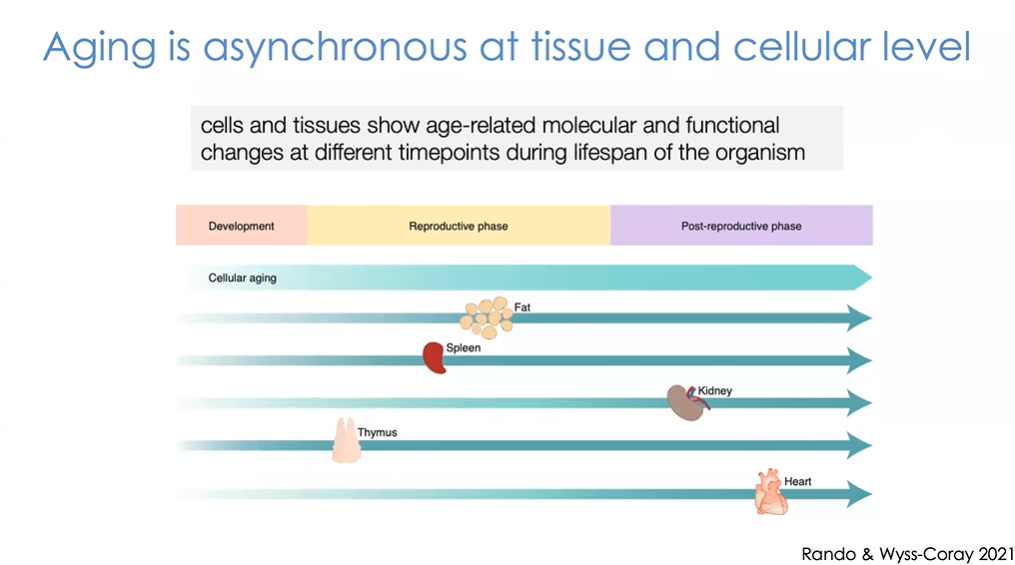
图16 部分细胞和特定转录物较早发生变化。其中最早出现的应该是胸腺,随后是脾脏、脂肪组织和其他组织。
我们可以观察到率先出现年龄相关变化的组织(图16)。一些细胞和特定转录物较早发生变化,而其中最早出现的应该是胸腺,紧接着是脾脏、脂肪组织和其他组织。这些结果是实实在在基于数据得出的,通过数据我们可以明确哪一个组织发生了老化,并采取针对性干预手段。
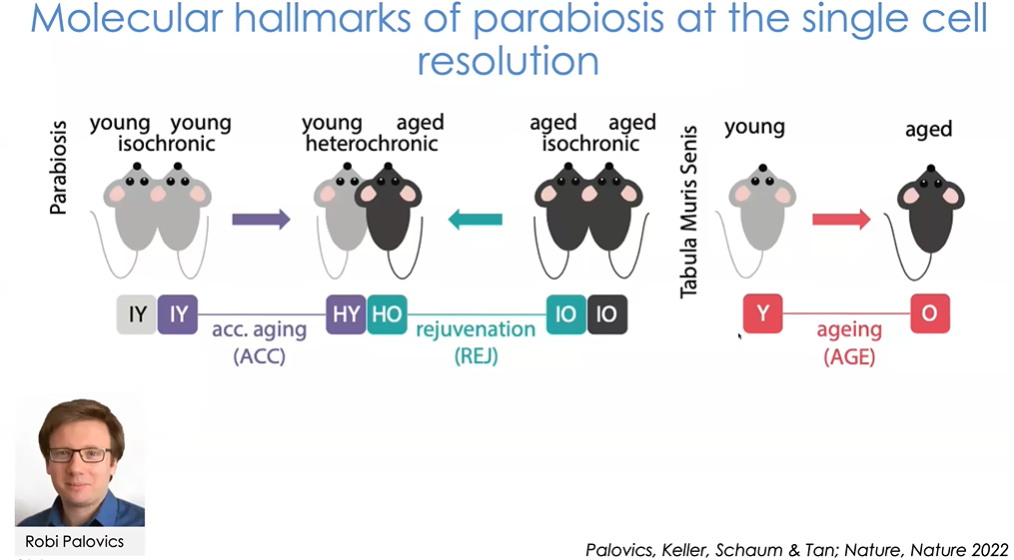
图17 Robi Palovics:共生模型中参与循环的因子对哪些细胞产生了影响?
实验中另的一个重要问题是:共生模型中参与循环的因子对哪些细胞产生了影响?解答这一问题的相关工作由Robi Palovics牵头(图17),Robi是一名优秀的计算机科学家,对生物学也具有浓厚兴趣。他通过创造性的数据挖掘方法,将这项研究带向了一个新高度。
在异体共生模型中,我们既有“异时共生”的年轻-年老小鼠对,也有“同时共生”对,即单独的年轻小鼠对和年老小鼠对;同时我们有Tabula Muris Senis数据库,其中包含正常小鼠整个生命周期所有主要组织和细胞类型的基因表达数据。我们的问题是:正常小鼠衰老过程与暴露在年老血液环境中的年轻小鼠衰老过程有何不同(图中我们将加速衰老标记为紫色)?暴露在年轻血液环境中的年老小鼠体内哪些组织和细胞发生了变化?我们需要关注哪些基因与正常衰老显示出相同的轨迹,即加速衰老;哪些表现出相反的趋势,即我们所说的“返老还童”。当然,这只是研究衰老过程的其中一种方式。
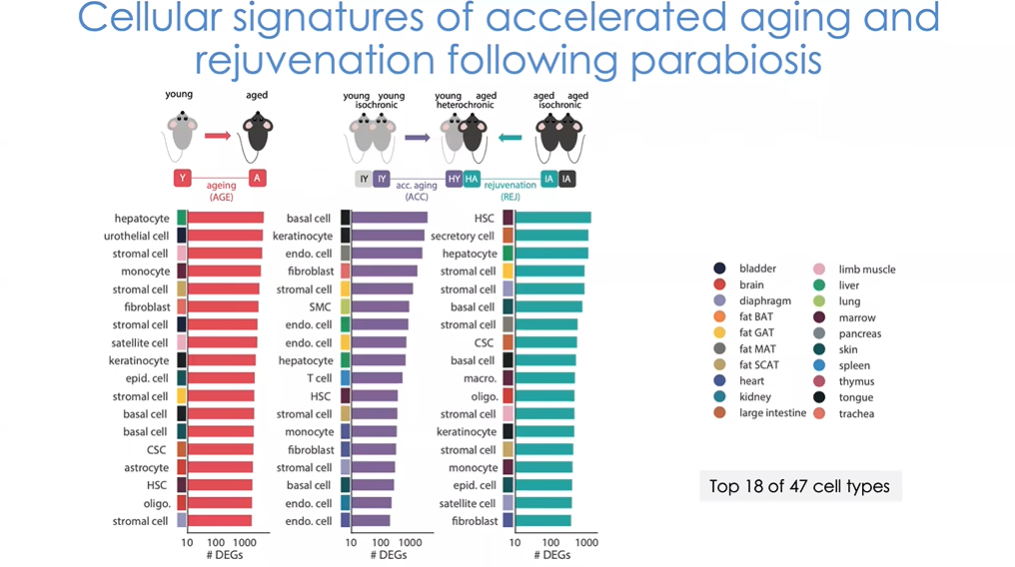
图18 加速衰老共生模型中小鼠细胞变化情况
首先我们来看这张细胞列表(图18),表中展示的是我们分析的47种细胞类型中的前18种。未来我们希望在分析中引入更多的细胞和动物类型,但当时的算力仅限于此。从3月龄至18月龄,有时可至24月龄,小鼠体内几乎所有细胞的基因表达都会随年龄而发生变化。那么在加速衰老模型中,哪些细胞表现出了和暴露在年老血液环境下的年轻小鼠相同的衰老轨迹?我们依据此对细胞进行了排名,可以看出对年老血液环境反应最明显的细胞包括不同组织中的内皮细胞、角化细胞、基底细胞以及一些干细胞,如基质细胞、平滑肌细胞等。
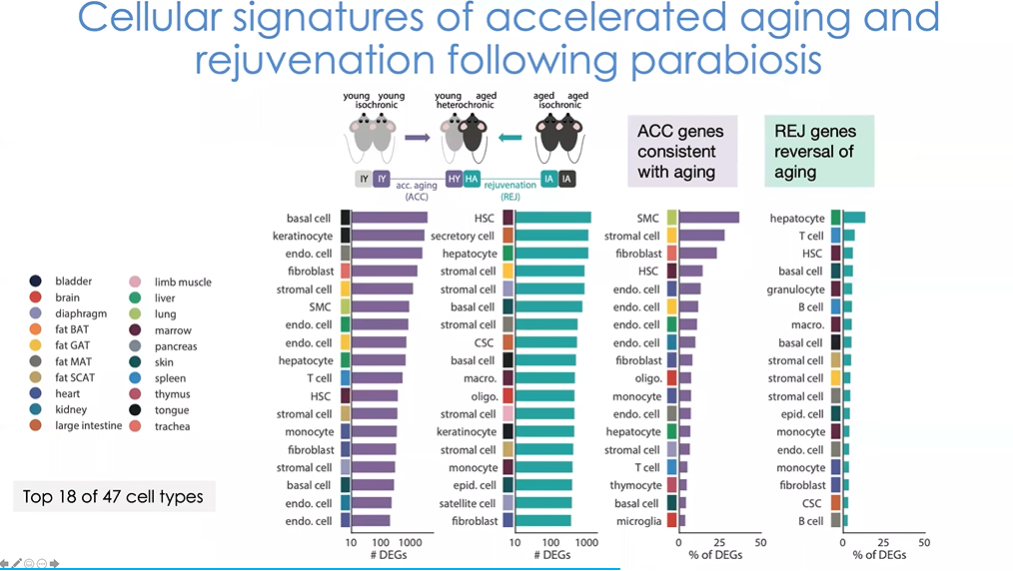
图19 逆转衰老共生模型中小鼠细胞变化情况
接下来我们看在逆转衰老模型中,哪些随年龄变化的基因发生了逆转(图19)。居首位的是造血干细胞,这一结果对免疫学者们而言尤为激动人心。实验中我们将老年小鼠暴露于年轻小鼠的血液环境中,结果表明小鼠体内干细胞对其所处环境高度敏感。同时我们也注意到肝细胞以及一些干细胞如基质细胞等,也表现出较强的反应。
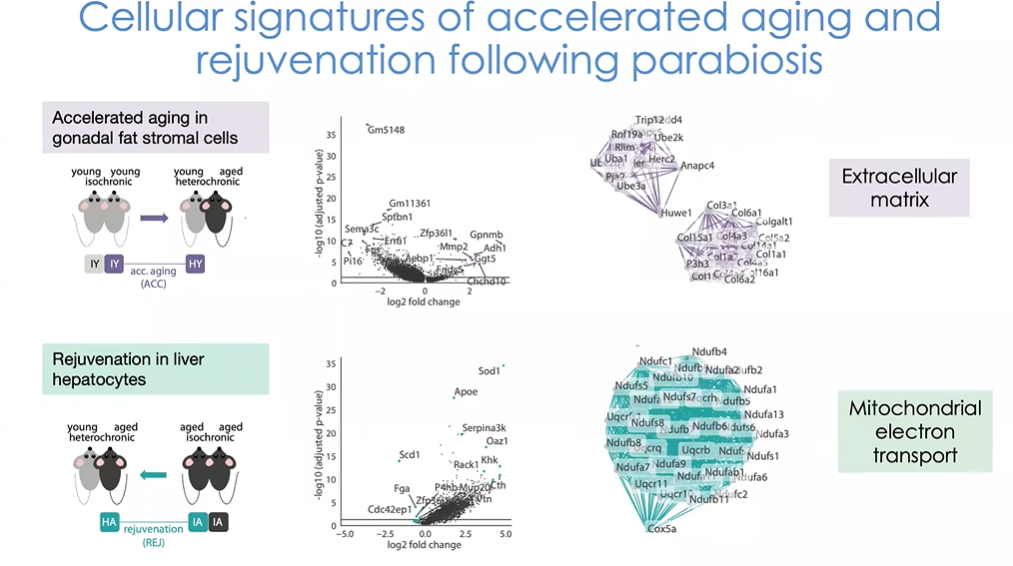
图20 共生模型中细胞外基质及线粒体基因或参与线粒体功能和电子传递的基因变化情况
细胞外基质随年龄的变化是衰老研究领域的一个共同课题。观察逆转衰老模型,我们能看出肝细胞是高度敏感的(图20)。有趣的是,线粒体基因或参与线粒体功能和电子传递的基因也对逆转环境有较强的响应,并且似乎对我们观察到的逆转起到了一定作用,这一发现与衰老研究领域的其他文献一致。
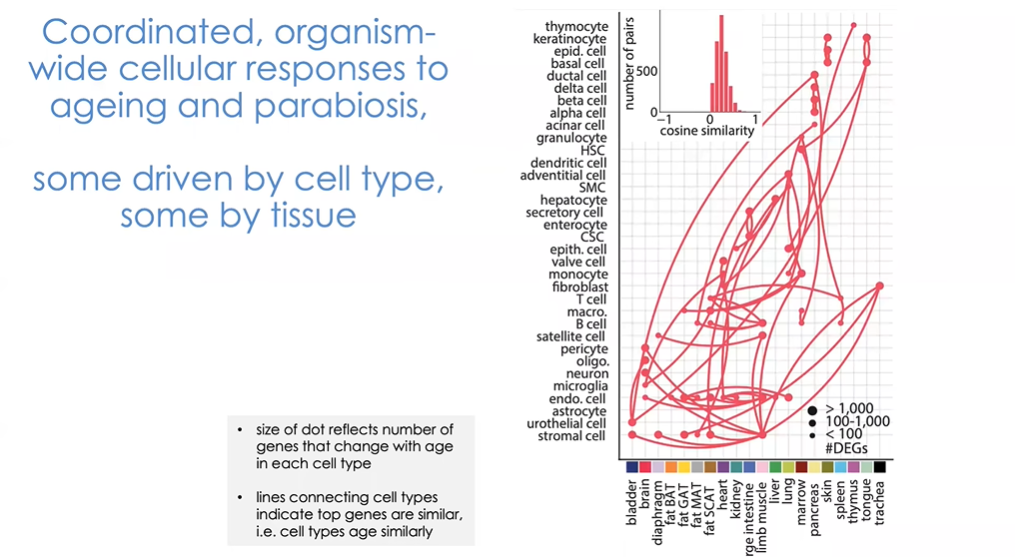
图21 一个更有趣的视角是从整个生物体的角度来看,在共生模型中,整个生物体对衰老过程是否存在整体的细胞反应?
一个更有趣的视角是从整个生物体的角度来看,在共生模型中,整个生物体对衰老过程是否存在整体的细胞反应?图21中的图表由Robi制作,反映了正常的衰老过程。图中主要展示了我们目前已经研究过的细胞,反映出了很多有趣的信息。研究中我们分析不同细胞类型及其来源组织,图中点的大小反映了每种细胞类型中有多少基因随着年龄而变化。点之间的连线显示了随年龄变化的基因之间的相似性。小图中展示了随着细胞的衰老,基因表达的总体相似性。一些细胞显示出许多随年龄变化的相同基因。我们可以假设,如果两个不同细胞类型具有相同的基因随年龄改变,那么他们可能会对外部刺激做出反应,从而诱发这些与年龄相关的变化。这些变化之间密切相关,由遗传程序决定。对此我们还没有最终结论,但能够在如内皮细胞等细胞中观察到这种现象也十分有趣。
许多不同组织的内皮细胞在基因表达变化方面存在很多相似之处,最大可能是由血浆中的循环因子导致的,这些因子在多个组织的内皮细胞中触发相应程序,产生这些与年龄相关的变化。基质细胞也出现了类似的转录过程。随后我们会发现,在多种不同细胞类型中,比如皮肤角化细胞、表皮细胞、基底细胞等,它们的细胞特征明显不同,但是都具有相似的衰老过程。也许导致皮肤衰老的是细胞中的一些自体遗传性因素,这是我们仍需探索的问题。
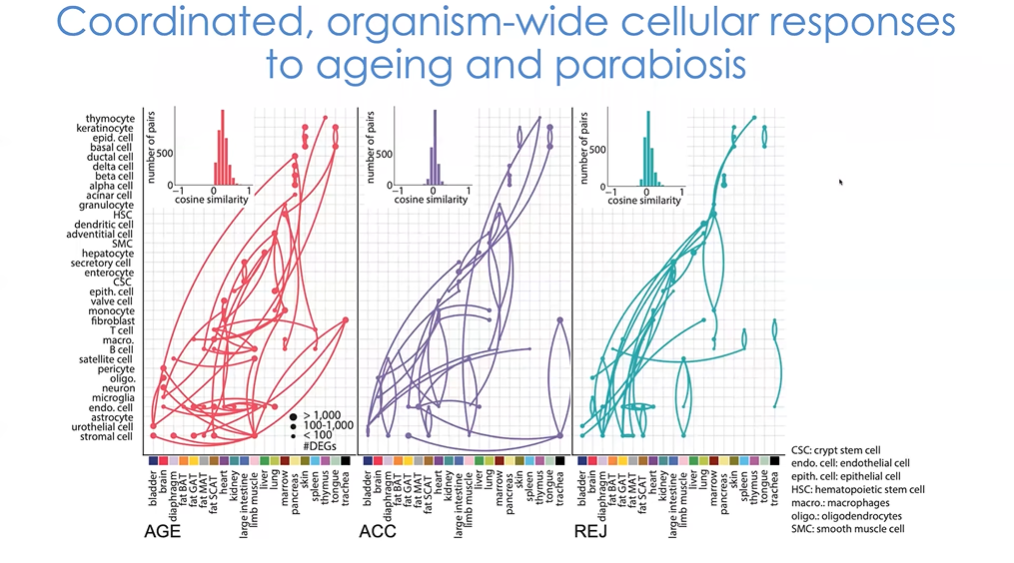
图22 正常衰老、加速衰老及逆转衰老模型细胞反应对比
我们可以在加速衰老和逆转衰老两个模型中同时进行观察(图22)。
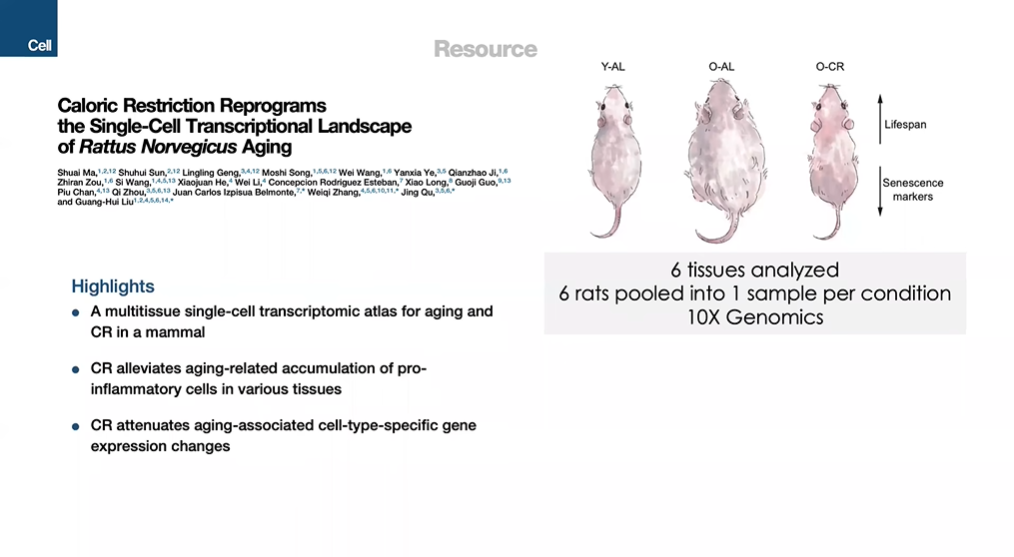
图23 Ma S, Sun S, Geng L, Song M, Wang W, Ye Y, Ji Q, Zou Z, Wang S, He X, Li W, Esteban CR, Long X, Guo G, Chan P, Zhou Q, Belmonte JCI, Zhang W, Qu J, Liu GH. Caloric Restriction Reprograms the Single-Cell Transcriptional Landscape of Rattus Norvegicus Aging. Cell. 2020 Mar 5;180(5):984-1001.e22.
目前已有研究者开始进行类似研究。例如在一项热量限制研究中(图23),研究人员分别设置自由进食和热量限制的大鼠或小鼠对照组,并在单细胞水平对其6种不同组织进行观察,实验结果显示单细胞转录组会以特定方式对以上进食干预做出反应。我们可以对不同干预措施进行对比,找出逆转或加速衰老的通用范式。我想未来我们将看到大量对不同实验范式进行整合的研究。
图24 血液连接生物体内所有器官,它的功能不仅仅是运输血细胞、免疫细胞和红细胞,同样也承担了细胞间交流的工作。
那么影响衰老的因素究竟有哪些?我们又如何来衡量衰老?我们可以通过研究血液的分子组成来解答这两个问题。血液连接生物体内所有器官,它的功能不仅仅是运输血细胞、免疫细胞和红细胞,同样也承担了细胞间交流的工作(图24)。因此我们也将其引入了衰老研究。
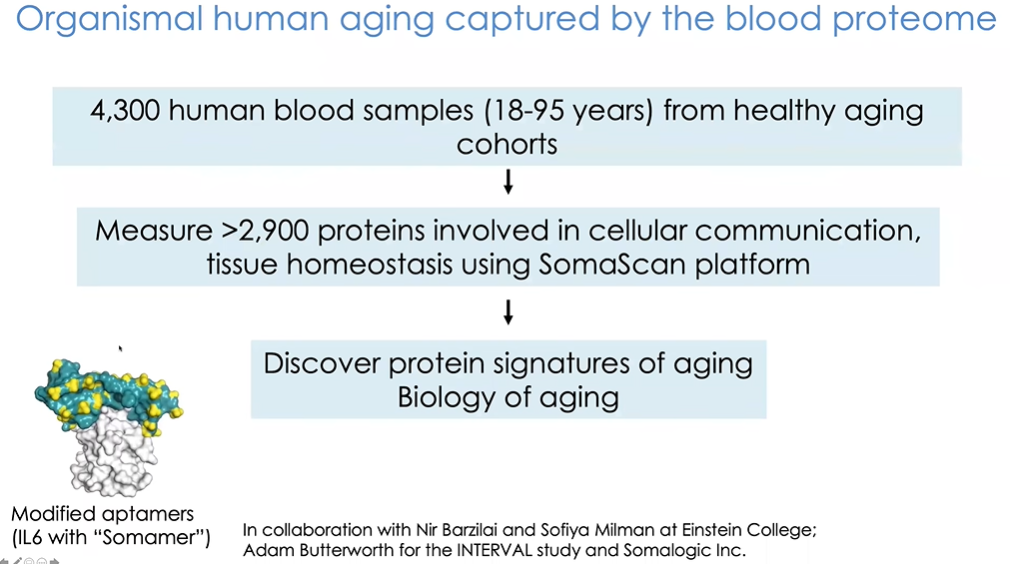
图25 对血液样本中的蛋白质进行测定
这里展示一个研究案例(图25)。该研究中我们通过INTERVAL项目以及与爱因斯坦医学院Nir Barzilai和Sofiya Milman的合作收集了4000多位受试者的血液样本,并借助SOMAscan平台对其中3000个蛋白质进行测定。SOMAscan利用经过特殊加工的核酸适配体(aptamers),能够对数千种蛋白的相对水平进行检测。
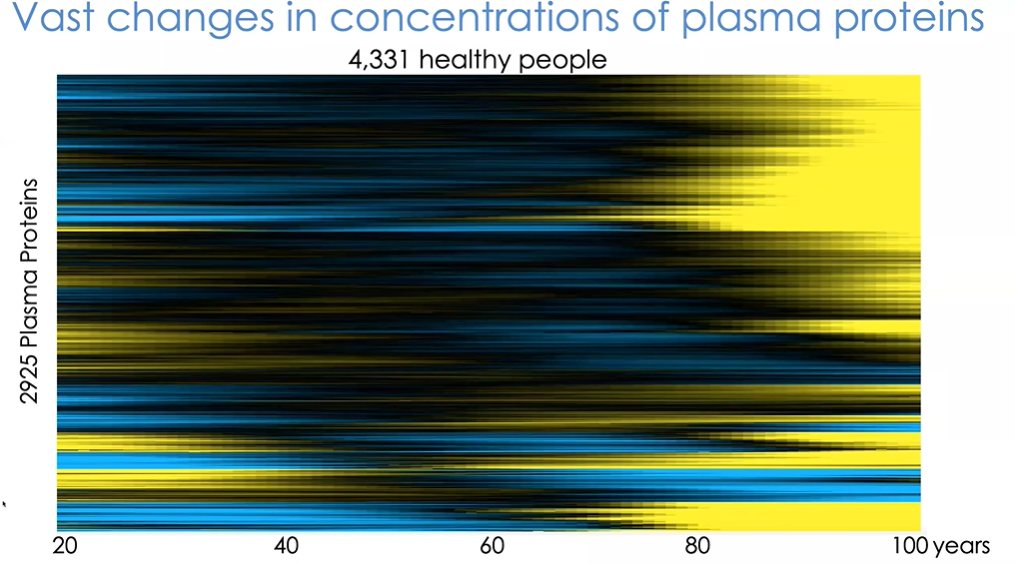
图26 随着年龄的增加,受试者的血液成分发生了惊人的变化
通过检测,我们能够在一定程度上可视化衰老过程中血液的变化。通过图26可以看出,随着年龄的增加,受试者的血液成分发生了惊人的变化,这或许可以解释共生模型和血液置换产生的效果,年老血液中的有害因子会对年轻个体造成有害影响,反之亦然。实验结果也很好地证明了衰老过程具有异步性,即人体中不同组织的衰老并非同时发生。接下来我们可以探究这些变化具体何时发生,以及在给定的不同年龄人群(如小于30岁和大于30岁)中蛋白质何时发生显著变化。
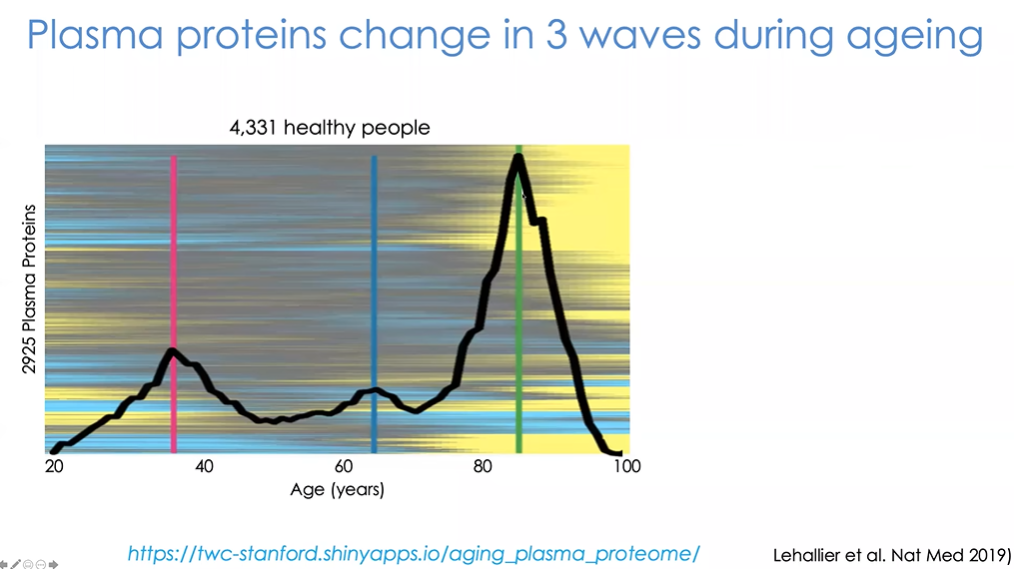
图27 “衰老波动(waves” of ageing)”
图27中我们标注出了所谓的“衰老波动(waves” of ageing)”。对比35岁以下和以上人群,约有400种蛋白质存在显著差异。随着年龄持续增长,蛋白质变化逐渐减少,直到65岁左右的出现另一个小高峰,到80岁左右呈现出最大变化。
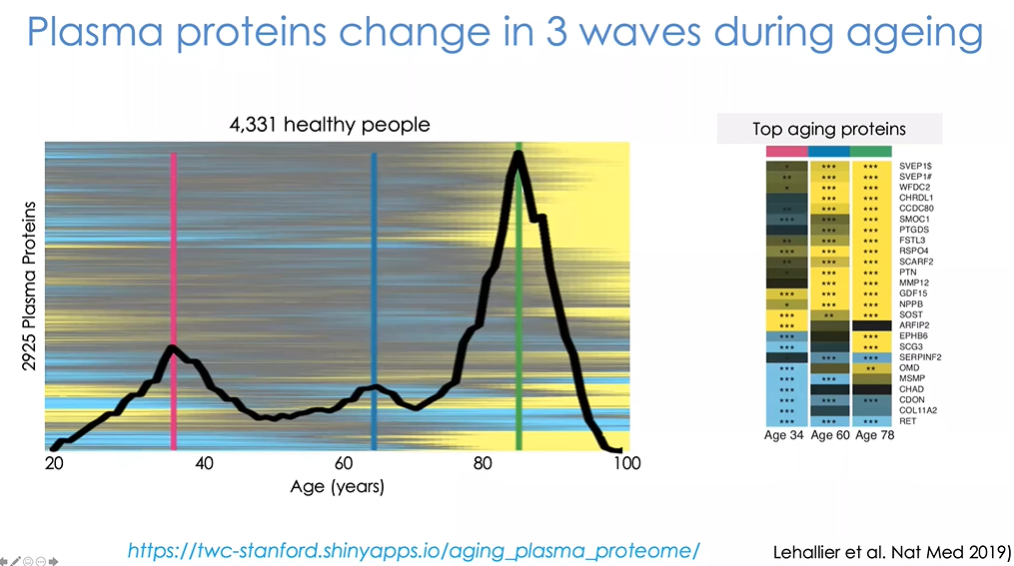
图28 波峰段具体的蛋白质种类,以及变化的显著程度
图28中具体展示了波峰段具体的蛋白质种类,以及哪些蛋白质变化最为显著。每处波峰都存在一些相同的蛋白质,而其他特有的蛋白质则可以帮助我们了解衰老的生物学原理。
图29 Hamilton Oh和Jarod Rutledge
最后,我想向大家展示利用这些信息我们还可以做些什么。这些蛋白质中包含了有关生物体生理状态的信息。由Hamilton Oh和Jarod Rutledge牵头的一系列研究目的在于探究我们是否能够通过观察血液中的蛋白成分来理解大脑衰老或大脑的生理状态(图29)。研究可行性在于,生物体血液中的一些蛋白质来源于大脑,因此如果我们能够识别这些蛋白质,我们就能在一定程度上解读大脑功能。当然,目前医院也能对血液中的特定蛋白进行检验,以确定胰岛素水平、滤过率等指标。但我们追求的是通过对数以千计的蛋白质进行大规模蛋白质组学分析,以将检测结果提高到一个全新的水平。通过观察具有组织特异性的特定蛋白质,我们可以推测其来源,同时观察它们是否能够反映其组织功能(图30)。
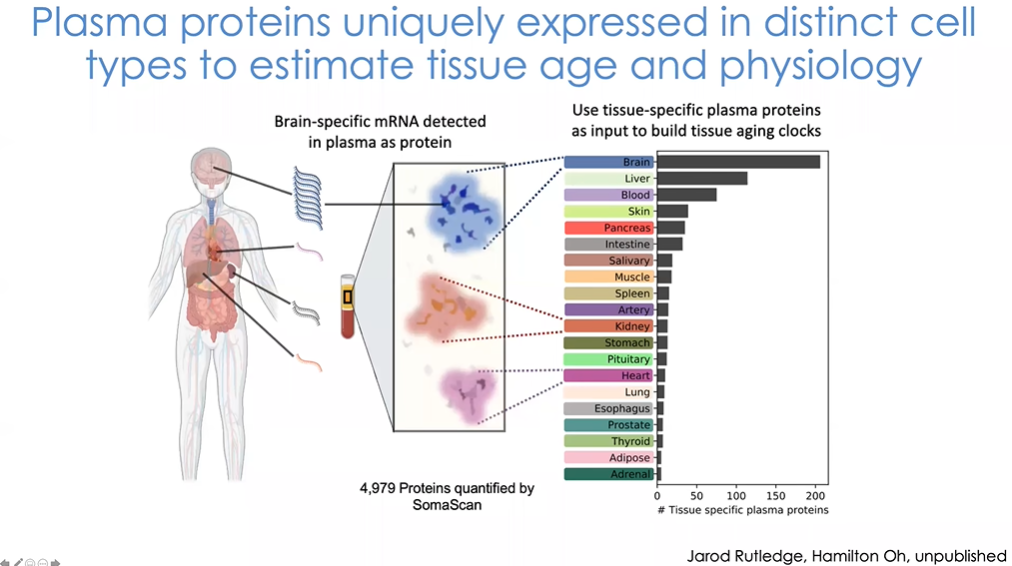
图30 通过观察具有组织特异性的特定蛋白质,我们可以推测其来源,同时观察它们是否能够反映其组织功能
具体来说,我们从数千名受试者的血浆中获得约5000个蛋白质,并探究每种蛋白质的来源。我们借助基因表达分析、gtext及Tabula Sapiens细胞图谱来研究特定蛋白表达。多数蛋白会在多种组织中表达,但约有15%的蛋白质具有器官或组织特异性。我们在5000个蛋白质中发现大约200种有较大可能来源于大脑的蛋白质,还有约120种来自于肝脏等器官。那么这些来自大脑的蛋白质是否会对我们理解大脑衰老有所帮助?
我们可以利用具有组织特异性,即仅表达在特定组织的蛋白质构建所谓的“组织时钟(tissue clock)”,其中可以看到免疫细胞中的表观遗传标记随实际年龄的增长发生了惊人变化。
我们为每个存在组织特异性蛋白的组织构建了组织时钟,用于了解人体各器官的生理年龄以及生理状态。
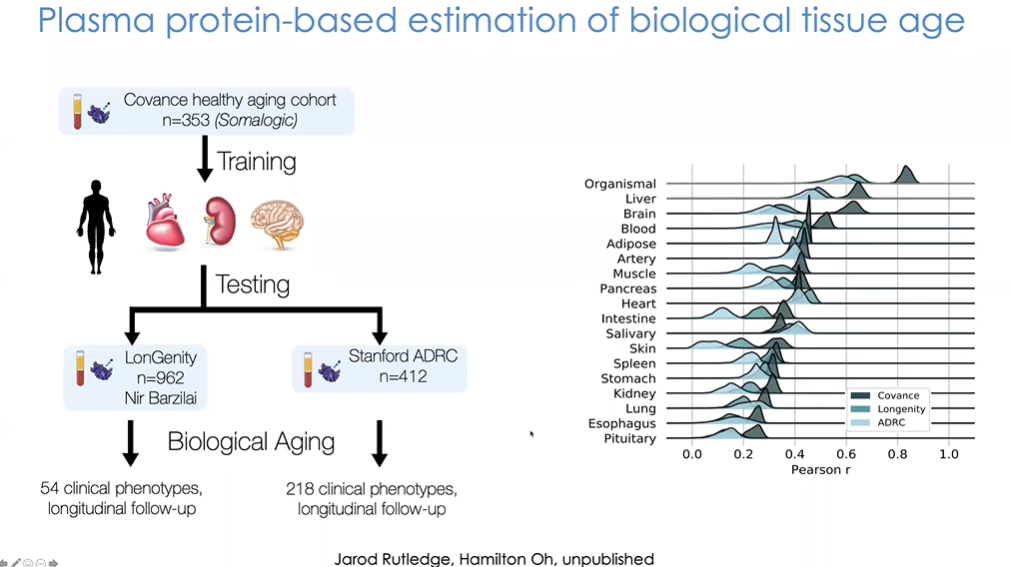
图31 建立了心脏、肾脏、大脑时钟,并在全身范围内对时钟进行了训练
在该研究中,我们与SomaLogic公司合作构建了一个正常衰老验证队列,建立了心脏、肾脏、大脑时钟,并在全身范围内对时钟进行了训练(图31)。研究中没有限制算法使用的蛋白质。接着我们将其在独立数据集中进行测试。其中一个来自于Nir Barzilai的长寿研究和百岁老人研究,另一个是斯坦福对早期阿尔茨海默病、帕金森病以及痴呆患者的研究。
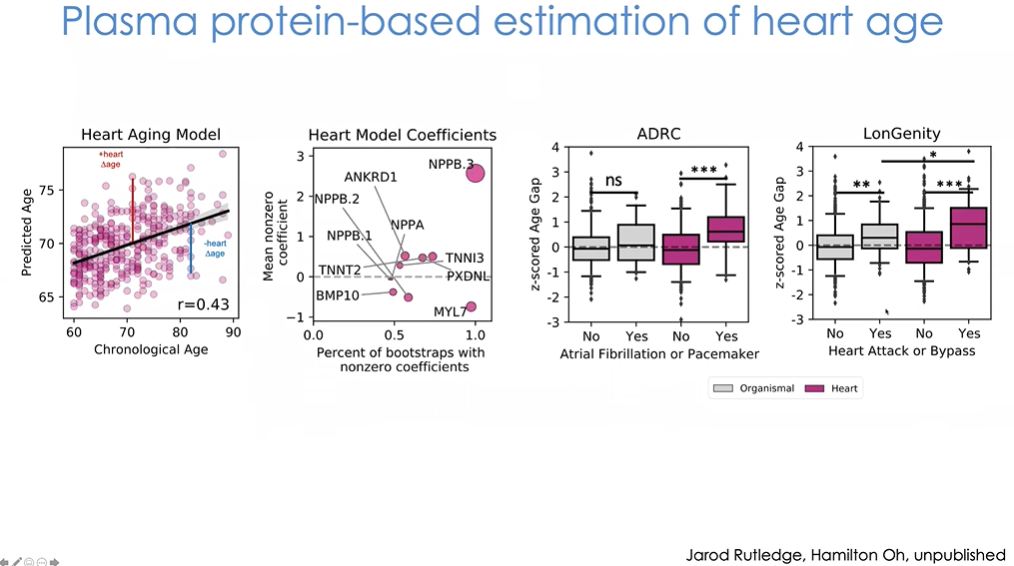
图32 心脏时钟
我们为每个器官都建立了时钟,这里仅展示个别例子。对于其中一部分受试者,我们建立了心脏时钟(图32),只要知道个体的实际年龄,就能够计算出其心脏年龄,这一过程中我们知道时钟包含了哪些蛋白质。有趣的是,该算法采用了两种临床常用的生物标志物:b型钠尿肽和肌钙蛋白,这是临床中存在心脏问题的老年患者需要检测的两项指标。同时我们还采用了其他几种参与心脏功能与衰老的蛋白质。在ADRC中使用生物体时钟,我们观测不到使用起搏器或存在房颤的受试者间有何差异,因此生物体蛋白质组时钟在此没有发挥作用。而当我们使用仅包含8个蛋白质的心脏特异性时钟时,使用起搏器或存在房颤的受试者在ADRC和LonGenity队列中都表现出明显差异。实际上在LonGenity中,生物体时钟是有效的,但显然单独使用心脏特异性蛋白质会有更好的预测结果。
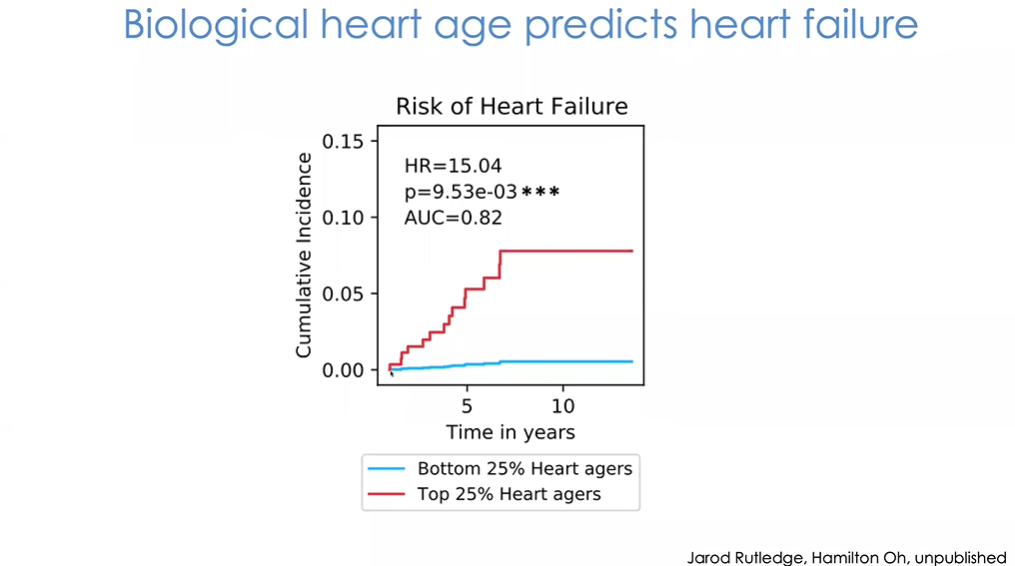
图33 基于心脏生理年龄预测心力衰竭风险
该领域长期研究更加有趣。研究中我们在第0年采集受试者血浆,然后对其进行15年以上的跟踪以获得后续数据(图33)。预测中心脏生理年龄较小的25%的受试者心脏功能完好,几乎没有受到心脏病影响,或只有轻微影响;而心脏生理年龄最高的25%人群,患心脏病的风险增加了15倍。
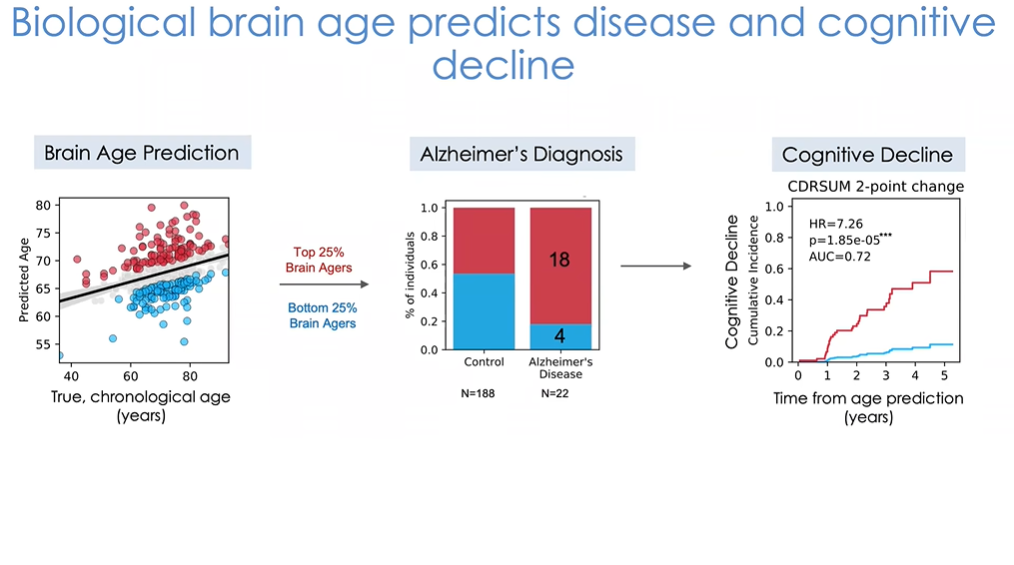
图34 基于大脑生理年龄预测认知衰退风险
对大脑的研究也得出了类似数据(图34)。同样的,我们使用个别大脑特异性蛋白来预测受试者脑部的生理年龄。在阿尔茨海默病研究队列中,22人中有18人为大脑老化前25%人群,仅有极少数人为后25%。同样我们在第0年采集受试者血样,并进行5年以上的跟踪,会发现那些预测中脑部年龄更大的受试者遭遇认知功能下降或丧失的风险增加了7倍,而模型中脑部年龄较小的受试者在此期间则会保持脑部功能的相对稳定。这些只是早期数据,我们目前正与华盛顿大学等院所进行合作,进一步验证以上发现。
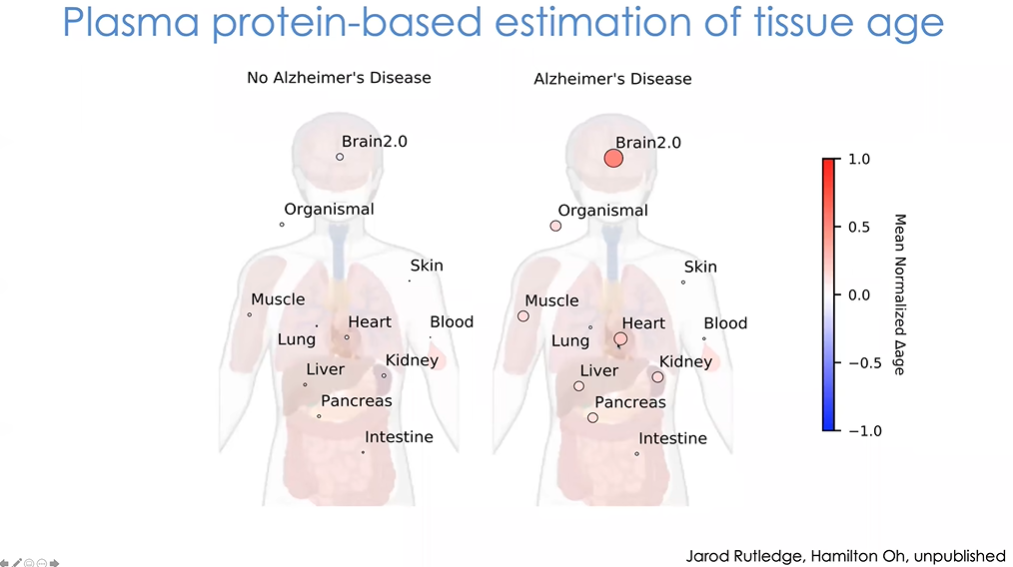
图35 身体各组织相对年龄
我们可以基于个体制作这样的图谱,图中能够直观看到身体中每个组织的相对年龄(图35)。我们再次看出,阿尔茨海默病患者的脑部年龄平均更大,同时他们的心脏及部分其他组织也呈现出加速老化的趋势。此外,阿尔茨海默病和痴呆与心血管疾病之间也有着公认的联系。
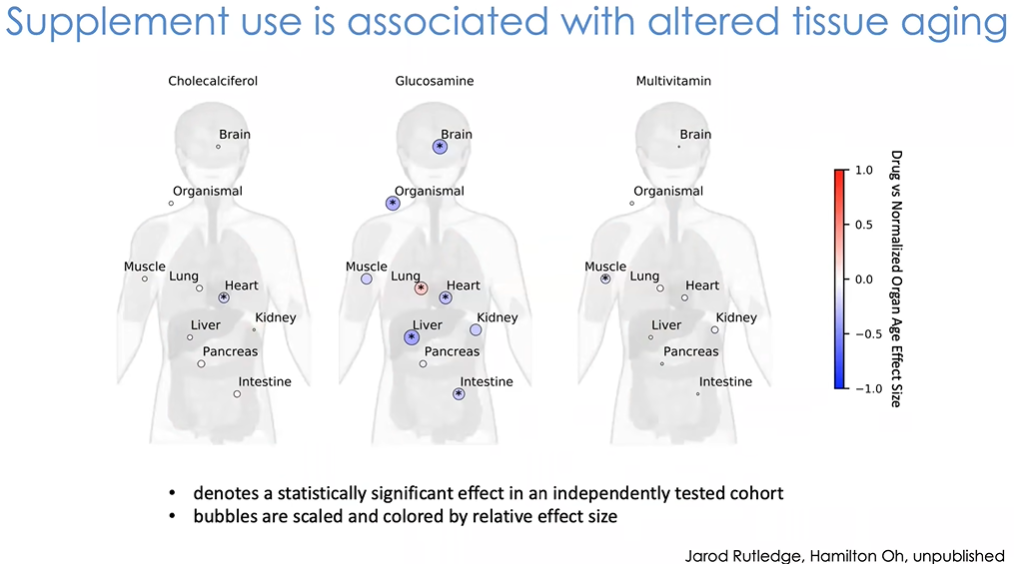
图36 使用特定补剂对于延缓衰老具有积极作用
另一个让人兴奋的发现是,使用特定补剂对于延缓衰老具有积极作用(图36)。例如研究中服用维生素D的受试者,其心脏年龄显著较小。服用氨基葡萄糖(glucosamine)补剂的受试者,其体内多种组织都相对未服用者更加年轻。接下来我们希望进一步优化现有结果,通过实际干预手段获得更多信息。人的年龄如何发生变化?各组织时钟的生物通路是什么?其生物学意义是什么?希望在未来,我们能够招募到组织状态符合特定临床干预手段的受试者,具体来说就是根据其组织状态判断特定疾病的患病风险,在患病前实施干预。例如现在已知的,大脑加速老化的人群有患阿尔茨海默病的风险,肾脏加速老化的人群可能患高血压,心脏加速老化的人群可能患心脏病等。

最后,非常感谢我们的合作者以及实验室成员,同时特别感谢对以上研究数据做出贡献的研究者们。



